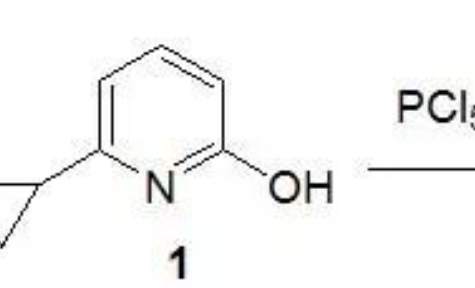
三光氣和胺反應制備脲,主要分為兩種方法,一種是和伯胺先生成異氰酸酯中間體,另外一種是和仲胺先生成氯甲酰胺中間體。
除了一些常用的伯胺的異氰酸酯可以購買到以外,在藥物化學中決大多數異氰酸酯是無法購得的,因此需要自己合成異氰酸酯。常用異氰酸酯的合成方法是伯胺與三光氣反在堿性條件下生成異氰酸酯,而后異氰酸酯與另一分子胺反應生成脲,第二步反應其實同前。對于低沸點的異氰酸酯,第一步反應完后最好將其蒸餾出來,再投第二步反應,這樣下一步產物相對干凈。如果異氰酸酯沸點很高,一般生成異氰酸酯后,直接一鍋用到下一部,但必須嚴格控制三光氣的用量(注意三光氣用底物胺的1/3的量)。光氣與雙光氣也適用本方法,但考慮到使用的方便性和安全問題,一般使用三光氣。
異氰酸酯與胺反應成脲是最為方便的一種方法,特別對于那些可以直接在市場上買到的異氰酸酯,一般這類反應收率也很高。但本方法最重要的一點是:反應物的用量是取決于底物的活性。通常是等量的底物在非質子性溶劑反應,加入適量的堿有利于反應的進行。如果其中一個底物的活性較差的話,可以適當增加用量。常用的溶劑有:二氯甲烷、四氫呋喃等。
三光氣與伯胺反應生成脲示例(Tetrahedron, 2002, 639-652)

將三光氣(0.99 g,3.3 mmoL)溶液加入到100 mL干DCM中3-氯-4-硝基苯胺(1.72 g,10 mmoL)和二異丙基乙胺(2.1 g,20 mmoL)的攪拌溶液中。將所得混合物在0℃攪拌3小時,然后用苯胺(930mg,10 mmol)處理。將反應混合物加熱至室溫。除去溶劑后,殘留物在乙酸乙酯和飽和碳酸氫鹽溶液之間分離。分離有機層,用鹽水沖洗,在無水Na2SO4上干燥并過濾。將過濾液濃縮到殘渣中,通過硅膠柱層析純化殘渣,得到1.9g 1-(3-氯-4-硝基-苯基)-3-苯基脲(65%)。
異氰酸酯與胺反應生成脲示例(J. Med. Chem. 2005, 1697-1700)

向3-氯-4-硝基苯胺(1.72 g,10 mmoL)和三乙胺(3 mL,20 mmoL)和100 mL THF的溶液中逐滴添加二氰基苯(1.19 g,10 mmoL)和10 mL THF。添加完成后,將得到的混合物放入水中(150 mL)之前,使其升高室溫并攪拌過夜。用DCM(3×100毫升)提取混合物。用鹽水洗滌合并的有機相,在無水Na2SO4上干燥并過濾。濾液經濃縮得到粗品,經柱純化得到2.4g 1-(3-氯-4-硝基-苯基)-3-苯基-尿素(80%)
二、 三光氣先和仲胺生成氯甲酰胺制備脲
對于仲胺由于無法形成異氰酸酯,我們可以通過其與三光氣反應得到氯甲酰胺然后再與另一個胺反應。一般仲胺的氯甲酰胺中間體對水是穩定的,可以分離純化出來。

三光氣與仲胺反應氯甲酰胺 ( J. Org. Chem. 2004, 3787-3793)

向2-烯丙基哌啶(0.63 g,5 mmol)和吡啶(0.52 g,6.6 mmol)在50 mL二氯甲烷中的溶液中添加三光氣(0.66 g,2.2 mmol)在10 mL二氯甲烷中的溶液,在0℃下滴加40 min以上。然后將所得混合物加熱至室溫并攪拌至文光。將反應混合物逐滴加入50毫升1 N HCl水溶液。分離后,用DCM(3x 50mL)萃取水相。用飽和的DNAHCO3溶液和鹽水(3 x 50 mL)洗滌組合的有機相,然后在硫酸鎂上干燥。除去溶劑后,粗品進入Et2O,固體被過濾。濾液濃縮至860mg氨甲酰氯為黃油(92%)。
氯甲酰胺與胺反應脲

將2-烯丙基哌啶-1-羰基氯(1.87 g,10 mmol)、三乙胺(5 mL)和4-氯-3-氟苯胺(1.7 g,12 mmol)在100 mL無水二氧六環中的溶液在室溫下在氮氣中攪拌26 h,然后在真空下濃縮至干燥。殘渣溶解于100毫升二氯甲烷中,用0.5 N的水氯化鈉溶液和鹽水洗滌,在無水Na2SO4上干燥并過濾后,濾液濃縮至粗品,用快速柱層析法純化,得到2-烯丙基哌啶-1-羧酸(4-氯-3-氟-苯基)-酰胺(2.3g,77%)
本文內容整理自網絡,版權歸原作者所有