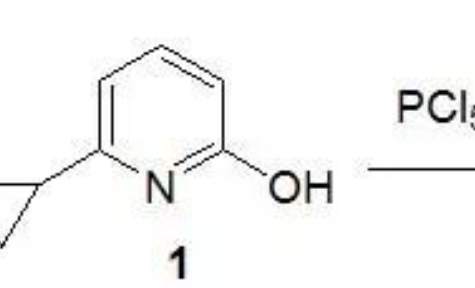
在催化量的四氧化鋨和共氧化劑的存在下,烯烴被氧化成鄰二醇。通過其他的試劑較難實現的烯烴轉化成鄰二醇通過此方法能很溫和平穩的進行。盡管鋨價格相對昂貴,毒性很大,但四氧化鋨作氧化劑進行烯烴的雙羥基化是一種較好的順式羥基化的方法,收率高。
反應常用丙酮/水、或者t-BuOH/水的混合溶劑體系。
由于四氧化鋨價貴且有毒,實驗中常用催化量的四氧化鋨和其他的氧化劑,如與氯酸鹽、碘酸鹽、過氧化氫等共用,或者用揮發度較低的鋨酸鉀代替。作為共氧化劑、處理操作方便的固體試劑N-甲基-N-氧化嗎啉(NMO)是最常用的(Upjohn法)。其他的氧化劑如氧化三甲胺(Me3NO)、t-BuOOH(Milas法)、OsCl3-K3Fe(CN)6等也被使用。用高碘酸鈉(NaIO4)做共氧化劑時,生成的二醇會被繼續氧化斷裂,生成相應的羰基化合物(Lemieux-Johnson酸化)。
反應歷程,形成環狀的鋨酸酯。由于鋨酸酯不穩定,常加入叔胺(如吡啶)組成配合物,以穩定鋨酸酯,加速反應。加入甲磺酰胺(MsNH2)也能起到加速反應的效果(MsNH2能促進中間體鋨酸酯的水解)。
反應機理
四氧化鋨與烯烴發生[3+2]加成、生成鋨酸酯中間體。使催化劑再生,必須通過加水分解餓酸酯。為此,反應通常在含水體系中進行。該加水分解是該催化體系的限速步驟。
反應實例
一、高碘酸鈉做共氧化劑時、一鍋法是烯烴氧化斷裂。2,6-二甲基吡啶添加在體系中可防止副反應。 Org. Lett. 2004, 6, 3217
Org. Lett. 2004, 6, 3217
二、氯胺-T等共存下、可以發生醇胺化。
J. Org. Chem. 1976, 41, 177
三、用磺酰氧胺基甲酸酯給分子內引入胺基的例子。 J. Am. Chem. Soc. 2006, 128, 2514
J. Am. Chem. Soc. 2006, 128, 2514
四、分子中含醇羥基的底物,能發生氧化環化反應。 J. Am. Chem. Soc. 2006, 128, 13704
J. Am. Chem. Soc. 2006, 128, 13704
五、苯硼酸存在下反應進行時,反應性有明顯的改善,同時、二醇以苯硼酸酯的形式易于分離。以下是用該條件合成Sordarin的實例。 J. Am. Chem. Soc. 2006, 128, 6931
J. Am. Chem. Soc. 2006, 128, 6931

2-〔4(芐氧羰基)哌嗪-1-基〕- 4〔反式(2-丁烯-1-基)氧基〕喹唑啉(1.30 g),四叔丁基四氧化鋨溶液(四氧化鋨106mg/t-丁醇8.36克)(312 mg)和4-甲基嗎啉N-氧化物(382毫克)在水中(2毫升)的混合物-丙酮(15毫升)在室溫下攪拌14小時。
從反應混合物中減壓蒸餾丙酮,用乙酸乙酯稀釋產物,用10%亞硫酸鈉水溶液和水沖洗混合物。.乙酸乙酯溶液經無水硫酸鎂干燥減壓蒸干,殘渣經中壓液相色譜(洗脫液,氯仿:甲醇=100:1,v/v)純化,得2-[4-(芐氧羰基)哌嗪-1-基]-4-[(2RS,3RS)-(2,3-二羥丁烷-1-基)氧基]喹唑啉(1.02g)泡沫。