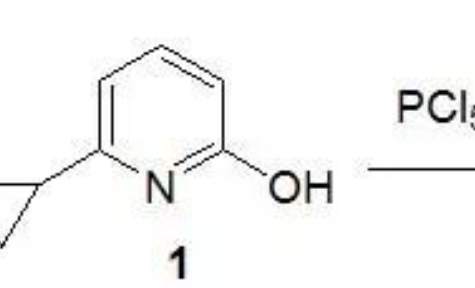
磺酸酯,如甲磺酸酯,對甲苯磺酸酯在極性非質子溶劑(DMF,CH3CN, DMSO等)中與堿金屬氟化物發生親核取代反應,得到氟化合物。
堿金屬氟化物在非質子溶劑中活性如下:CsF>KF>NaF>LiF。CsF的活性最高,但由于KF價格相對便宜,所以最常用。
反應體系中加入冠醚等相轉移催化劑會加快反應進行,提高產率。
有的底物在離子液體中進行反應,能得到很好的結果。如下這個反應在離子液體[bmim]BF4中進行,產率相當高。
【Kim, D, W. Song, C, E. Chi, D, Y. J. Org. Chem. 2003, 68,4281-4285】
黃原酸酯也能被取代生成氟化物。

【Keon, M, J. LeGuyader, F. J. Chem. Soc.Chem.Commu. 1995, 25,1241】
反應實例

將CsF(760mg,5 mmol)添加到2-(3-甲磺酰氧丙基)萘(264 mg,1.0 mmol)、[bmim]-[BF4](3.0 mL)和H2O(90μL,5 mmol)在乙腈(3.0 mL)中的混合物中。將混合物在100℃下攪拌20分鐘。用薄層色譜法監測反應。用乙醚(7mL×3)從離子液相萃取反應混合物。乙醚層在硫酸鈉上干燥并在減壓下蒸發。用硅膠(5%EtOAc/正己烷)快速柱層析法純化產物,得到2-(3-氟丙基)萘(179mg,95%)無氯油。
【Kim, D, W. Song, C, E. Chi, D, Y. J. Org. Chem. 2003, 68,4281-4285】
對甲苯磺酸酯與TBAF反應

將四丁基氟化銨(TBAF)在THF(14ml,1M)中的溶液加入到無水THF(15ml)中的甲苯磺酸(0.78g,1.8mmol)溶液中。然后將反應混合物回流4h。減壓去除揮發物,殘渣溶解在乙酸乙酯(80ml)中。用水(30ml)、鹽水(30ml)和飽和NaHCO3水溶液(30ml)洗滌有機溶液。然后在Na2SO4上干燥有機層。過濾后,減壓濃縮濾液,用乙酸乙酯/正己烷(30/70,v/v)硅膠柱層析純化殘渣,得到無色油狀物(0.29 g,57%)。
【Zhude Tu, et al. J. Med. Chem., 2011, 54 (6), 1555–1564】
甲磺酸酯與TBAF反應

將TBAF(1 M in THF,0.20 mL)添加到8(27 mg,0.05 mmol)無水THF(10 mL)的溶液中。將混合物回流4h,然后冷卻至室溫。用乙酸乙酯進行標準檢測后,用硅膠色譜法(正己烷/乙酸乙酯=1:1)純化殘渣,得到22 mg 9(94.0%)。
【Masahiro Ono, et al J. Med. Chem., 2011, 54 , 2971–2979】
甲磺酸酯與CsF反應

將CsF(456mg,3.0 mmol)加入2-(3-甲磺酰氧基)萘(280 mg,1.0 mmol)與叔戊醇(4.0 mL)的混合物中。將混合物在80℃下攪拌6小時。用乙醚研磨反應混合物以去除大部分離子鹽。濾液在減壓下蒸發。殘渣經快速柱層析法(20%CH2Cl2/己烷)純化,得到192 mg(94%)2-(3-氟丙氧基)萘,為無色油,含醚副產物。
【DongWook Kim et al. J. Org. Chem. 2008, 73, 957-962】
甲磺酸酯與TBAF(tBuOH)4反應

將市售水合TBAF(1.0g,3.17mmol)添加到t-BuOH(88ml)和正己烷(22ml)中。將混合物在90℃下攪拌30分鐘。在此期間,TBAF完全溶解。溶液冷卻至室溫,沉淀出白色結晶固體。用40毫升70%叔丁醇/正己烷快速過濾和洗滌結晶固體。濾液在真空中保留15-20分鐘以除去殘留溶劑,得到TBAF(tBuOH)4(1.63g,2.92mmol)白色結晶固體,產率92%。
將TBAF(t-BuOH)4(1.1g,2mmol)加入甲磺酸(280mg,1.0mmol)在CH3CN(4.0ml)中的溶液中。將混合物在70℃下攪拌1.0 h。殘渣溶于水(6.0ml),用乙醚(6.0ml×3)從水相中萃取。將有機層干燥(硫酸鈉)并減壓蒸發。用短柱層析法(5%乙醇酸/己烷)純化殘渣,得到2-(3-氟丙氧基)-萘(200 mg,98%)作為無色油
【Dong Wook Kim et al. Angew. Chem. Int. Ed. 2008, 47, 8404 -8406】
相關鏈接
【氟化反應】磺酸酯參與的氟化反應
版權歸原作者所有,如有版權問題,請聯系刪除。