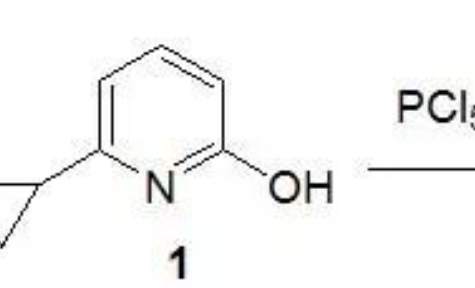
1. 脫羧氟化

Decarboxylative Fluorination of Electron-Rich Heteroaromatic Carboxylic Acids with Selectfluor
Xi Yuan Jian-Fei Yao and Zhen-Yu Tang
Org. Lett. 2017, 19, 1410?1413
DOI: 10.1021/acs.orglett.7b00335
文摘:報道了富電子五元雜環芳烴呋喃、吡唑、異惡唑、噻吩、吲哚、苯并呋喃和吲唑羧酸的過渡金屬無羧基氟化反應。對含氮雜環羧酸如吲哚和吡唑進行了氟化二聚體的觀察。研究了以Li2CO3為堿,在低溫下合成2-和3-氟吲哚單體的有效方法。

Practical Access to Difluoromethyl Ketones via Straightforward Decarboxylative Difluorination of β-Ketoacids
Yin-Long Li, Jian Li and Jun Deng
Adv. Synth. Catal. 2017,Advance Article
DOI: 10.1002/adsc.201601315
文摘:介紹了由β-酮酸合成一系列二氟甲基酮的簡便方法。這種轉化是通過β-酮酸在沒有任何催化劑的情況下直接脫羧基二氟化實現的。此外,所得到的二氟甲基酮可以很容易地轉化為相應的二氟甲基化藥物和材料的構建塊。
2. 烯烴三氟甲基化

Metal-free andlight-promoted radical iodotrifluoromethylation of alkenes with Togni reagentas the source of CF3 and iodine
Redouane Beniazza, Maxime Douarre, Dominique Lastécouèresand Jean-Marc Vincent Chem. Commun., 2017, Advance Article
DOI: 10.1039/C7CC00214A, Communication
文摘:建立了烯烴碘三氟甲基化的光催化方法。首次利用Togni試劑作為CF3基和碘原子的來源。初步的機理研究表明,CF3I和2-碘苯甲酸都是碘原子轉移到產物中的直接來源。
3. 吲哚烷基化

Cs2CO3-catalyzed alkylation ofindoles with trifluoromethyl ketones
Tetrahedron 73 (2017) 2283-2289
Doi:10.1016/j.tet.2017.03.012
文摘:介紹了一種Cs2CO3催化吲哚與三氟甲基酮的烷基化反應。雙鹵環和芳香三氟甲基酮以及各種取代吲哚與本方法相容。以三氟甲基取代的叔醇2,2,2-三氟-1-(1H-吲哚-3-基)-乙烷-1-醇為原料,得到了較好的產率。
之前我們介紹過芳雜環直接氟化法,主要為單氟取代,詳情請點擊:
芳雜環間接氟化法
接下來我們將介紹一下芳雜環碳氫鍵的三氟甲基化方法,并對常見的幾類方法進行簡單的匯總。
由于三氟甲基的強電負性,高穩定性和良好的脂溶性,三氟甲基的引入,往往使化合物的性質,特別是其生理活性發生顯著的改變,其在新藥開發中越來越被關注。所以如何將三氟甲基引入目標分子,成為氟化學中的一個重要的課題。經過多年的研究,已經發展了許多引入三氟甲基的方法,近年來通過C-H鍵活化實現C-CF3的構建成為研究的熱門方向。
示例1
2011年,Baran課題組報道了經由三氟甲基自由基的含氮雜環碳氫鍵的直接三氟甲基化方法。該反應在室溫下進行,條件溫和,官能團耐受性好,包括吡啶、吲哚、吡咯、吡嗪、嘧啶、咖啡因在內的雜環都是合適的底物。該反應使用Langlois試劑CF3SO2Na在氧化劑過氧叔丁醇存在下失去一分子二氧化硫產生三氟甲基自由基,再對雜環發生原子轉移/自由基加成形成中間體[ArHCF3]·以及被氧化劑過氧叔丁醇單電子氧化,失去質子得到最終三氟甲基化的產物。該反應使用的三氟甲基試劑和氧化劑都需要很大當量,但由于這些試劑本身廉價易得,且反應即使放大至克級,也能以較高的產率進行,充分證明了該方法的實用性。

雜環的三氟甲基化:標準程序:在二氯甲烷(1毫升)和水(0.4毫升)在0℃時,將雜環(0.25 mmol,1當量)和三氟甲基亞磺酸鈉(117毫克,0.75 mmol,3當量)在0℃緩慢加入叔丁基過氧化氫(70%溶液在水中,0.17毫升,1.25毫摩爾),5.0當量),劇烈攪拌,使反應升溫至室溫,并通過薄層色譜法監測,直至完成。對于不在24小時內完成的底物,可以加入第二次添加三氟甲基亞磺酸鈉(3當量)和叔丁基過氧化氫(5當量)以驅動反應完成。原料消耗后,反應在二氯甲烷(2.0毫升)和飽和碳酸氫鈉(2.0毫升)之間進行分配。分離有機層,用二氯甲烷(3x 2.0ml)萃取水層。有機層用硫酸鈉干燥,濃縮,硅膠柱層析純化。
示例2
2010年,余金權課題組報道了鈀催化導向鄰位碳氫鍵活化構筑C-CF3鍵。該反應從二價鈀啟動,在導向基團吡啶的作用下形成二價環鈀物種,在親電型三氟甲基化試劑Umemoto試劑的作用氧化到高價鈀(三價鈀或四價鈀),并且形成Pd-CF3鍵,再還原消除得到鄰位三氟甲基化的產物。該反應利用了高價鈀有利于芳基和三氟甲基之間的還原消除,但需要鄰位導向基團極大地限制了這一反應的應用。

鈀(OAc)2催化鄰三氟甲基化的一般程序:
在20毫升密封管中,將2-苯基吡啶2a(0.2 mmol,1.0當量)、Pd(OAc)2(4.5毫克,0.02 mmol,0.1當量)、Cu2(36.3毫克,0.2 mmol,1.0當量)和5-(三氟甲基)-二苯并噻吩四氟硼酸鹽1b(102.0毫克,0.3 mmol,1.5當量)溶于空氣中的1.0毫升干燥二氯乙烷中,然后將三氟乙酸(148.6μl,添加2.0 mmol,10當量)。用聚四氟乙烯內襯蓋密封管,并在110℃下攪拌反應混合物48小時。冷卻至室溫后,用含水NaOH(2n,8ml)和飽和Na2S溶劑(8ml)對混合物進行淬火,并用二氯甲烷(15ml×3)小心萃取。溶劑在真空下除去,殘渣用正己烷和乙酸乙酯梯度洗脫液在硅膠上柱層析純化,得產品3a(收率50%)。
除了上述方式外,本文匯總了一些其他芳雜環碳氫鍵三氟甲基化方法供大家學習使用: