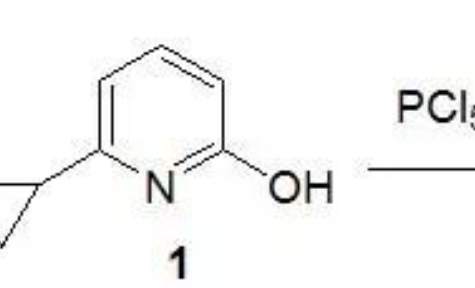
醇通過酯的保護一般用在糖化學中較為多見,一般主要通過乙酰基、苯甲酰基和特戊酰基等。乙酰基保護也常常用于天然產物結構鑒定中羥基衍生化。一般上乙酰基方法較多,其中用乙酸酐在吡啶中引入乙酰基最為常用,由于該方法不能乙酰化位阻較大的叔醇,要想在叔醇引入乙酰基需要加入酰化催化劑(DMAP, 4-PPY)等,有時對位阻特別大的即使加入酰化催化劑(DMAP, 4-PPY)也無效時,可以考慮通過Lewis酸催化,Procopiou P. A.等人報道利用TMSOTf催化位阻較大的叔醇的乙酰化(J. Org. Chem. 1998, 2342),效果要比Ac2O/DMAP體系更好(J. Org. Chem. 1998, 2342)。苯甲酰化的常用方法是BzCl或Bz2O/吡啶。特戊酰化的常用方法是PvCl /吡啶, 0-75℃。這些酰基化對伯醇選擇性要大于仲醇,選擇性特戊酰基>苯甲酰>乙酰基;有時特戊酰基可化學選擇性的上在伯醇上。
一、乙酰化保護羥基示例 (DMAP: J. Org. Chem. 1993, 3791)

化合物1(1.38 g,10 mmol)和Ac2O(0.95 mL,10 mmol)在CH2Cl2(30 mL)中用Et3N(2 mL,10 mmol)和DMAP(122 mg,1 mmol)在20℃下處理,攪拌4 d。用CH2Cl2稀釋混合物,用2 M HCl、NaHCO3、H2O洗滌,干燥,用乙酸乙酯-環己烷(1:3)硅膠洗脫,1: 提供二乙酸鹽(2)(500mg,22%)、鄰芳基乙酸鹽(3)(705mg,39%)和鄰烷基乙酸鹽(4)(54mg,3%)。
二、 苯甲酰化保護羥基示例( J.Org.Chem. 1981, 46, 5252)

向吡啶(20 ml)中的1(0.94 g.2.9 mmol)溶液中加入苯甲酰氯(1.26 g.9 mmol),攪拌并冰冷卻。在室溫下攪拌過夜。將混合物倒入冰水中,用苯萃取。苯萃取物用水洗滌、干燥并蒸發以留下淡黃色焦糖(l.62 g),用i-PrOH研磨以形成晶體。這些都是由i-PrOH共晶無色板,m.p.106-107.5oC,產率1.31g(85%)
三、 特戊酰基保護羥基示例 (J.Am.Chem.Soc. 1980,102,7962)

將三醇1(3.24 g,20 mmol)溶解在吡啶(20 mL)中,并添加干燥的二氯甲烷(20 mL)。在低溫(0oC)中,在氬氣下逐滴加入新戊酰氯(2.48 mL,20 mmol),攪拌30分鐘。然后去除冷卻液,將混合物在室溫下攪拌14小時。濃縮后再共沸去除吡啶(甲苯)得到糖漿,該糖漿在硅膠(石油醚中50%的醚)上通過快速柱層析法純化,得到無氯油2,得率4.43g,(90%)
四、 乙酸酯脫保護示例 (J.Am.Chem.Soc. 1972, 94, 8613)

將1(1.59 g,6.0 mmol)和K2CO3(2 g,14.3 mmol)在甲醇(5 mL)和水(3 mL)中的混合物在室溫下攪拌12 h。將混合物在真空中濃縮至3.5 mL的體積,并用CH2Cl2(25 mL'3)萃取。提取物在硫酸鎂上干燥并在真空中濃縮,得到21.13 g(85%)。
五、苯甲酸酯脫保示例 ( J.Org.Chem. 1981, 46, 5252)

將二苯甲酸鹽1(500 mg,0.9 mmol)加入氫氧化鈉(250 mg,62 mmol)的甲醇(35 mL)溶液中,在室溫下攪拌所得混合物50 min,在真空中蒸發甲醇并加水后,用苯乙醚萃取分離出的固體。將有機提取物用水洗滌、干燥并除去溶劑。用硅膠層析得到無色焦糖2,收率360mg(90%)
六、特戊酸酯脫保護示例 (J.Am.Chem.Soc. 1990,112,3693)

將136mg(0.3mmol)的1/20ml甲醇溶液在40 mg 5%Pd/BaCO3的常壓下在室溫下氫化24小時。混合物用硅藻土墊過濾,濾液蒸發。將得到的無色玻璃溶解于10ml甲醇中,并與49mg(0.9mmol)氫氧化鈉在室溫下攪拌20h,在此期間白色晶體分離。這些被過濾,并與MeOH很好地洗滌,給予66毫克的2。濾液用HOAc中和濃縮,殘渣用制備性TLC(EtOAc/n-PrOH/H2O上相4:1:2)純化。從MeOH/95%EtOH再結晶得到額外的18mg,總收率為84mg(80%)的2。
本文非原創內容,版權歸原作者所有。