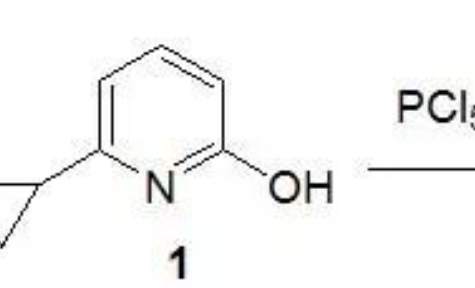
該類反應屬于典型的親核取代反應,按照反應歷程分兩種類型:單分子的親核取代反應(SN1)和雙分子的親核取代反應(SN2)。
一、單分子的親核取代反應(SN1)
單分子的親核取代反應(SN1)歷程中反應速度只與反應底物鹵代物的濃度有關,與堿的濃度無關。因此,從動力學上講它是一個一級反應。例如溴代叔丁烷的水解:

此反應是分兩步進行,第一步是反應物在溶劑中首先離解成叔丁基正離子和溴負離子:

第二步則是生成的叔丁基碳正離子再與HO-作用,生成叔丁醇:

二、雙分子的親核取代反應(SN2)
另一類為雙分子的親核取代反應(SN2),它的水解速度與鹵代烴的濃度和堿的濃度成正比,因此該類反應是一個二級反應。例如溴甲烷的水解:

反應過程中C-Br鍵的斷裂與C-O鍵的形成是同時進行的。當進攻試劑HO-從離去基團Br的背后進攻中心碳原子時(這是比較有利的進攻方式)。此時,HO- 、Br和中心碳原子幾乎處于同一直線上,形成一個“過渡態”。而中間碳上的三個H原子則處于垂直于這個直線的平面上,當HO-與中心碳原子進一步接近,最終形成一個穩定的C-O鍵時,C-Br也徹底斷裂,生成Br-離子,同時中心碳上的三個H原子也向后翻轉,使碳原子恢復成原來的sp3雜化狀態。從立體化學上來看,在反應過程中發生了構型的轉化,使得產物與原來的反應物構型正好相反,這也正是在1893年發現的瓦爾登(Walden)轉化。另外許多反應,鹵代物直接水解并不是太好,因此一般先用AcO-取代,而后再水解得到相應的醇。
反應實例
一、鹵代烴的水解反應制備醇示例

Combined the material with 75%DMF, 1.2 equiv of NaOH were stirred for 30 min at room temperature. Andrecrystallized from MeOH to give the colourless needles (95% yield).
【J.Org.Chem.1982, 47, 4024-4029】
二、鹵代烴的水解反應制備醇示例

將水(100mL)和碳酸鈣(18g,180mmol)加入10.5g(35mmol)1-溴-2-(溴甲基)萘溶液中,加入對二氧六環100mL,回流10h。在減壓下冷卻溶液并去除二氧六環。加入二氯甲烷(200mL),然后用稀鹽酸處理,直到所有固體溶解。分離有機相,用NaHCO3溶液洗滌,用硫酸鎂干燥,并過濾。溶劑的去除留下白色固體,從正己烷重結晶得到7.9g(1-溴對苯二甲酸-2-基)甲醇(95%產率)。
【J.Org.Chem.1986, 51, 3762-3768】
三、鹵代烴的乙酰氧基取代示例

將150 g獲得的1-氯-(E,Z)-7,9-十二二烯與150 g含水乙酸鉀和100 g乙酸混合,在160℃下洗滌6小時,在氮氣的氣氛中攪拌,將氯化物轉化為乙酸。。反應完成后,將反應混合物倒入大量水中,在減壓下蒸餾通過相分離得到的有機相,共蒸餾80 g 7,9-十二烯基乙酸乙酯,其中E,Z-異構體的純度至少為75%。
【Patent; Shin-Etsu Chemical Co., Ltd.; Publ.: EP241335 A1 (1987/10/14),Appl.: EP1987-400592 (1987/03/17)】
四、酯水解得到相應的醇示例

將2N氫氧化鈉(40 mL)加入5(2-乙酰氧基乙基)-2-甲基-4-苯基惡唑(16.6克)的甲醇溶液中(40 mL),攪拌30分鐘,用水稀釋,提取乙酸乙酯,乙酸乙酯層用水洗滌,過脫水硫酸鎂干燥。
然后蒸餾溶劑,用硅膠色譜法(硅膠:190g,洗脫液:異丙醚)純化殘渣wwas,得到5-(2-羥乙基)-2-甲基-4-苯唑油,收率11.7g(84.8%),核磁共振(CDCl3):2.40(3H,s),3.07(2H,t),3.20(1H,寬),3.97(2H,寬),7.23-7.80(5H,m)。
【Patent;Takeda Chemical Industries, Ltd.; Publ.: US4596816 A1 (1986/06/24), Appl.:US198】
本文非原創內容,版權歸原作者所有。