分享一篇發表在Nature Chemistry上的文章:Structure-informed design of an ultrabright RNA-activated fluorophore,通訊作者是來自美國國家癌癥研究所的John S. Schneekloth Jr教授,該課題組的研究方向是利用化學生物學方法來識別和研究與RNA結合的小分子。

在生物醫學研究領域,對RNA進行可視化和追蹤是一項關鍵任務,這有助于深入了解基因表達調控、RNA代謝以及細胞內信號轉導等諸多重要生物學過程。目前發熒光的適配體已被用于多種細胞成像研究,例如多色RNA成像,單分子光譜以及傳感器等。在RNA適配體中,Mango是一種表征明確的系統,它能與噻唑橙(TO)及相關染料緊密結合,例如Mango與TO-生物素衍生物的親和力能達到納摩爾級。Mango折疊成一種復雜的G四鏈體,并通過將TO熒光團限制在平面構象中來實現熒光發射。Mango II 型適配體含有一個定義明確但具有可塑性的口袋,能夠以多種方式結合TO衍生物。目前,有關Mango系統的大部分工作都集中在改進適配體,或對TO熒光團進行合理修飾以改變親和力和激發/發射性質等。
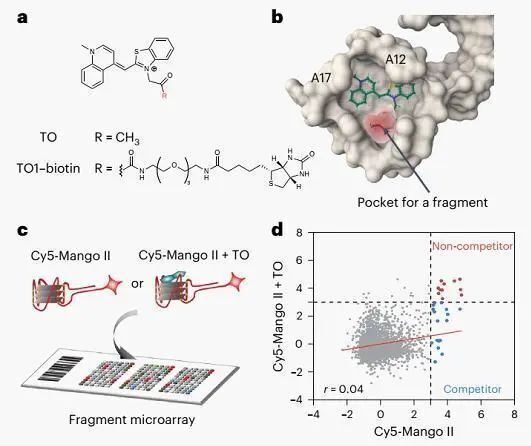
為了開發新一代高亮度、高親和力的RNA激活熒光團,本文作者通過結構信息指導的合理設計,基于Mango系統和基于片段的高通量篩選,構建了一種超亮的RNA激活熒光探針SALAD1,顯著提高探針對RNA的檢測靈敏度和特異性,為RNA相關研究提供一種有力工具。

為了開發新型TO衍生熒光團,作者首先分析了Mango中配體的結合口袋,并發現配體結合口袋是疏水性的,而且對于不連接生物素的TO而言,口袋內存在一個空位,可以容納一個單獨的片段,該片段可能通過TO上的甲基基團連接,從而提高結合力。
基于片段的藥物設計可以從弱但特異性強的低分子量配體快速開發出針對靶點的緊密而特異的小分子結合體。于是,作者就開發了片段微陣列來篩選有或沒有TO的Mango結合配體。作者通過將片段與TO連接,產生了多種染料,其結合親和力達到亞納摩爾級。作者初步篩選到11個片段候選者,并利用滴定實驗進行了熒光強度測定。從中作者發現F2顯示出最強的的熒光,并且通過進一步的實驗證明了F2與TO-Mango II 復合物的結合。
在觀察到非共價結合的F2可增強TO的熒光后,作者將TO與F2及相關化合物連接,設計合成了一系列的熒光探針,并發現其中一種化合物(SALAD1)具有最好的效果,其亮度比TO1生物素提高了3.5倍。
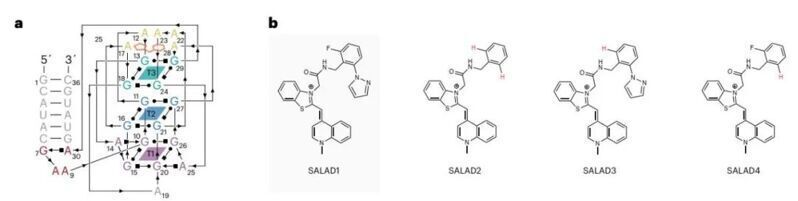
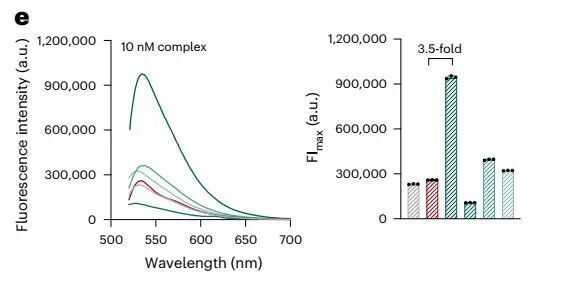
總而言之,本文作者通過結構信息指導的合理設計,構建了一種超亮的RNA激活熒光探針,顯著提高探針對RNA的檢測靈敏度和特異性。
本文作者:MB
責任編輯:LZ
DOI:10.1038/s41557-025-01832-w
原文鏈接:https://doi.org/10.1038/s41557-025-01832-w








