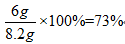實驗產率的計算
有機化學反應中,理論產量是指根據反應方程式計算得到的產物的數量,即原料全部轉化成產物,同時在分離和純化過程中沒有損失的產物的數量。
產量(實際產量)是指實驗中實際分離獲得的純粹的數量。
產率是指實際得到的純粹產物的質量和計算的理論產量的比值,

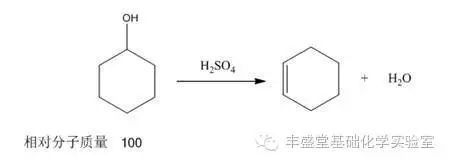
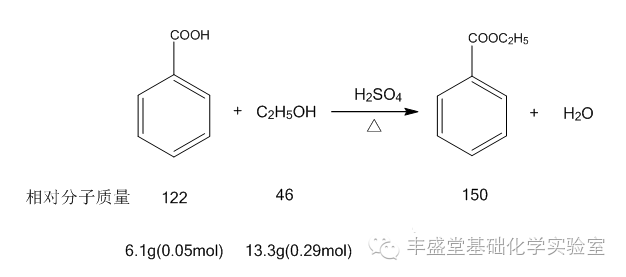
用10g環己醇和催化量的硫酸一起加熱時,得到6g環己烯,試計算它的產率? 根據化學反應式:1mol環己醇生成1mol環己烯,今用10g即(10/100)mol=0.1mol環己醇,理論上得0.1mol環己烯,理論產量為82g?mol-1×0.1mol=8.2g,但實際產量為6g,所以產率為 在有機化學實驗中,產率通常不可能達到理論值,這是由于以下一些因素影響所致: 可逆反應。在一定的實驗條件下,化學反應建立了平衡,反應物不可能完全轉化成產物。 有機化學反應比較復雜,在發生主要反應的同時,一部分原料消耗在副反應中。 分離和純化過程中所引起的損失。 為了提高產率,常常增加其中某一反應物的用量。究竟選擇哪一個物料過量要根據有機化學反應的實際情況,反應的特點,各物料的相對價格,在反應后是否易于除去,以及對減少副反應是否有利等因素來決定的。下面是在這種情況來計算產率的一個實例。 用6.1g苯甲酸,17.5mL乙醇和2mL濃硫酸一起回流,制得苯甲酸乙酯6g。這里,濃硫酸是該酯化反應的催化劑。 從反應方程式中各物料的物質的量之比很容易看出乙醇是過量的,故理論產量應根據苯甲酸來計算。0.05mol苯甲酸理論上產生0.05mol即(0.05×150)mol=7.5g苯甲酸乙酯。產率為 摘自 《有機化學實驗》-蘭州大學 編