▲第一作者:張健;通訊作者:何靜
通訊單位:北京化工大學
論文DOI:10.1021/acscatal.9b03245
全文速覽
飽和含 N 雜環化合物是構成生物活性藥物和天然產物的核心架構。目前,飽和含 N 雜環化合物的制備主要由不飽和 C=C/C=N 鍵加氫或貴金屬配合物均相催化 C-C 或 C-N 鍵構建。因此亟需發展一種綠色、高效合成飽和含 N 雜環化合物的方法及催化體系。本工作設計了一種負載型納米 Ni 催化劑,同時構筑 C-C/C-N 鍵,Ni0 和 Niδ+ 協同催化乙醇和 2-氨基芐醇高效轉化為 1,2,3,4-四氫喹啉(THQ)及其衍生物。
背景介紹
乙醇可廣泛來源于化石資源和生物質資源:既可由乙烯水合制得,也可通過生物質發酵獲得,還可由天然氣一步轉化直接合成或經由二甲醚、醋酸酯或草酸酯等路線合成。與“明星分子”甲醇相比,乙醇分子中化學鍵更加豐富,其既可直接進行 C-C 加成或羰基插入轉化為高值化學品,也可經由乙醛進行豐富的化學轉化,乙醇轉化不僅具有重要的科學意義,而且可延長產業鏈,促進資源有效利用和相關產業可持續發展,具有重大的實用價值。
C-N 鍵構建是制備含 N 化合物的重要途徑。2016 年,Min Zhang 教授(Org. Lett. 2016, 18, 724?727) 報道了在外加液體堿條件下,均相 Ru 配合物催化醇和胺基醇同時構建 C-C/C-N 鍵,為高效構建 C-N 鍵提供了新方法,同時也為乙醇分子的轉化利用指明了新方向。
研究出發點
催化醇和胺基醇轉化同時構建 C-C/C-N 鍵包含醇脫氫、醛氨/aldol 雙重交叉縮合、氫轉移過程,因此不僅要求催化劑同時具有金屬催化中心和酸堿催化中心,同時還要求金屬催化與酸堿催化之間協同作用。對此,本工作提出同時具有酸堿中心的復合氧化物負載Ni催化劑,以實現 C-C/C-N 鍵的同時構建。但如何有效控制催化劑結構又是一個挑戰。層狀雙金屬氫氧化物 (LDHs) 以其主體層板化學組成可調、組成層板的金屬元素以原子水平高度分散、層狀結構拓撲轉變形成層狀雙金屬氧化物 (LDO) 等特點,成為氧化物負載過渡金屬催化劑的良好前驅體。
因此,本工作以 NiAl-LDHs 為前體,設計制備了 NiAl-LDO 負載納米 Ni 催化劑(Ni-NiAl-LDO)。納米 Ni 顆粒為脫氫和氫轉移提供了有效的金屬催化活性位點,NiAl-LDO 為醛氨/aldol 雙重交叉縮合提供了足夠的酸堿催化活性位,因此實現了無需外加液體堿及氫氣條件下 C-C/C-N鍵的同時構建,Ni-NiAl-LDO 催化伯醇和 2-氨基芐醇有效轉化為 THQ 及其衍生物。研究結果發表在 ACS Catal. (DOI: 10.1021/acscatal.9b03245)上,第一作者為北京化工大學的博士生張健,通訊作者為何靜教授。
圖文解析
a.催化劑制備與性能
首先,通過 Ni/Al 比為 2.0 的 NiAl-LDHs 在還原氣氛下的拓撲轉變得到了 Ni 顆粒為 5.0 nm、暴露 Ni(111)晶面的 Ni-NiAl-LDO。應用于乙醇和 2-氨基芐醇反應中,120 oC,反應22h,以 96 %的收率得到了 THQ 。通過監控反應歷程發現,2-氨基芐醇可以很快脫氫形成2-氨基苯甲醛,2-氨基苯甲醛是重要的中間體(圖1,a)。
表面上看,2-氨基苯甲醛的轉化控制著該反應的進行,但實際上,2-氨基苯甲醛的轉化不僅受自身與乙醛雙重交叉縮合的影響,而且受乙醇脫氫生成乙醛速率的影響。因此我們以乙醛代替乙醇,與 2-氨基芐醇反應,發現 2-氨基芐醇在 1h 內即可完全轉化為 1,2-二氫喹啉,且反應過程沒有檢測到 2-氨基苯甲醛和喹啉的產生(圖1,b),這說明 2-氨基苯甲醛與乙醛的交叉縮合以及氫轉移均可很快進行。因此可以斷定,乙醇脫氫形成乙醛為速率控制步驟。
同時還可發現,僅在乙醇和 2-氨基苯甲醇的反應初期檢測到痕量的喹啉(圖1,a),這一方面說明反應歷程經過喹啉中間體,另一方面說明納米Ni具備良好的氫轉移能力,形成的喹啉很快加氫形成目標產物THQ。為此,我們進一步對反應氣氛進行了調控,將反應氣氛由自然氣氛調整為氧氣氣氛,抑制氫轉移,發現產物停留在喹啉,反應 24 h,以 78 %的收率得到喹啉。
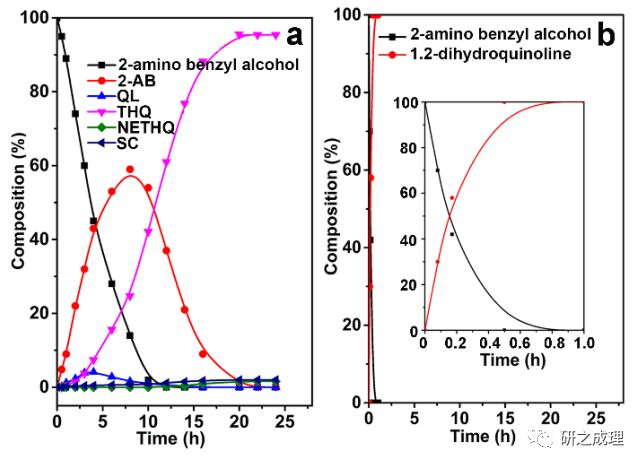
▲Figure1. Time course for the reaction between (a) 2-amino benzyl alcohol and ethanol and (b) 2-amino benzyl alcohol and acetaldehyde on 5.0nmNi-NiAl-LDO at 120 °C under an Ar atmosphere. The insert in (b) shows an enlarged view of the reaction profile within 1 h.
b.粒徑效應及本質
隨后,我們通過調控 NiAl-LDHs 的 Ni/Al 比及焙燒還原時間調控了 Ni 顆粒尺寸,得到了 Ni 顆粒粒徑尺寸分別為 3.0、5.0、5.6、6.4 和 7.8 nm,均暴露 Ni(111) 晶面且酸堿性相近的 Ni-NiAl-LDO(圖2)。將2-氨基苯甲醇脫氫、雙重交叉縮合和 THQ 產生速率與納米 Ni 粒徑相關聯,發現了明顯的 Ni 粒徑效應,即隨著 Ni 粒徑降低到 3.0 nm, THQ 生成速率明顯提升;而對于 2-氨基芐醇脫氫,Ni 粒徑低于 6.0 nm 時,其速率即有所提升(圖3,a)。
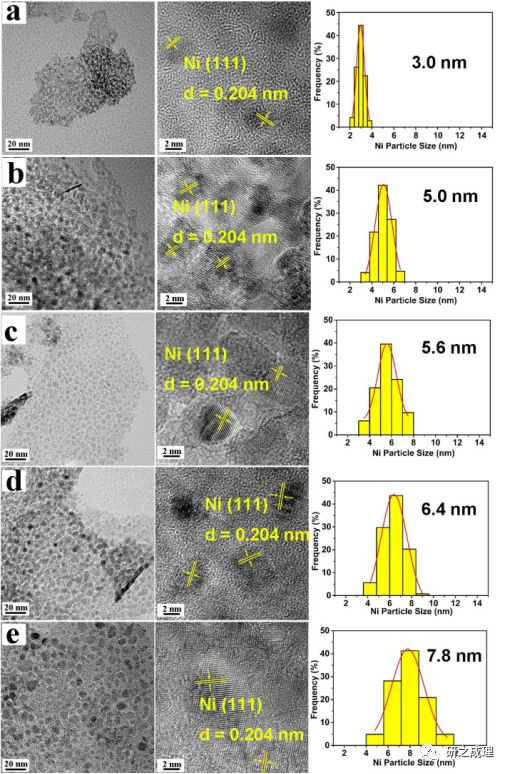
▲Figure 2. TEM images, HRTEM images, and size distribution of metallicNiparticleforNi-NiAl-LDO prepared by calcination under H2 atmosphere at 400 oCof(a) Ni1.08Al-LDHs for 1 min, (b) Ni2.01Al-LDHs for 1h, (c) Ni2.98Al-LDHs for 1.5h,(d) Ni3.97Al-LDHs for 2.0h, and (e) Ni5.03Al-LDHs for 2.5 h.
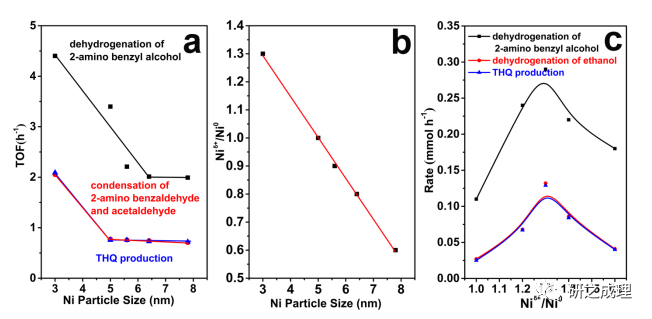
▲Figure3.(a) Profiles of turnover or product frequency as a function of Ni particle size. (b) ProfilesofNiδ+/Ni0 as a function of Ni particle size. (c) Conversion rate for 2-amino benzyl alcohol/2-amino benzaldehyde and formation rate for THQ vs the ratio ofsurfaceNid+ to Ni0.
為了探究 Ni 粒徑效應的本質,對Ni粒徑不同的 Ni-NiAl-LDO 進行了準原位 XPS 表征,發現 Ni 顆粒表面除了存在 Ni0 位之外,還存在表界面 Niδ+,并且隨著Ni粒徑的降低, Niδ+/Ni0 比例增高(圖3,b)。因此我們推測可能是表界面 Niδ+ 與表面 Ni0 之間存在協同效應促進了反應的進行。
為驗證這一推測,我們進一步對 Ni 粒徑為 5.0 nm 的 Ni-NiAl-LDO 進行了氧氣處理,將部分表面 Ni0 轉化成 Niδ+。發現隨著適當量的 Ni0 氧化成 Niδ+,催化性能明顯提升,但是過量的 Ni0 氧化成 Niδ+ 反而不利于反應的進行(圖3,c),說明 Niδ+ 與 Ni0 協同催化醇脫氫。
原位紅外光譜能夠實時有效地獲得反應物在活性中心上的活化模式,從而揭示反應機理。因此,我們選取乙醇作為探針分子,進行了原位紅外表征(圖4),探究 Niδ+與 Ni0 之間的協同。發現 NiAl-LDO 或者Niδ+位可以活化乙醇的 O-H 鍵形成乙氧基,Ni0 斷裂乙氧基中的 α-C-H 鍵形成 Ni-H(1597-1625 cm-1) 和 acetate(1419-1424 cm-1) (圖4, a-e)。隨著粒徑增大,Niδ+/Ni0 比例降低,acetate 峰強度降低(圖4,a-c)。而將部分 Ni0 轉化成 Niδ+, acetate 峰強度又明顯提升(圖4,d),表明 Niδ+/Ni0 比例增加,乙醇脫氫性能提升,但是過少的 Ni0 位反而不利于α-C-H斷裂,acetate峰強度降低(圖4,e)。由此可以得出:Niδ+ 和 Ni0 兩者協同完成乙醇脫氫過程,即 Niδ+ 負責活化 O-H 鍵形成乙氧基,Ni0 負責斷裂 α-C-H 鍵。吸附在 Ni0 位上的 H 可以有效釋放,完成氫轉移,部分表面 Ni0 轉化成 Niδ+ 不影響氫轉移(圖5)。
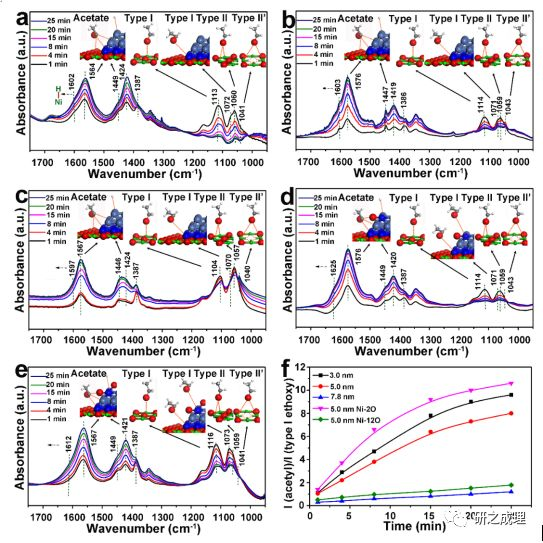
▲Figure 4. OperandoFT-IR spectra recorded during the reaction of adsorbed ethanol at 120 °C under vacuum conditions for (a) 3.0nmNi-NiAl-LDO, (b) 5.0nmNi-NiAl-LDO, (c) 7.8nmNi-NiAl-LDO, and 5.0nmNi-NiAl-LDO treated with (d) 2mLand (e) 12mLof O2. (f) The intensity ratio of acetyl (1576 cm-1) to type I ethoxy (1070-1073 cm-1) absorption on Nid+ sites as a function of time. Ethanol activation models are shownin the inserts. The red, blue, green, white, gray-blue, and gray spheres and the red dotted circle represent the O, Nid+, Ni2+, H, Ni0, C, and O vacancies, respectively.
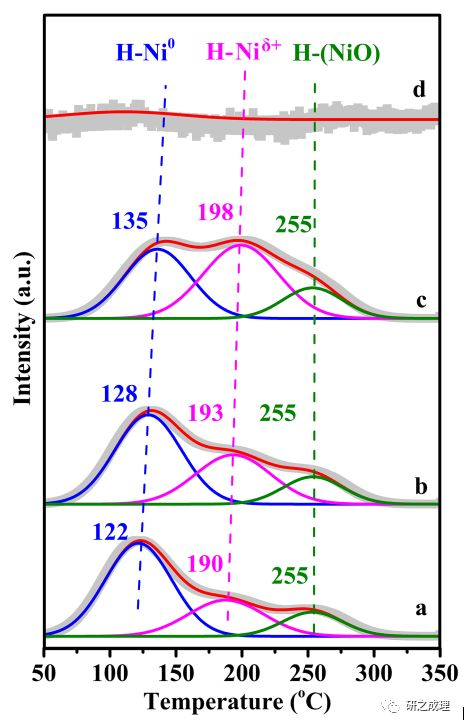
▲Figure 5. H2-TPDprofilesfor 5.0nmNi-NiAl-LDO before (a) and after treatment with 2mL(b) or 12mL (c) of O2 and (d) on NiAl-LDO.
c.底物拓展
將 5.0 nm 的 Ni-NiAl-LDO 催化劑應用于其它長鏈醇或者取代的 2-氨基芐醇中,均取得了很好的 THQ 收率(表1)。
通過調控納米 Ni 催化劑 Ni 顆粒表面 Niδ+ 與 Ni0 協同效應,成功實現了無外加液體堿和氫氣條件下的 C-C/C-N 鍵同時構筑。根據該工作的研究發現,單原子 Ni 或者團簇可能具有更好的脫氫和轉移加氫的能力。其次,在該工作中,NiAl-LDO 表面上的堿性和酸性位點足以催化縮合反應形成 C=N/C=C 鍵。然而,為了進一步衍生生成 N-烷基化的 THQ,對于催化劑載體表面的堿性或酸性位點的調控可能更具挑戰性。因此,開發單原子 Ni 或者團簇并結合適當的酸度和堿性來制備 N-烷基化 THQ 值得更多的關注和研究。
通訊作者:何靜,女,北京化工大學教授,博士生導師,現任化工資源有效利用國家重點實驗室主任、化學學院院長。分別于 1984 和 1991 年于北京大學獲得學士和碩士學位,1999 年于北京化工大學獲得博士學位。作為(高級)訪問學者分別于 1996、2003 和 2006 年赴澳大利亞新南威爾士大學、英國牛津大學、德國馬普煤化學研究所進行學術訪問。2002 年獲得“教育部優秀骨干教師”稱號,同年入選國務院享受政府特殊津貼專家;2004 年入選首屆教育部“新世紀優秀人才”資助計劃;2010 年獲得“國家杰出青年科學基金”資助;研究方向為:納米催化與生物質資源有效利用、單原子催化與化石資源清潔利用、多相不對稱催化與手性分子綠色合成、外場(光、電)協同與催化機理:在 J Catal、AIChE J、Angew Chem Int Ed、ACS Catal、Chem Eur J 等刊物上發表學術論文 180 篇;以第一發明人獲得美國發明專利授權 1 件、國家發明專利授權 23 件;以第一完成人獲北京市科學技術一等獎 1 項;以主要完成人獲得國家技術發明二等獎 1 項、科技進步二等獎 1 項、中國石油和化學工業協會技術發明一等獎 1 項。
第一作者:張健,男,北京化工大學化學學院博士研究生。2011 年于河北工業大學獲得學士學位。2013 年進入北京化工大學何靜教授課題組攻讀碩士學位,2015 年轉為博士研究生,2019 年赴德國卡爾斯魯厄理工學院聯合培養。主要研究方向:生物質產氫、乙醇轉化、合成氣轉化催化劑原位表征:在 ACS Sustainable Chem Eng、ACS Catal 等刊物上發表學術論文 2 篇。














