近日,南方科技大學王杰課題組和北京大學陳鵬課題組合作在Nature Chemical Biology期刊上發表了文章A gasdermin-based life–death evolution system for reprogramming protease specificity,將蛋白酶的進化與宿主的生命周期偶聯,構建了一種基于“生死選擇”的高通量定向進化系統。并進一步通過該系統進化TEV蛋白酶,使其能識別并切割多種細胞靶蛋白。

蛋白酶通過切割酶原或前體蛋白生成新的生物活性分子,參與調控多種生理與病理過程,包括程序性細胞死亡、血液凝固級聯反應以及病原體感染等。重編程蛋白酶底物特異性,有望實現對目標蛋白的選擇性降解、特定信號通路的按需激活,甚至病理性蛋白的精準清除,從而衍生一系列在基礎研究與疾病干預中的革命性應用。
對標基因編輯工具對核酸序列進行靶向切割(或改寫),若能以類似的“可編程”理念重塑蛋白酶的底物特異性,使其識別并切割新的目標蛋白,將為蛋白質層面的精準編輯開辟全新路徑。與基因編輯需要識別15-18個堿基長度的核酸序列才可以在基因組上實現特異性不同,蛋白酶僅需要識別5-7個氨基酸長度的多肽序列就可以在蛋白組上實現特異性,而一個蛋白酶的口袋大小,通常在4-8個氨基酸范圍,因此,通過高效的定向進化方法,改變蛋白酶的底物特異性,有望實現蛋白質的靶向編輯。
天然蛋白酶的序列多樣性有限,難以滿足大規模、精確的蛋白質編輯需求。要實現這一目標,必須對天然酶的底物特異性進行系統性重編程。然而,要讓一種蛋白酶“改刀換刃”并非易事。蛋白酶識別底物的方式極為精細:它們依賴4–8個連續氨基酸殘基在空間和化學上的精確匹配,以定位切割位點。哪怕微小的識別序列改變,也可能擾動酶的整體構象或催化中心,導致活性喪失。傳統的定向進化方法雖然可以通過突變和篩選獲得部分改良的酶,但受限于通量和成本,難以在龐大的突變空間中快速篩選出理想變體,實現對不同序列的高特異性切割。這使得蛋白酶的特異性改造長期停留在“微調”階段,而難以實現真正意義上的重編程。
為了高效實現對蛋白酶底物特異性的重塑,研究團隊利用細胞焦亡的功能執行蛋白-Gasdermin D(GSDMD),構建了一種基于“生死選擇”策略的蛋白酶定向進化平臺。
首先,他們發現在原核生物中表達GSDMD的N端結構域(1-275,GD-N)可以對大腸桿菌的膜結構產生破壞,從而對其生長產生明顯的抑制。不僅如此,大腸桿菌的生長速度可以很好的受到GD-N的表達水平的調控,呈現出劑量依賴的效果,從而驗證GD-N是一個很好的篩選標簽。
隨后,他們在GD-N蛋白表面的loop區(R153-V163)插入了TEV蛋白酶的目標序列,通過篩選發現這一序列的引入不影響GD-N蛋白對大腸桿菌生長的抑制,進而實現對蛋白酶突變體的篩選:當蛋白酶突變體能識別并切割目標序列,毒蛋白GD-N的活性被破壞,細胞存活;當蛋白酶突變體不能識別目標序列,GD-N蛋白對細菌膜結構破壞,細菌生長受到抑制。
通過連續的培養,含有高活性突變體的大腸桿菌,生長速度較快,從而被富集,構建好的蛋白酶定向進化平臺可一輪篩選中,對高活性突變體可以實現百萬倍的富集效果。
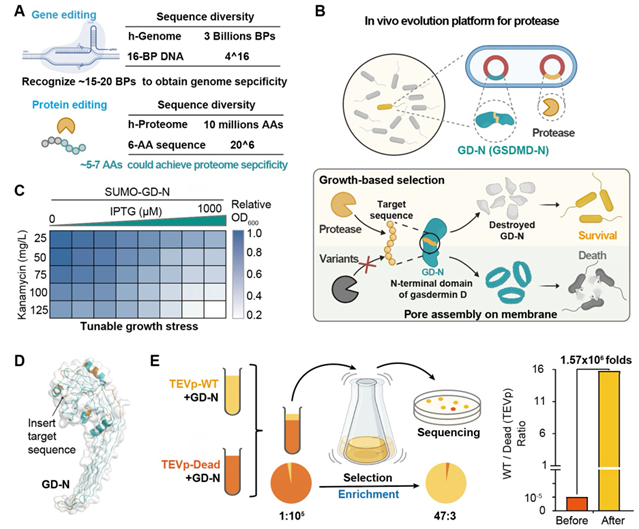
圖1:基于GSDMD的蛋白酶定向進化平臺的建立與表征
研究團隊利用所建立的定向進化平臺,對TEV蛋白酶進行了系統進化,使其能夠特異性識別并切割來源多樣、結構復雜的內源性底物,包括膜蛋白CD22、線粒體蛋白ALAS1以及核蛋白EZHIP。其中CD22是一種B細胞特異性膜受體,通過抑制BCR信號維持免疫穩態,同時是B細胞相關腫瘤的重要治療靶點。ALAS1是血紅素生物合成途徑中的關鍵限速酶,其異常激活是Ⅰ型卟啉病的主要致病因素。EZHIP是一種位于細胞核的調控蛋白,通過抑制PRC2活性重塑H3K27甲基化圖譜,在維持發育可塑性及中樞神經系統腫瘤發生中發揮關鍵作用;其異常高表達可導致表觀遺傳失衡并促發彌漫性中線膠質瘤。
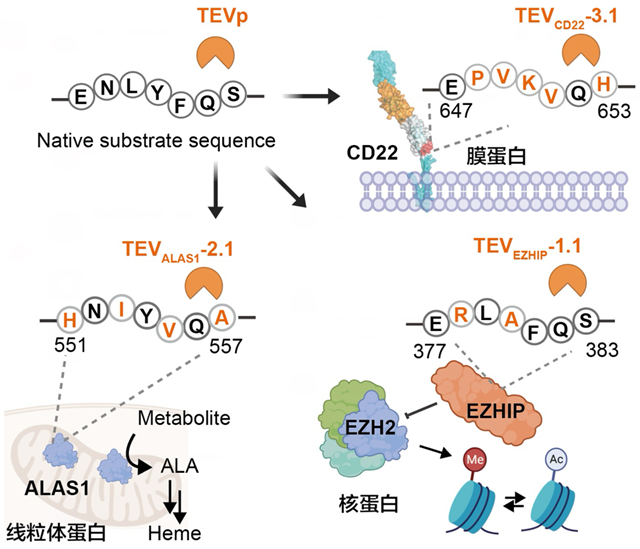
圖2:蛋白酶的特異性進化與蛋白質的靶向編輯
對于CD22靶點,研究者選取了其靠近細胞膜結構域的一段序列,該序列與TEV原始識別序列相比,在7個氨基酸中有5處發生了改變(ENLYFQS vs. EPVKVQH)。基于對底物不同氨基酸位點對特異性貢獻的分析,以及識別口袋中關鍵殘基在底物結合中的作用,團隊設計了TEV蛋白酶的進化路徑,并構建了滿足多輪進化需求的飽和點突變文庫,最終獲得了能夠高效切割目標序列的酶切活性突變體。
對于ALAS1靶點,研究者選取了HNIYVQA(551-557)作為目標序列, 研究團隊通過定向進化獲得了能夠特異性識別并切割ALAS1特定氨基酸序列的TEV蛋白酶突變體。在體外和體內實驗中,該突變體均表現出良好的序列正交性,未觀察到明顯脫靶效應。
對于EZHIP靶點,研究者選取了ERLAFQS(377-383)作為目標序列,研究團利用GSDMD進化平臺,僅一輪進化便獲得了能夠特異性酶切EZHIP的TEV突變體。該突變體在體外對EZHIP表現出明顯的切割活性;將其遞送至U2OS細胞后,能有效降低內源性EZHIP蛋白水平,同時顯著提高組蛋白H3K27Me3水平。
總之,這項工作建立的GSDMD定向進化平臺能夠高效重編程蛋白酶底物特異性,實現對多種內源性蛋白的精準切割。該平臺可在單輪篩選中實現百萬倍富集,顯著提高篩選效率;結合飽和點突變庫和底物-逐步策略,能夠覆蓋超過10?級別的蛋白酶突變體,充分探索突變空間。利用該平臺成功進化TEV蛋白酶切割膜蛋白CD22、線粒體蛋白ALAS1及核蛋白EZHIP,驗證了其在不同亞細胞環境下的普適性與可編程性。此外,該平臺可與多種蛋白遞送系統結合,實現內源性蛋白在活細胞中的定點切割,為蛋白質組水平的精確編輯提供強有力工具,同時為治療、診斷及功能研究應用奠定了基礎。
南方科技大學王杰教授和北京大學陳鵬教授為本文的共同通訊作者,南方科技大學博士后高子奇、李天真和研究生葉昊為本文的共同第一作者。深圳灣實驗室博士后魏書程和課題組成員王薈杰為共同作者。
DOI:10.1038/s41589-025-02063-3
原文鏈接:https://doi.org/10.1038/s41589-025-02063-3








