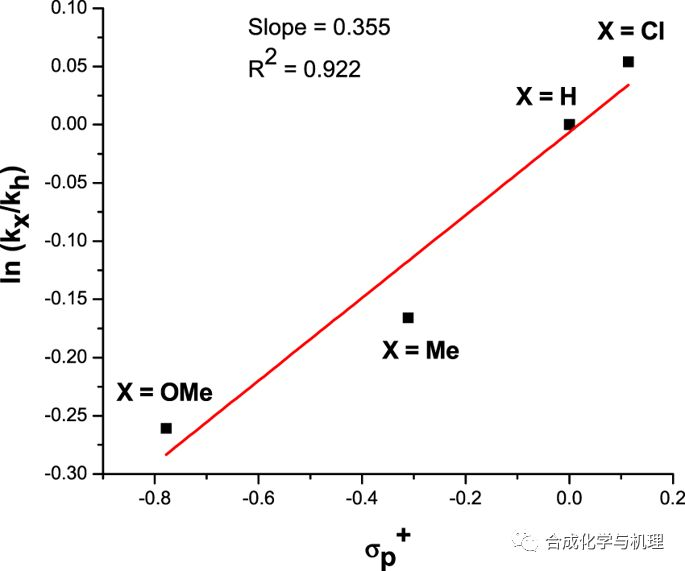
前面我們介紹了定量描述反應速率及平衡常數(shù)和反應物取代基類型之間線性自由能關(guān)系的Hammett方程(式1)。其中取代基常數(shù)σx和反應常數(shù)ρ對于反應過渡態(tài)的研究具有十分重要的物理意義。基于這兩個常數(shù),我們可以得到許多關(guān)于有機反應機理的信息。
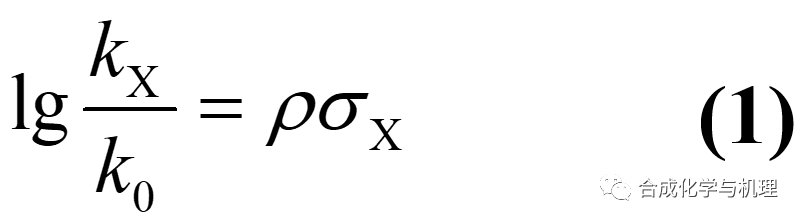
1 取代基常數(shù)σ
σ是取代基電子效應的度量。研究取代基電子效應需要避免空間效應的影響,這就要求取代基與反應中心保持一定的距離,但如果距離太遠又會導致電子效應太小。面對這種兩難的選擇,Hammett用間位和對位取代的苯甲酸的電離常數(shù)來定義取代基效應,避免了空間位阻的影響,電子效應又可以通過芳環(huán)的共軛體系而有效傳遞。
取代基常數(shù)的大小不僅與取代基的種類有關(guān),還與取代基在苯環(huán)上所處的位置有關(guān),而與反應物中除了取代基外的其它部分無關(guān),與反應類型和反應進行的條件也沒有關(guān)系。由于對位和間位苯甲酸的離解常數(shù)不同,每一取代基有兩個取代基常數(shù),即間位取代基常數(shù)和對位取代基常數(shù)。常見取代基的取代基常數(shù)列入下表中。
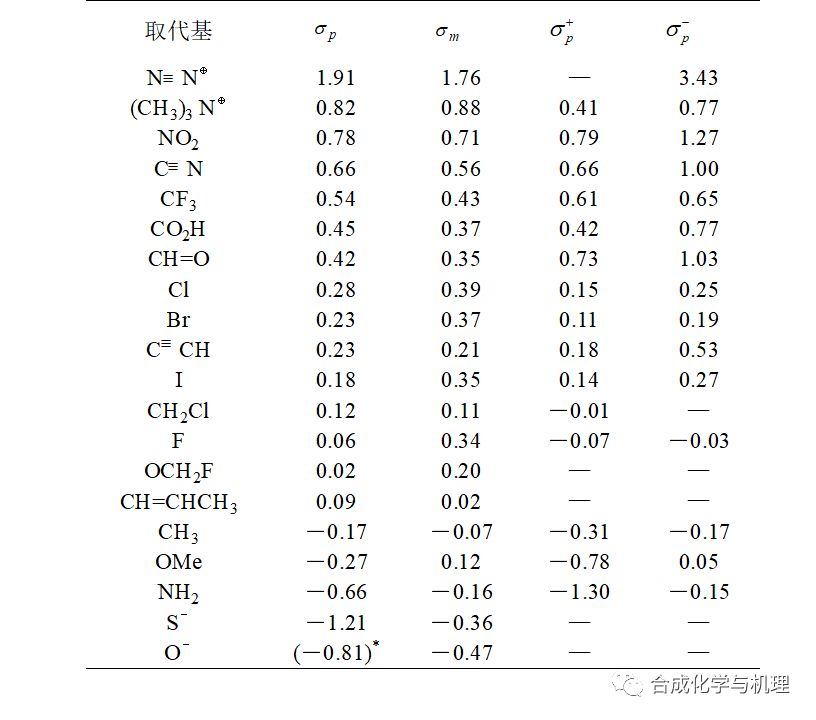
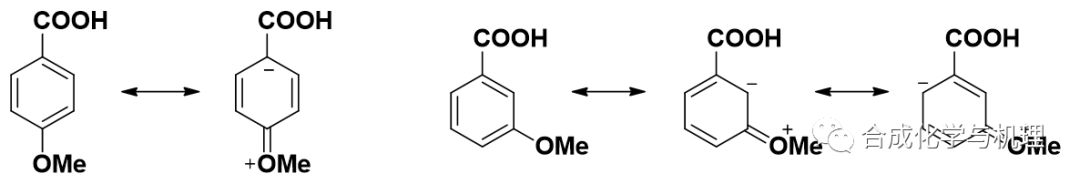
因為取代基常數(shù)代表的是對于負電荷的穩(wěn)定性,所以吸電基的取代基常數(shù)是正的,供電基的取代基常數(shù)是負的。一般來說取代基常數(shù)的正負與位置無關(guān),但有一個例外甲氧基的對位取代基常數(shù)是負的,而間位取代基常數(shù)是正的。這說明甲氧基在對位的時候是供電基,而在間位的時候更多的表現(xiàn)出吸電基的特性。為什么?
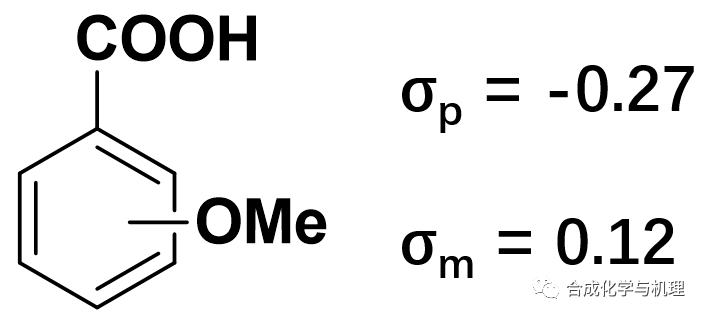
利用共振理論可以很好的解釋這個問題。如下圖所示,當甲氧基在對位時,其負電荷可以通過共軛作用有效傳遞給羧基,因此對位取代基常數(shù)σp是正的。而當甲氧基在間位時負電荷無法通過共軛作用到達間位,由于氧原子電負性較大,此時誘導效應起了主要的作用,因此間位取代基常數(shù)σm是負的。
2 取代基常數(shù)σ+和σ-
最初對σx的定義是建立在取代基效應對取代苯甲酸在25 ℃水溶液中電離反應的影響之上的,對于這些反應,取代基與反應中心不存在直接的共軛作用。有些發(fā)生在芳環(huán)支鏈或芳環(huán)上的反應,取代基與反應中心存在直接的共軛效應,例如取代苯基異丙基氯的水解反應。對于這些反應,反應速率的對數(shù)對s作圖不能得到好的線性關(guān)系,有必要定義一組新的取代基常數(shù)。
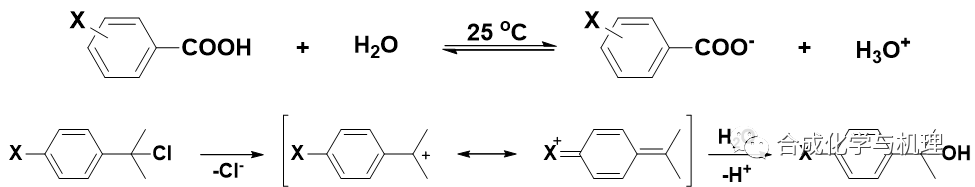
以取代苯基異丙基氯在90%丙酮中25℃時的SN1水解反應為標準反應。由于間位取代基與反應中心不發(fā)生直接共軛作用,σm+與σm相差不應很大,因此用部分取代基的σm代替σm+與速率常數(shù)的對數(shù)相關(guān)聯(lián)(Hammett方程),求出該標準反應的反應常數(shù)ρ為-4.54。然后再由ρ值和其它取代苯基異丙基氯在90%丙酮中25℃時的SN1水解反應的速率常數(shù)求出取代基位于對位時的取代基常數(shù)。對于強供電基,σp+的值通常較σp的值更負,反映了直接共軛效應的影響(電離常數(shù)變小)。同理以苯酚的電離反應為標準反應,我們可以求出σ-。以部分取代基的σm代替σm-,求得反應常數(shù)ρ=2.113。根據(jù)ρ值就可求出其它取代基的σm-和σp-。

3 反應常數(shù)ρ
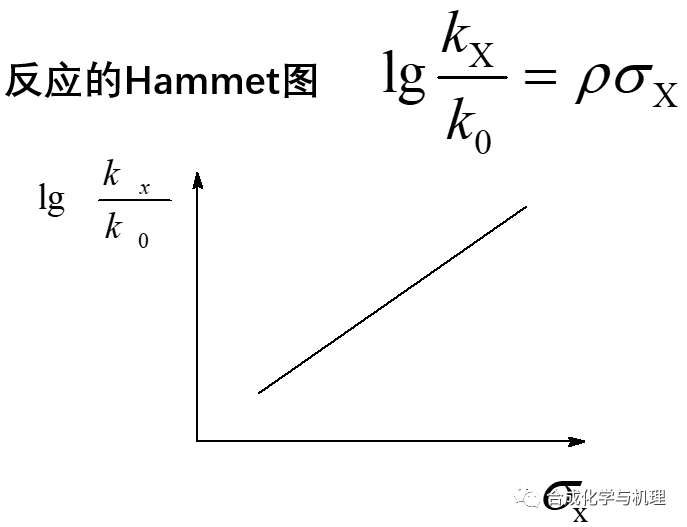
根據(jù)Hammet方程,如果以芳環(huán)側(cè)鏈某一反應的速率常數(shù)的對數(shù)作縱坐標,以取代基常數(shù)作橫坐標作圖,則可得到一條直線,反應常數(shù)ρ對應于直線的斜率。因此,反應常數(shù)ρ反映了與標準反應相比,所研究的反應對取代基效應的敏感程度。很明顯,ρ的絕對值越大,反應對取代基效應越敏感。
反應常數(shù)ρ的符號與反應機理的關(guān)系:
(1)ρ> 0時
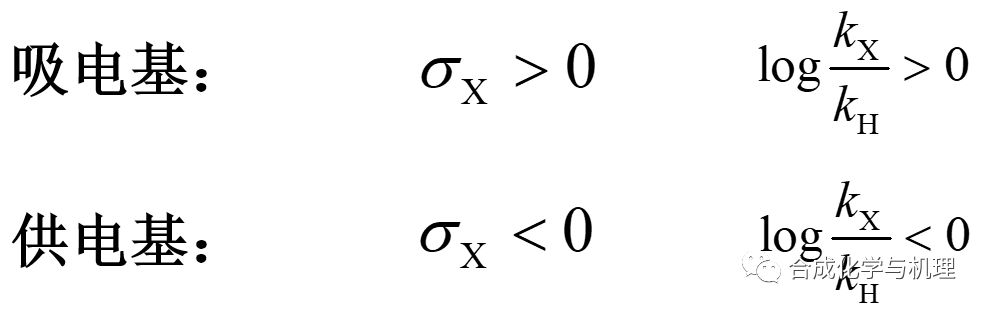
吸電基有利反應,供電基對反應不利,表明反應過渡態(tài)帶負電荷,或從反應物到過渡態(tài)負電荷增加。
(2)ρ< 0時
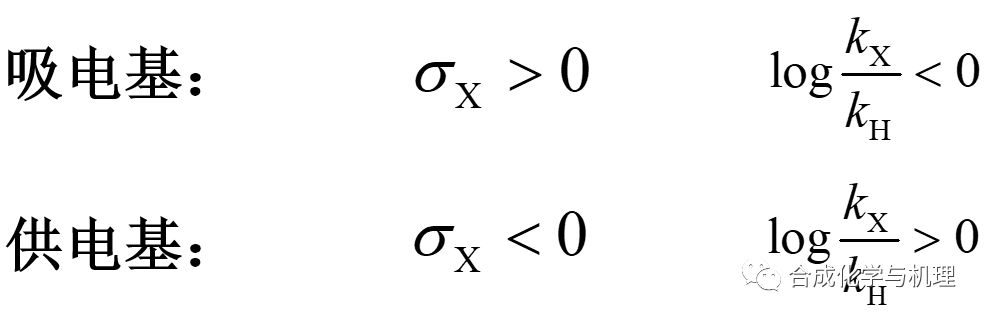
供電基有利反應,吸電基對反應不利,表明反應過渡態(tài)帶正電荷,或從反應物到過渡態(tài)正電荷增加。








