1、乙醚中的氧原子難于和水形成氫鍵,所以稍溶于水,室溫下,乙醚中可溶有1%~1.5%的水,水中可溶解7.5%的乙醚。離子型化合物在乙醚中不溶,所以在鹽類化合物的乙醇溶液中加入乙醚,可以從中析出沉淀物。可用此方法將油狀物轉變為固體以及提純化合物。
2、醚基中的氧含有兩對孤對電子,具有堿性和親核性;受電子效應的影響,醚α碳上有氫時易被氧化。醚久置會自發氧化產生不易揮發的過氧化物(自由基機理),過氧化醚是爆炸性極強的高聚物,蒸餾久置醚液時,過氧化醚殘留在容器中,繼續加熱即會爆炸。(進行醚液蒸餾時,通常保留適量液體,靠余溫揮干,可降低爆炸風險)。在進行乙醚蒸餾時,即使醚液中不含過氧化物,由于乙醚高度會發及蒸汽易燃,也會有爆炸和著火的危險,使用時一定要注意并要有預防措施。
3、乙醚能吸收相當量的鹽酸氣,形成钅羊鹽,把形成的钅羊鹽與有機堿的乙醚溶液放在一次,即可析出胺的鹽酸鹽,這是制備銨鹽的一種較好的方法。
4、醚與氫碘酸一起加熱,酸先與醚形成钅羊鹽,然后發生SN1或SN2反應,經碳氧鍵的斷裂生成碘代烷和醇,在過量的氫碘酸存在下,所產生的醇也會轉變為碘代烷。該方法可用于某些甲基化反應之后的脫保護,注意分析醚鍵斷裂生成的主產物。
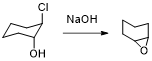
5、1,2-環氧化合物酸性開環與堿性開環問題:在酸性條件下,酸的作用是使環氧化合物的氧原子質子化并帶上正電荷,從而使氧向相鄰的環碳原子吸引電子,削弱了碳氧鍵,并使環碳原子帶有部分正電荷,增加了與親核試劑結合的能力,親核試劑向碳氧鍵的碳原子背后進攻(進攻碳原子的選擇考慮該碳原子穩定正電荷的能力),發生SN2反應。堿性開環,環氧化合物沒有帶正電荷或者負電荷,親核試劑進攻空間位阻小的環碳原子,發生SN2反應。
6、Williamon合成法制備醚類化合物:醇鈉與鹵代烷在無水條件下生成醚,在反應中,RO-是親核試劑,RX是反應底物,X-是離去基團。(RONa + R’X
生成 ROR’+ NaX)因為醇鈉既是親核試劑又是堿性試劑,所以三級鹵代烷在此條件下能發生消除反應,因此若想保證產物的單一性,最好用一級鹵代烷。分子間成醚反應,醇必須做成醇鈉,分子內成醚反應,醇只需在氫氧化鈉存在下就可以進行反應。
7、相轉移催化劑
將反應實體從水相轉移到有機相中,并把反應中另一種離子帶入到水相中,在轉移過程中催化劑本身沒有損耗,只是重復地起“轉送”負離子的作用,這種催化劑即稱為相轉移催化劑。
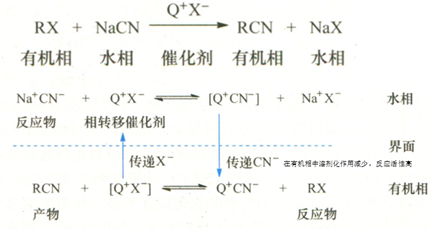
多數相轉移反應要求催化劑把負離子轉移到有機相中,還有些催化劑是把正離子或中性分子從一相轉移到另一相中。常用的相轉移催化劑有鎓鹽(四級銨鹽最常用)、冠醚、三相催化劑(不溶的固體催化劑,用于加速水-有機兩相體系的反應,操作簡便,易于后處理,催化劑可定量回收)。相轉移催化劑可使許多反應比在慣用條件下容易進行,且反應選擇性強,產品純度高,在降低溫度及縮短反應時間等方面有明顯的優越性。
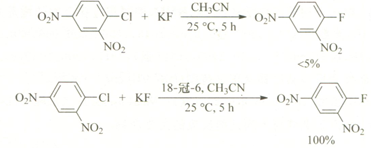
(總結于基礎有機化學第四版)








