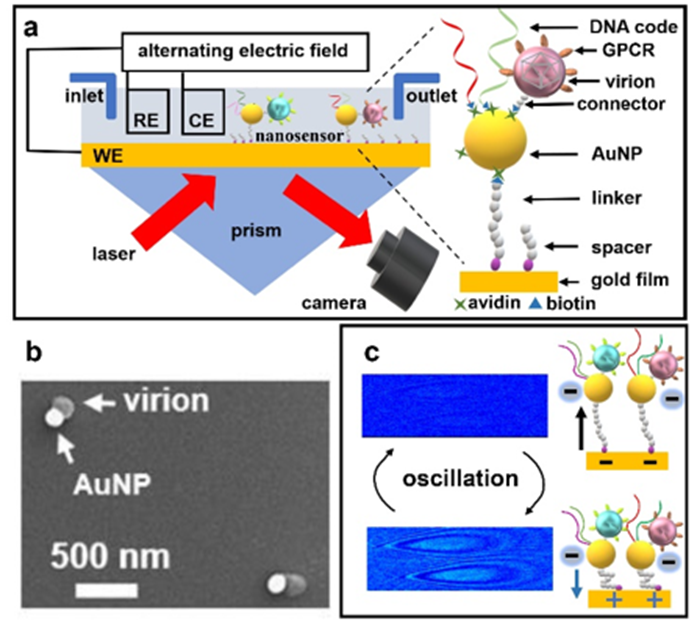
膜蛋白作為細胞膜上的關鍵功能分子,在細胞信號轉導、物質運輸和能量轉換等生命過程中發揮著核心作用,是現代藥物研發的重要靶點,超過60%的臨床藥物通過作用于膜蛋白發揮療效。然而,如何在接近生理環境的條件下保持膜蛋白的天然構象并準確測定其與小分子配體的相互作用動力學參數(包括結合常數Kd、結合速率kon和解離速率koff等),一直是藥物研發領域面臨的重要技術挑戰。 近日,亞利桑那州立大學的王少鵬副教授團隊、廈門大學的曹爍暉副教授以及約翰霍普金斯大學醫學院朱恒教授的團隊展開合作研究,取得了突破性進展。研究團隊通過將金納米顆粒-病毒復合物自組裝在表面等離子體傳感器芯片上,構建了高密度、高靈敏度的表面等離子體納米振子陣列檢測系統。在交變電場驅動下,研究團隊采用寬場表面等離子體成像技術實現了納米振子振幅變化的精確測量。這項技術將病毒展示技術與電荷敏感表面等離子體測量技術相結合,其獨特的電荷敏感檢測機制,能夠在單個納米傳感器分辨率水平上,靈敏地檢測病毒顆粒表面膜蛋白與小分子配體的特異性結合,其檢測靈敏度顯著超越了傳統的基于質量變化的檢測技術。該平臺引入"親和力"編解碼策略,具有指數級的多重檢測能力。以五對G蛋白偶聯受體(GPCR)及其對應小分子配體的相互作用為模型,僅需兩種四態DNA解碼輸入,即可在單一傳感器芯片上實現對全部納米振子的同步識別和動力學參數的并行測定,充分驗證了該平臺的高通量篩選能力。 該項研究成果為膜蛋白測量研究提供新工具,不僅解決了傳統技術難以在生理條件下保持膜蛋白天然構象的技術難題,更為創新藥物研發提供高效、精準的篩選平臺,對推動精準醫療和個性化藥物研發具有重要意義。 文章的第一作者是廈門大學的曹爍暉副教授,通訊作者為亞利桑那州立大學的王少鵬副教授。
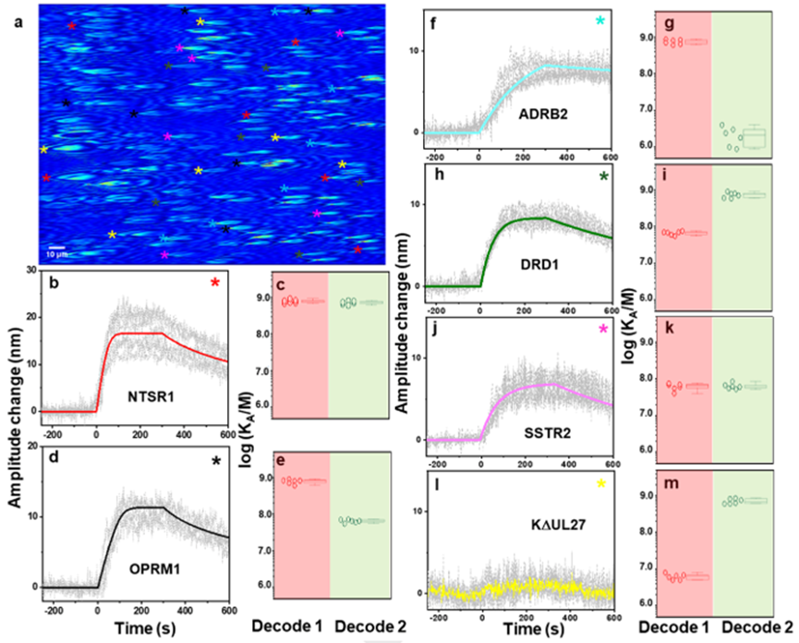
圖1金納米顆粒-病毒復合物及電場驅動表面等離子體成像過程 圖2基于表面等離子體單顆粒成像的膜蛋白-小分子動力學參數高通量并行測量 論文信息 Plasmonic DNA-Barcoded Virion Nano-Oscillators for Multiplexed Quantification of Small-Molecule Binding Kinetics to Membrane Proteins Shuo-Hui Cao, Zijian Wan, Eric Johansen, Guangzhong Ma, Prashant Desai, Heng Zhu, Shaopeng Wang Angewandte Chemie International Edition DOI: 10.1002/anie.202506464