分享一篇發表在Angewandte Chemie International Edition的文章,文章的標題為“Engineered Thermostable Chemically Responsive GlowCas9 System for Real-Time Therapeutic Monitoring Applications”,本文的通訊作者為 Basudeb Maji。

傳統CRISPR/Cas9技術的脫靶效應與Cas9在細胞中暴露時間密切相關,因此需要一種可實時監測其在細胞內分布與活性的手段。現有的抗體或熒光檢測方法靈敏度有限,且不適用于活體體系。為此,作者通過蛋白工程構建了一個兼具高穩定性與實時可檢測特性的發光型 Cas9 系統——GlowCas9。
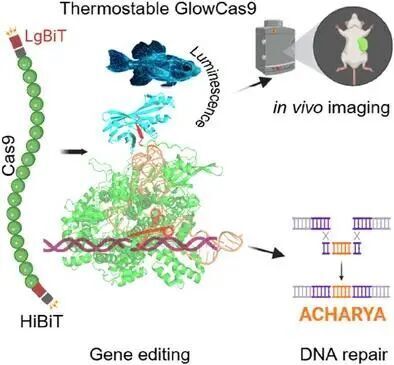
研究團隊選擇利用一種來自 Oplophorus gracilirostris 蝦的納米熒光素酶(NanoLuc)系統,該系統由兩個亞基 LgBiT 和 HiBiT 組成,在接近時能高親和性結合并恢復發光功能。作者將這兩個亞基分別連接到Cas9蛋白的N端和C端,使其在分子內部閉合重組,形成一個可自發光的GlowCas9融合蛋白,從而賦予Cas9實時報告的功能。
在結構驗證中,研究者通過重組質粒表達和Western Blot檢測發現GlowCas9的分子量增加,證明融合成功。僅在GlowCas9轉染細胞中觀察到顯著的發光信號,說明熒光素酶亞基在細胞中能正確折疊并恢復活性。非變性凝膠電泳實驗顯示僅有單一條帶,排除了線性寡聚化的可能,證實該系統以單體閉環形式存在。細胞發光成像進一步顯示GlowCas9在添加底物NanoGlo后產生強烈信號,而對細胞活性無明顯影響,表明該系統兼具功能性與生物相容性。
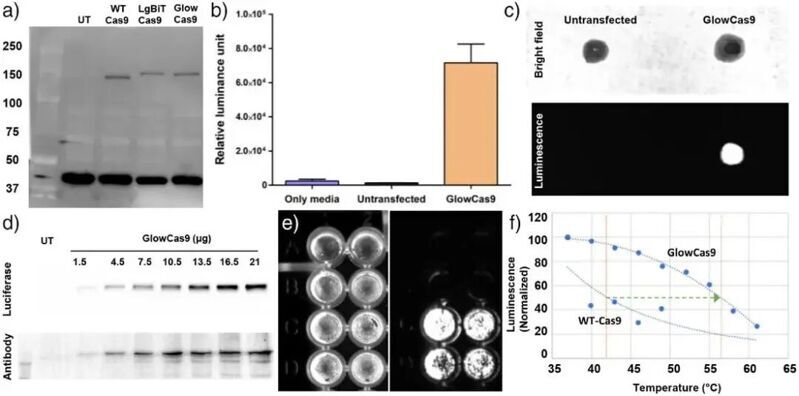
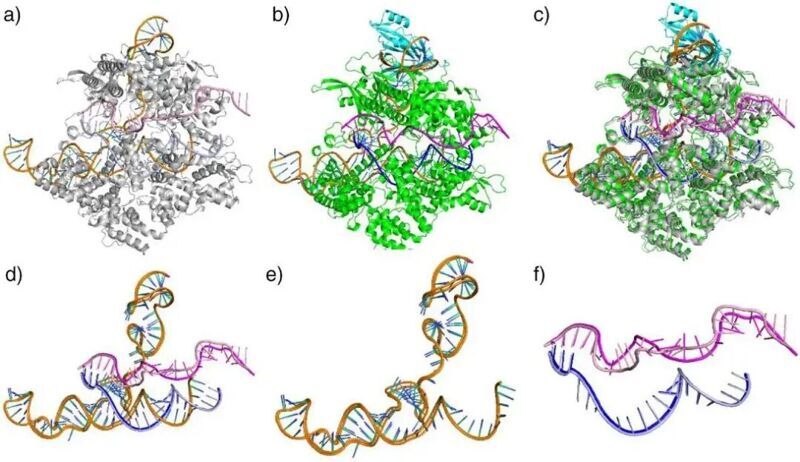
隨后,作者從結構與功能兩方面系統評估了GlowCas9的性能。通過細胞熱位移實驗(CETSA)測得其熔解溫度(Tm)明顯高于野生型Cas9,體現出優異的熱穩定性。在基因編輯實驗中,GlowCas9與自切割GFP報告系統共轉染后,可抑制GFP信號約 75%以上,略高于WTCas9的70%,顯示其保持甚至增強了核酸切割活性。利用AlphaFold3進行的結構預測表明,GlowCas9與sgRNA和DNA的結合方式與WTCas9 高度一致。熒光偏振實驗也證實GlowCas9–sgRNA–DNA復合體能夠正確組裝,這說明發光結構域的引入并未破壞Cas9的天然活性中心。
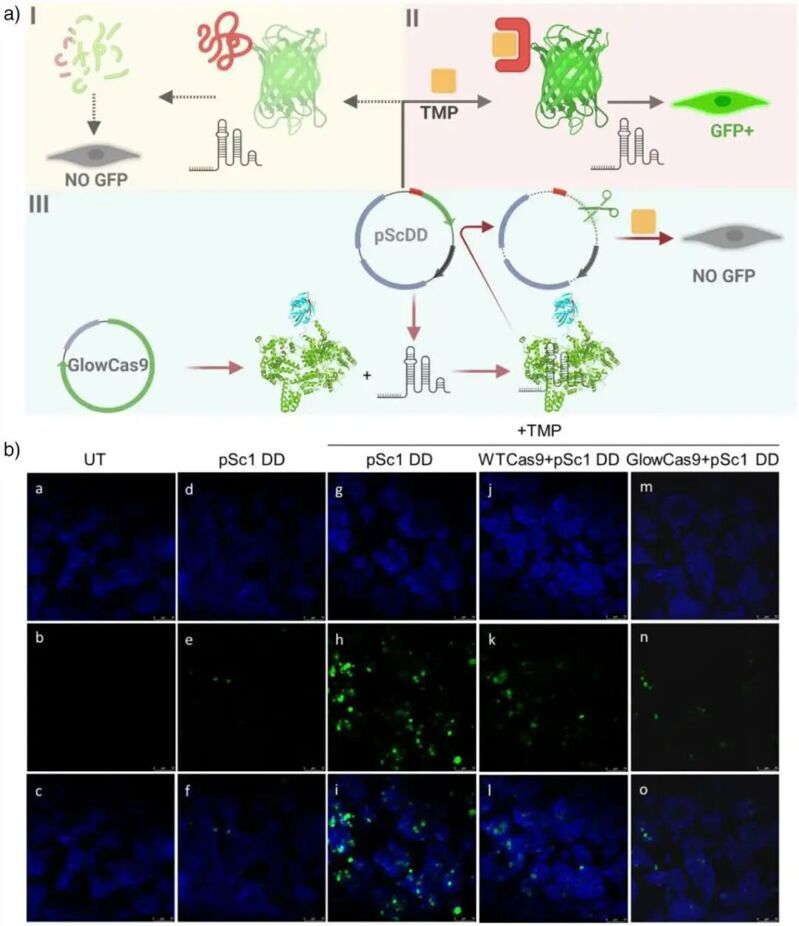
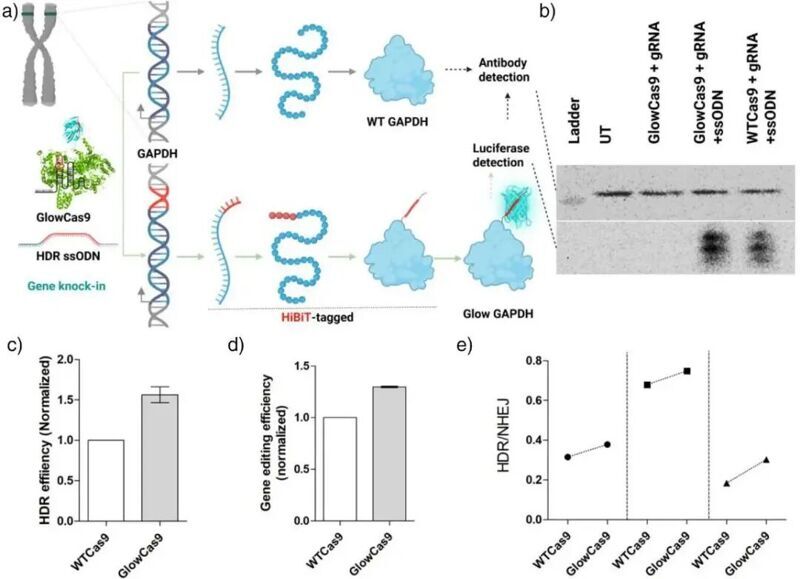
接下來,作者發現GlowCas9 展示了顯著優于 WTCas9 的精確敲入能力。作者在GAPDH 基因C端設計了靶位點,并提供包含HiBiT序列的單鏈寡核苷酸(ssODN)作為修復模板。由于GlowCas9自身帶有發光結構,研究者改進了檢測方法,將發光信號與非變性凝膠電泳結合,在分離后的凝膠上加入LgBiT與NanoGlo底物,從而檢測成功整合HiBiT標簽的GAPDH蛋白。結果顯示,GlowCas9介導的HDR信號強度顯著高于WTCas9組,其模板依賴性修復效率提升約1.5倍。進一步在EMX1基因位點的敲入實驗中,高通量測序結果同樣表明 GlowCas9不僅總體HDR效率更高,而且HDR與NHEJ的比值也明顯上升,說明其在修復途徑選擇上更傾向于精確的模板重組。
最后,作者將GlowCas9的發光特性用于跨系統的蛋白追蹤實驗。在植物葉片注射實驗中,作者成功在 Solanum tuberosum 葉片中實現GlowCas9的原位檢測,僅注射區域在底物存在下顯示強烈發光,證明該系統可用于跨物種、跨體系的Cas9遞送監控。
總的來說,本文開發了一種高兼容性的實時檢測Cas9的系統GlowCas9。
本文作者:CJJ
責任編輯:TZS
DOI:10.1002/anie.202511707
原文鏈接:https://doi.org/10.1002/anie.202511707








