研究背景
氧原子轉(zhuǎn)移反應是有機化學中一類重要的反應。環(huán)氧化物是合成表面活性劑、環(huán)氧樹脂和藥物的重要中間體,通常是由烯烴的環(huán)氧化反應制備。大部分的烯烴環(huán)氧化反應需要用到如叔丁基過氧化氫(TBHP)、間氯過氧苯甲酸(mCPBA)等過氧化物或者經(jīng)過氯乙醇過程實現(xiàn),這些方法操作流程較為復雜、存在潛在的安全問題且會產(chǎn)生副產(chǎn)物。通過O2還原或水分解原位產(chǎn)生過氧化氫(H2O2)實現(xiàn)烯烴的環(huán)氧化是更好的途徑,仿生的均相復合物、雜多酸、金屬團簇或氧化物均可以催化這類反應。此外,光催化烯烴環(huán)氧化反應也被廣泛應用,但這一方法也存在一些問題,如需要較高的反應溫度(~80-100°C);需要光敏劑;均相催化劑的分離以及需要使用H2O2等有潛在危險的氧化劑。因此,發(fā)展一種以水為氧供體且不經(jīng)過H2O2中間體的烯烴環(huán)氧化途徑是非常必要的。
2 成果簡介
針對上述問題,麻省理工學院Karthish Manthiram團隊在Journal of the American Chemical Society上發(fā)表了題為“Epoxidation of cyclooctene using water as the oxygen atom source at manganese oxide electrocatalysts”的論文。該工作發(fā)展了一種在室溫常壓的條件下利用Mn3O4作為電催化劑在電解水的同時實現(xiàn)環(huán)氧化物合成的方法,這一方法更為安全簡便,且環(huán)氧化反應的法拉第效率>30%,陰極產(chǎn)氫的法拉第效率>94±5%。該工作為氧原子轉(zhuǎn)移反應提供了新的電化學方法。
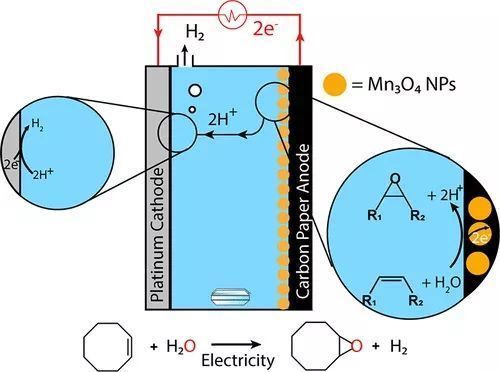
圖1 實現(xiàn)烯烴環(huán)氧化反應的新途徑
3 圖文導讀
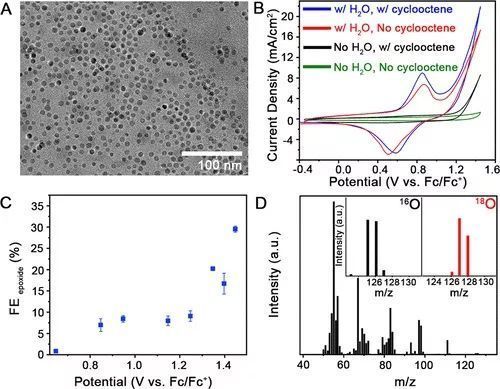
圖2 (A)MnO納米顆粒的TEM圖片,(B)不同條件下以Mn3O4為電催化劑的循環(huán)伏安曲線,(C)不同電壓下環(huán)氧化反應的法拉第效率,(d)環(huán)氧化產(chǎn)物的GC-MS圖。
考慮到氧化錳納米顆粒是高效的電解水催化劑,且在催化過程中形成的Mn(Ⅳ)=O活性中間體也可能作為烯烴環(huán)氧化反應的氧供體,因此該工作選擇Mn3O4作為這一體系的電催化劑。圖2A是通過熱注入法制備的單分散MnO納米顆粒的TEM圖片。之后MnO納米顆粒經(jīng)過配體交換和退火處理轉(zhuǎn)變?yōu)橛糜诜磻w系的Mn3O4納米顆粒催化劑。
該工作研究了反應體系中水、環(huán)辛烯和Mn3O4對于環(huán)氧化反應的影響,圖2B是不同條件下的CV曲線,由圖可以看到只有在體系中有水存在時Mn3O4才會有在大約0.7V處的氧化還原峰,這說明水是形成Mn(Ⅲ)/Mn(Ⅳ)氧化還原對的氧供體。圖2C是通入20 C電量時不同電壓下的法拉第效率,由NMR和GC-MS檢測到陽極只有環(huán)辛酮一種副產(chǎn)物。由圖2C可以看到在大約0.8 V(vs Fc/Fc+)電壓下環(huán)氧化反應開始發(fā)生,這與Mn氧化還原對的電位相匹配。有趣的是在低電壓下只生成了環(huán)氧環(huán)辛烷,在高電壓下環(huán)氧環(huán)辛烷和環(huán)辛酮都有生成。在1.45 V(vs Fc/Fc+)時環(huán)氧環(huán)辛烷與環(huán)辛酮的比為3.91:1。該工作利用同位素標記的方法證明了水是環(huán)氧化反應中的唯一氧供體,由圖2D可以看到當換成H2O18時,環(huán)氧環(huán)辛烷荷質(zhì)比的峰位從125和125偏移至127和128。而且不論體系中是否有環(huán)辛烯的存在,均檢測不到H2O2中間體,這些結(jié)果都證實了水是唯一的氧供體且不產(chǎn)生H2O2中間體。
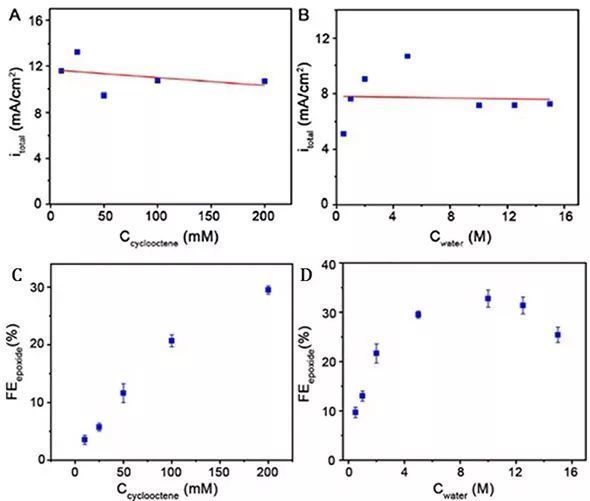 圖3 在1.45 V(vs Fc/Fc+)電壓下環(huán)辛烯和水的濃度對電流密度和法拉第效率的影響。
圖3 在1.45 V(vs Fc/Fc+)電壓下環(huán)辛烯和水的濃度對電流密度和法拉第效率的影響。
接著該工作分別研究了體系中環(huán)辛烯和水的濃度對于電流密度和法拉第效率的影響。由圖3A-B可以看到隨著體系中環(huán)辛烯或水濃度的增大總的電流密度沒有太大變化,這說明該反應是由Mn氧化還原對活性位點濃度決定的。由圖3C可以看到FEepoxide隨著環(huán)辛烯的濃度增大而線性增大,這是由于高濃度下的環(huán)辛烯更易吸附在Mn氧化還原對活性位點上經(jīng)反應生產(chǎn)環(huán)氧環(huán)辛烷。從圖3D可以看到FEepoxide一開始隨著水的濃度增大而增大,當水的濃度為10 M時達到最大值,之后開始單調(diào)遞減。這是由于當水的濃度大于10 M(即環(huán)辛烯的溶解度小于200 mM)時電解液變得渾濁同時環(huán)辛烯的濃度下降,使得FEepoxide變小。
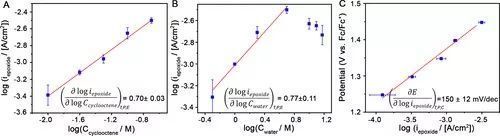
圖4 Mn3O4電催化烯烴環(huán)氧化反應的動力學曲線
從圖4A可以看到環(huán)氧化反應分電流iepoxide與環(huán)辛烯濃度的關(guān)系符合一級反應的特點;由圖4B可以看到當水的濃度為0.5~5 M時iepoxide與環(huán)辛烯濃度的關(guān)系符合一級反應的特點,而當水的濃度大于5 M時二者呈負相關(guān),這是由于體系內(nèi)環(huán)辛烯濃度下降造成的。從塔菲爾曲線(圖4C)中可以看到在實驗條件下Mn3O4納米顆粒的塔菲爾斜率是150±12 mV/dec,表明該反應的決速步是一個單電子轉(zhuǎn)移過程并且整個環(huán)氧化反應中沒有先于決速步的其他電子轉(zhuǎn)移過程。
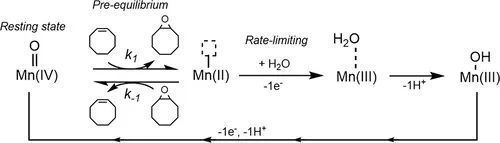
圖5 錳氧化物電催化烯烴環(huán)氧化反應的機理圖
由上述電化學動力學研究提出了錳氧化物電催化烯烴環(huán)氧化反應的機理:Mn(Ⅳ)=O作為反應的準備態(tài)與環(huán)辛烯反應后變?yōu)楹醒蹩瘴坏腗n(Ⅱ),這一過程是一個可逆的預平衡過程。該工作在體系中加入1,2-環(huán)氧辛烷后檢測到了1-辛烯的生成,這一實驗結(jié)果證實了這一平衡過程的確存在。之后H2O親核進攻含有氧空位的Mn(Ⅱ),經(jīng)過單電子轉(zhuǎn)移過程生成Mn(Ⅲ)-OH2,這一中間體由于其姜-泰勒形變效應Mn(Ⅲ)-OH2的穩(wěn)定性較低所以形成它的能壘變大,因此這一過程的是反應的決速步。
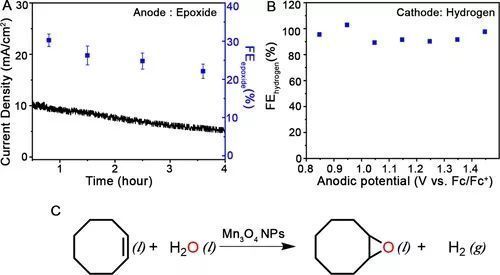
圖6 全反應的性能表征
由圖6A可以看到在陽極的環(huán)氧化反應中4小時內(nèi)的總轉(zhuǎn)化率為~50%,其法拉第效率的降低是由于底物濃度的降低引起的。由圖6B可以看到陰極的析氫反應的法拉第效率為94±5%。這些結(jié)果表明這一體系在電解水的同時還可以利用產(chǎn)生的氧物種使烯烴發(fā)生環(huán)氧化反應制備環(huán)氧化物。
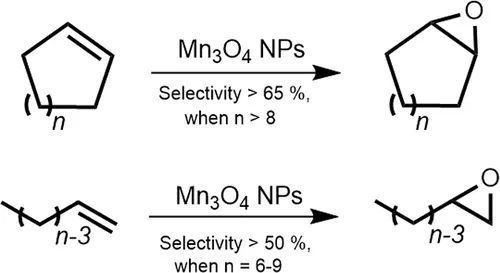
圖7 烯烴環(huán)氧化反應的底物拓展
接著該工作將不同的烯烴應用于這一反應體系中,由圖7可以看到不論是環(huán)烯烴還是鏈烯烴均適用于這一體系。實驗結(jié)果表明當鏈狀烯烴的碳鏈變長時環(huán)氧化物的選擇性變好;當環(huán)烯烴的環(huán)更大時環(huán)氧化物的選擇性也更好;而當環(huán)烯烴的碳原子個數(shù)小于8時縮環(huán)反應更容易發(fā)生。因此未來可以探究對于不同烯烴底物最優(yōu)的反應條件。
4 總結(jié)與展望
這一工作發(fā)展了一種在室溫常壓的條件下利用Mn3O4作為電催化劑在電解水的同時實現(xiàn)環(huán)氧化物合成的方法,并且研究了反應的機理。這一方法更為安全簡便、適用于各種烯烴底物,且環(huán)氧化反應的法拉第效率>30%,陰極產(chǎn)氫的法拉第效率>94±5%。該工作為氧原子轉(zhuǎn)移反應提供了新的電化學方法。
5 文獻信息
Epoxidation of cyclooctene using water as the oxygen atom source at manganese oxide electrocatalysts (J. Am. Chem. Soc., 2019, 141, 15, 6413-6418)
原文鏈接:
https://pubs.acs.org.ccindex.cn/doi/10.1021/jacs.9b02345
供稿丨深圳市清新電源研究院
部門丨媒體信息中心科技情報部
撰稿人丨Star sheep
主編丨張哲旭








