分享一篇發表在angewandte chemie international edition上的文章,題目為“Rational Design of CDK12/13 and BRD4 Molecular Glue Degraders”。通訊作者是來自斯坦福大學的Nathanael S. Gray教授,他們課題組的主要研究方向為運用合成化學、蛋白質生物化學與癌癥生物學等技術手段,發現針對抗癌靶點的新策略。

分子膠是一類通過鄰近驅動機制促使兩種蛋白質二聚化、形成三元復合物的小分子。這類分子能特異性募集特定蛋白,從而精確調控信號轉導、轉錄、蛋白質定位、穩定化及降解等多種生物學過程。其中,分子膠降解劑可誘導E3泛素連接酶與靶蛋白接近,導致靶蛋白發生泛素化并被降解。與傳統基于占據驅動藥理學(主要通過抑制蛋白酶活性)的藥物發現模式不同,分子膠展現出獨特的事件驅動藥理學特性——包括能消除靶蛋白所有功能,以及在低藥物濃度下仍可維持靶蛋白耗竭。與PROTAC相比,具有類藥特性的分子膠降解劑雖更具優勢,但其發現往往具有偶然性,設計仍面臨挑戰。
作者探索了在分子膠降解劑設計中引入膠聯基團(gluing moiety)的策略。通過對母體抑制劑進行添加膠聯基團的微小修飾,即可實現功能獲得性轉變,將其有效轉化為蛋白降解劑.
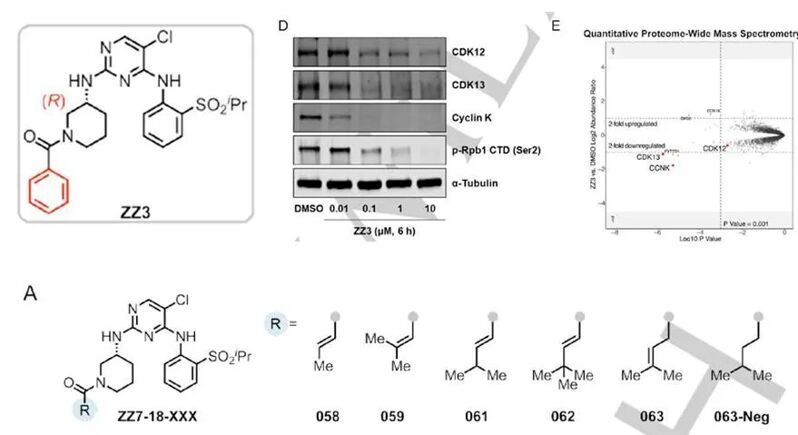
作者首先在CDK12/13結合分子中引入疏水性膠聯基團(如芳環或雙鍵)可募集DDB1,從而將高分子量CDK12 PROTAC轉化為高效的單價CDK12/13分子膠降解劑。
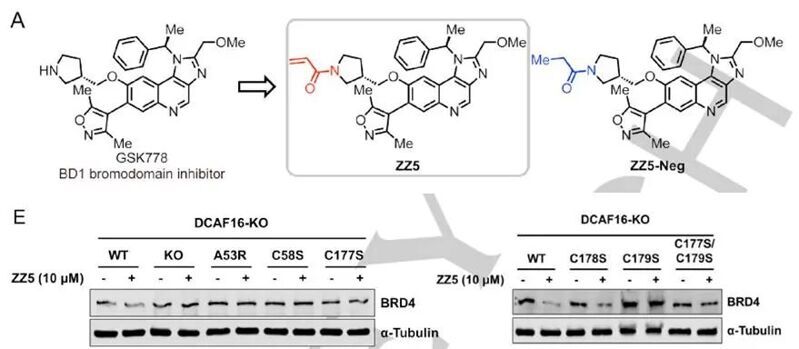
此外,研究還表明,通過在BRD4抑制劑上附加半胱氨酸反應彈頭,可募集DCAF16 E3連接酶使其轉化為降解劑。
這些發現表明,對已知靶標抑制劑或結合分子進行結構衍生化,將成為發現分子膠降解劑的重要途徑。
本文作者:CZH
責任編輯:TZS
DOI:10.1002/anie.202508427
原文鏈接:https://doi.org/10.1002/anie.202508427








