分享一篇發(fā)表在Cell Metabolism上的文章:Homocysitaconate controls inflammation through reshaping methionine metabolism and N-homocysteinylation,通訊作者是來自同濟大學的梅馨予和Dashi Qi,梅馨予課題組的研究方向主要是高同型半胱氨酸血癥的致病機制和干預方法,以及同型半胱氨酸修飾的鑒定方法、生物機制等。

免疫代謝物是炎癥調節(jié)的關鍵因子,例如衣康酸及其衍生物具有抗炎活性和治療潛力。另外這些活性代謝物也可能會產生新的次級代謝物,衣康酸可以代謝成檸康酸和中康酸,也可以和硫醇反應(半胱氨酸殘基和谷胱甘肽等)。在細胞硫醇代謝物中,同型半胱氨酸具有促炎特性。在炎癥應激條件下,巨噬細胞中同型半胱氨酸的生理濃度范圍為1-10 μM。本文作者發(fā)現同型半胱氨酸和衣康酸可以形成加合物,并且具有抗炎活性。
作者首先對LPS刺激的巨噬細胞進行了代謝組分析,發(fā)現有一個未知的化合物(m/z=264.0550)顯著上調,并且在其它炎癥模型中也有同樣的發(fā)現,說明它是一個炎癥反應性代謝物。作者注意到這個化合物的二級譜圖的離子m/z=129.0195和m/z=134.0284分別對應衣康酸和同型半胱氨酸,隨后通過標準品對照等實驗,證明了m/z=264.0550就是衣康酸和同型半胱氨酸通過邁克爾加成的產物,并將其命名為homocysitaconate, 簡稱Hci。
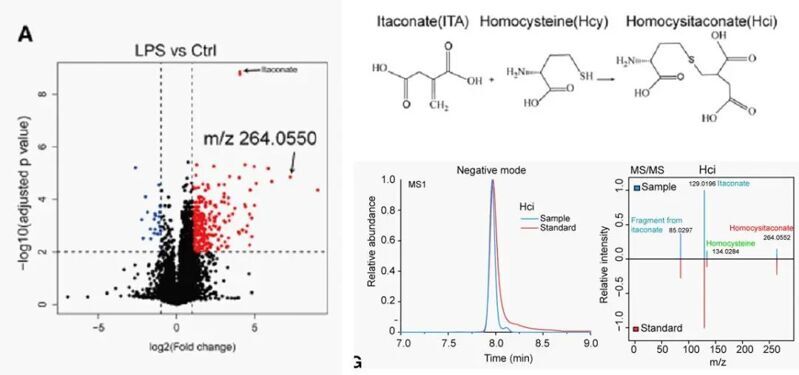
作者隨后對Hci的抗炎活性進行了研究,發(fā)現接近生理濃度的Hci在野生型巨噬細胞中,以劑量依賴性抑制IL-1β,IL-6和TNF-α的產生,需要的濃度是≥2 μM。作者表示與衣康酸不同,Hci在更短的時間內以更低的濃度表現出抗炎作用。
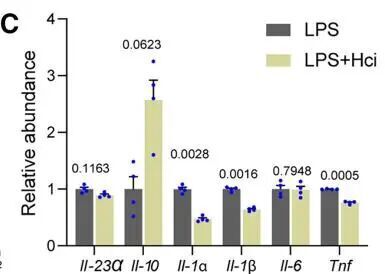
為了闡明Hci的抗炎機制,作者采用限制性酶切化學蛋白質組學(LiP-SMap)來鑒定其蛋白質靶標,對TOP16的靶點進行驗證,并有兩個主要的發(fā)現。
第一個靶標是促炎蛋白甲硫酰-tRNA合成酶(MARS),它是同型半胱氨酸代謝通路的下游,負責催化同型半胱氨酸硫內酯(HTL)的產生,而HTL可以修飾蛋白質賴氨酸殘基,形成N-同型半胱氨酸酰化。隨后作者對N-同型半胱氨酸酰化修飾蛋白進行鑒定,發(fā)現NLRP3的K194,K338 和 K339位點被修飾,并發(fā)現這種修飾促進了NLRP3去泛素化,使NLRP3炎性小體激活。作者為了研究Hci對MARS的影響,根據LiP-SMap的結果和理論預測,作者發(fā)現Hci主要結合在MARS的CAT催化結構域,關鍵殘基是D312。進一步的實驗表明,Hci能抑制MARS的活性,最終抑制了NLRP3的N-同型半胱氨酸酰化修飾和炎性小體激活。
此外,作者關注的第二個Hci靶蛋白是S-腺苷-L-同型半胱氨酸水解酶(AHCY),并發(fā)現AHCY能催化Hci的產生。
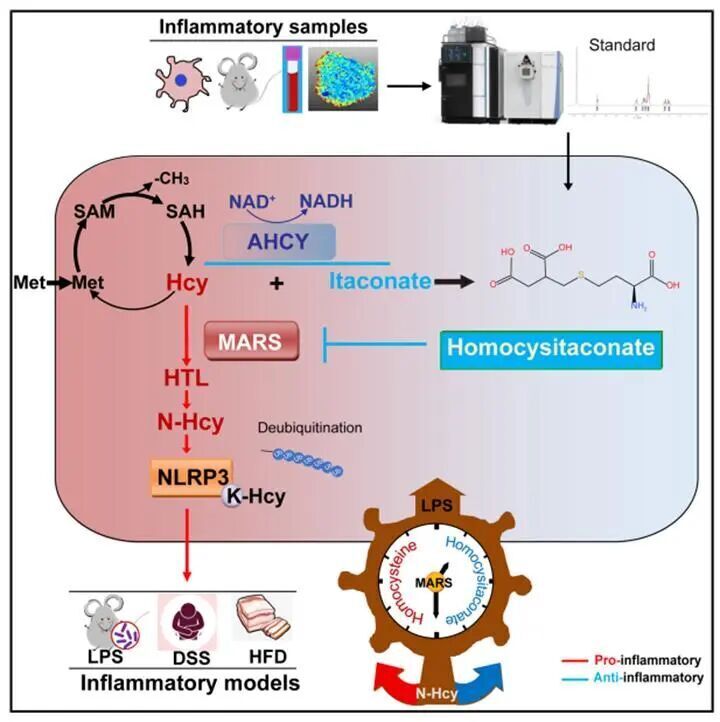
總而言之,本文作者證明了炎癥中同型半胱氨酸和衣康酸可以形成加合物Hci,并解析了它的形成和抗炎機制。
本文作者:MB
責任編輯:LZ
DOI:10.1016/j.cmet.2025.08.001
原文鏈接:https://doi.org/10.1016/j.cmet.2025.08.001








