推薦一篇發(fā)表在Nature Chemistry上的文章,文章標題“De novo design of light-responsive protein–protein interactions enables reversible formation of protein assemblies”。文章的通訊作者是來自西湖大學的曹龍興研究員,其課題組主要從事蛋白質(zhì)設計領域的研究。

光響應蛋白通過感知和響應環(huán)境光信號發(fā)揮其生物學功能。這種工作模式啟發(fā)研究人員探索光響應蛋白質(zhì)的設計路線,以實現(xiàn)對蛋白質(zhì)功能的精確、可逆和非侵入性的控制。目前的光響應蛋白設計工作主要集中于優(yōu)化天然存在的蛋白質(zhì);然而這一思路無法適應更廣泛的光響應調(diào)控需求。對于從頭設計方法而言,由于20種天然氨基酸通常是光惰性的,需要引入光敏發(fā)色團解決光響應性的問題。本文,作者將具有光響應能力的非天然氨基酸苯丙氨酸-4′-偶氮苯(AzoF)引入到設計流程中,通過結合非天然氨基酸插入技術,最終成功設計并驗證了能夠響應光信號、實現(xiàn)寡聚體可逆解離的蛋白質(zhì)。
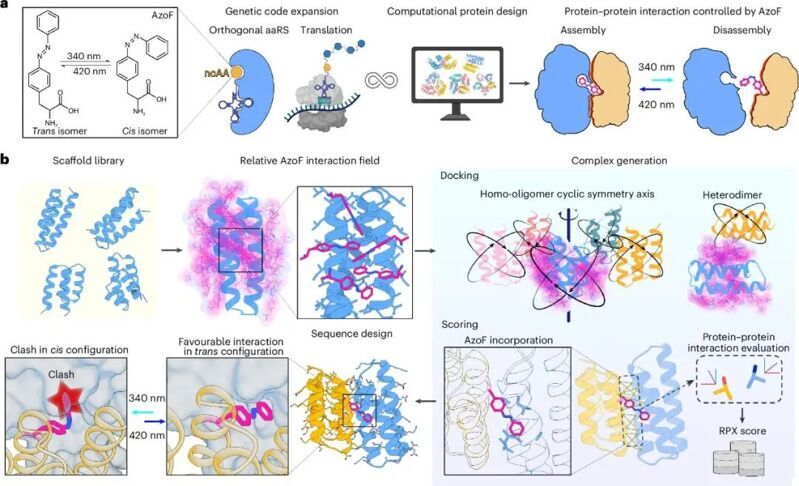
為了借助AzoF的光致構象變化調(diào)控蛋白質(zhì)的解離狀態(tài),作者設計了如下流程。首先,生成包含65個殘基的螺旋束作為蛋白骨架用于光響應性蛋白設計。其次,為了設計可以穩(wěn)定結合反式AzoF的區(qū)域,作者一方面基于AzoF的疏水性質(zhì)優(yōu)化了蛋白表面殘基的分布,另一方面采用對接的手段將AzoF小分子與蛋白質(zhì)進行對接;后者得到一個AzoF的相互作用場,它描述了AzoF相對于該骨架不同位置的結合能,可以用于快速評估AzoF能否與周圍殘基形成有利互作。隨后,通過蒙特卡洛對接方法,作者基于骨架優(yōu)化了蛋白質(zhì)互作以及AzoF的插入位置,最終組裝形成更大的復合物。最后,通過序列設計,作者進一步優(yōu)化互作界面,即有利于反式AzoF結合而不利于順式AzoF結合。
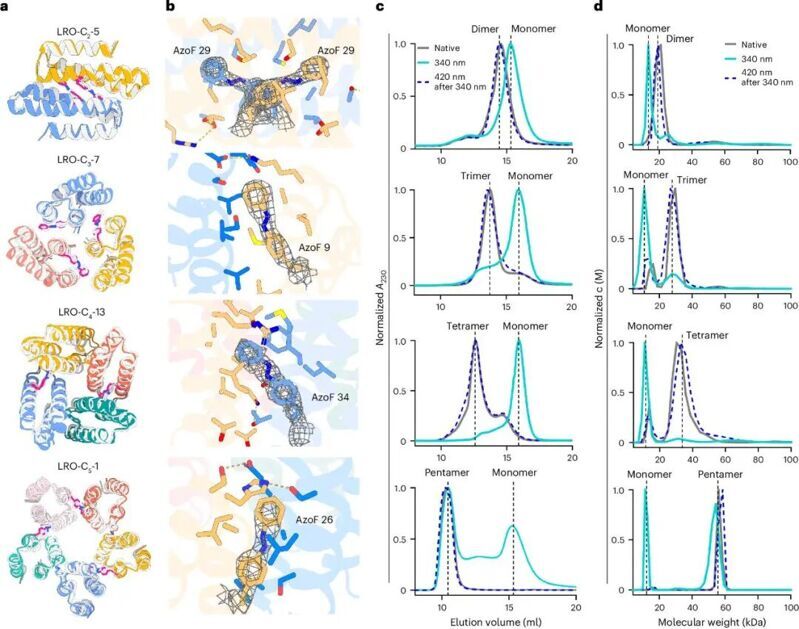
利用這一策略,作者成功地設計了不同類型的寡聚體。晶體結構與計算結構高度吻合,尺寸排阻色譜實驗亦驗證了其光致可逆組裝的特性。作者后續(xù)還利用五聚體構建了可以響應光的水凝膠。340nm光照后五聚體解離,水凝膠交聯(lián)程度降低,呈現(xiàn)液滴狀;420nm光照后則恢復原有的狀態(tài)。
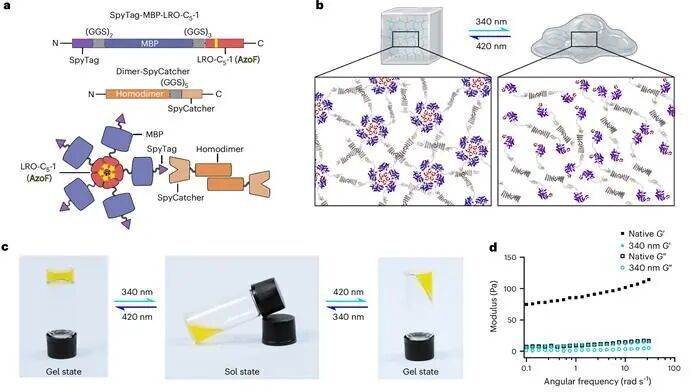
總而言之,本文作者利用包含有光響應性偶氮苯基團的非天然氨基酸,通過計算設計實現(xiàn)了蛋白復合物的可逆組裝。
本文作者:ZF
責任編輯:MB
DOI:10.1038/s41557-025-01929-2
原文鏈接:https://doi.org/10.1038/s41557-025-01929-2








