介紹的是最近在Nature Chemical Biology上報道的一篇標(biāo)題為“ELOVL6 activity attenuation induces mutant KRAS degradation” 的文章。該文的通訊作者是美國西北大學(xué)Feinberg醫(yī)學(xué)院的Shana O. Kelley教授。本研究通過全基因組CRISPR-Cas9敲除篩選發(fā)現(xiàn)了一種在KRAS多種類型突變體的功能調(diào)控中發(fā)揮作用的脂肪酸延長酶(ELOVL6),并將其開發(fā)為一種誘導(dǎo)KRAS突變體(主要是KRAS G12V)選擇性降解的抑制劑藥物用于腫瘤治療。
KRAS是胰腺癌、結(jié)直腸癌和非小細(xì)胞肺癌等侵襲性癌癥中最常見的突變致癌基因,靶向KRAS突變的治療對開發(fā)新的癌癥療法至關(guān)重要。其中,G12位氨基酸是一個突變熱點,占所有KRAS突變的89%。迄今為止,取得較大成功的是KRAS G12C突變體的共價抑制劑,通過與半胱氨酸的共價交聯(lián)將蛋白構(gòu)象限制在GDP結(jié)合的非活性形式中,從而抑制下游信號傳遞。但使用該策略選擇性抑制蛋白質(zhì)功能并不適用于其他KRAS突變體,其中一些如KRAS G12V突變也具有極大的臨床價值。
鑒于KRAS G12V的靶向抑制難度和重要性,本文作者專注于識別和調(diào)控細(xì)胞內(nèi)KRAS突變體水平的遺傳調(diào)控因子。通過細(xì)胞分選技術(shù)進行全基因組CRISPR-Cas9介導(dǎo)的敲除(KO)篩選,作者在野生型(WT)和KRAS G12V細(xì)胞系中尋找既能選擇性降低內(nèi)源性KRAS G12V前體蛋白水平又不影響WT KRAS的調(diào)控因子。篩選結(jié)果表明,脂肪酸延長酶ELOVL6是一種新型且具有選擇性的KRAS G12V調(diào)控因子。盡管ELOVL6此前已被發(fā)現(xiàn)與一些代謝疾病相關(guān),但其與KRAS致癌突變的關(guān)聯(lián)尚未見報道。本研究證實,ELOVL6功能缺失會導(dǎo)致KRAS G12V蛋白選擇性降解、致癌信號減弱以及KRAS依賴性腫瘤細(xì)胞增殖抑制。并基于此開發(fā)了具備等位基因選擇性的抗KRAS治療藥物。
具體而言,作者團隊首先使用CRISPR-Cas9全基因組敲除SgRNA文庫(TKOv3)感染SW480(G12V)和HT29(WT)細(xì)胞,采用微流控磁性分選細(xì)胞術(shù)(MagRC)平臺根據(jù)KRAS蛋白水平進行分選,提取低表達KRAS細(xì)胞群體進行gRNA富集測序分析。結(jié)果發(fā)現(xiàn),ELOVL6是SW480細(xì)胞中特異性富集程度最高的基因之一,而在HT29細(xì)胞中無顯著富集。流式細(xì)胞術(shù)驗證ELOVL6敲除后,KRAS G12V蛋白水平顯著下降。(圖1)
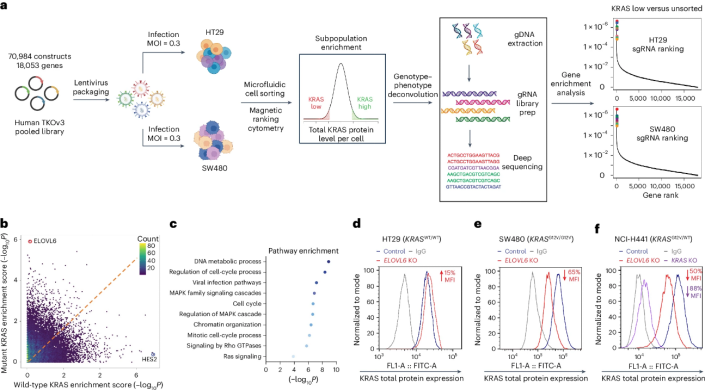
圖1. 全基因組敲除鑒定KRAS-G12V突變體的特異性調(diào)控因子。
接下來,作者團隊據(jù)此重點研究了ELOVL6在癌細(xì)胞系中對KRAS G12V突變蛋白水平的影響。他們在SW480(KRAS G12V/G12V)、HT29(KRAS WT/WT)和NCI-H441(KRAS G12V/WT)上分別構(gòu)建了ELOVL6敲除系統(tǒng),采用Western blot檢測KRAS總蛋白和G12V特異性蛋白水平。ELOVL6敲除導(dǎo)致KRAS G12V蛋白量下降50-80%,而WT KRAS無明顯變化。ELOVL6小分子抑制劑(ELOVL6i)處理也呈劑量依賴性降低KRAS-G12V蛋白。KRAS mRNA水平未受影響,說明調(diào)控發(fā)生在蛋白層面。(圖2)
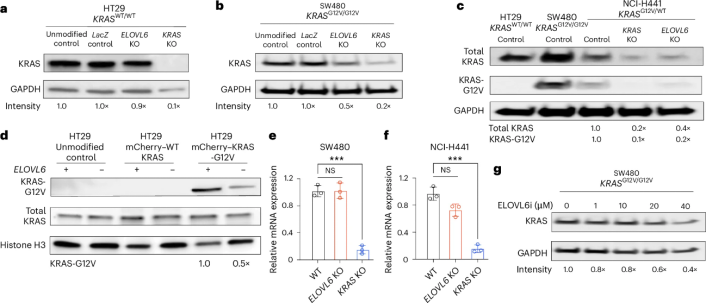
圖2. ELOVL6的缺失或抑制誘導(dǎo)突變KRAS G12V的選擇性降解。
進一步地,作者研究了ELOVL6抑制后的KRAS信號傳導(dǎo)相關(guān)功能。細(xì)胞增殖實驗結(jié)果表明,ELOVL6敲除或抑制顯著降低了KRAS G12V細(xì)胞的增殖能力。Western blot實驗也表明了ELOVL6敲除或抑制劑作用能夠在KRAS G12V或其他突變細(xì)胞系上顯著降低結(jié)合GTP的活性KRAS亞型水平。表明ELOVL6影響KRAS的活性和下游信號傳導(dǎo)。(圖3)
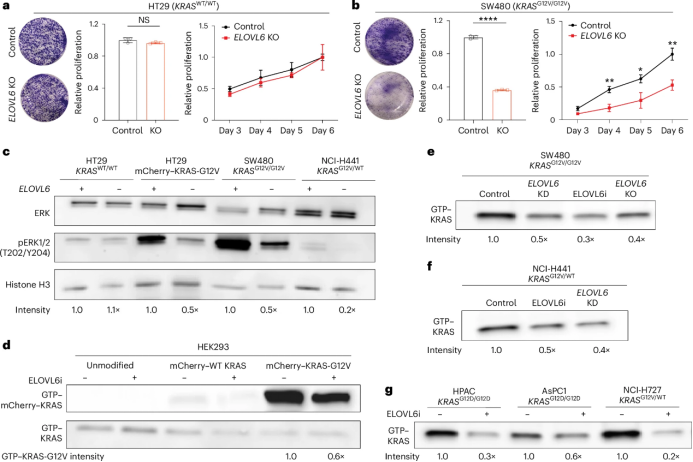
圖3. 抑制ELOVL6可影響KRAS G12V的活性及下游信號功能。
接下來,作者團隊深度研究了ELOVL6影響KRAS突變體水平的機制。由于ELOVL6在長鏈脂肪酸的從頭合成中起重要作用,與硬脂酰輔酶A脫氫酶1共同催化棕櫚酸向硬脂酸和隨后向油酸的碳鏈延伸。靶向脂質(zhì)定量分析發(fā)現(xiàn)在ELOVL6抑制劑處理后,硬脂酸(C18:0)和油酸(C18:1)含量均出現(xiàn)了顯著降低。而外源補加硬脂酸或油酸則能在一定程度上救援細(xì)胞活力,表明脂質(zhì)匱乏是細(xì)胞致死的重要原因。隨后,作者團隊通過LC-MS/MS定量分析不同物種中不對稱磷酯酰絲氨酸(PS)的組成變化。結(jié)果表明,共六種曾被文獻報道為能穩(wěn)定KRAS膜錨定的不對稱PS組成出現(xiàn)下降。共聚焦成像結(jié)果也表明,添加了抑制劑后,能夠顯著影響KRAS G12V的表達水平和膜共定位指數(shù)。同時,向細(xì)胞中補充混合鏈PS也能夠挽救因ELOVL6敲除導(dǎo)致的KRAS水平降低。證明了ELOVL6抑制通過影響胞內(nèi)脂質(zhì)組分水平而降低KRAS的膜定位情況,從而導(dǎo)致KRAS的降解。(圖4)
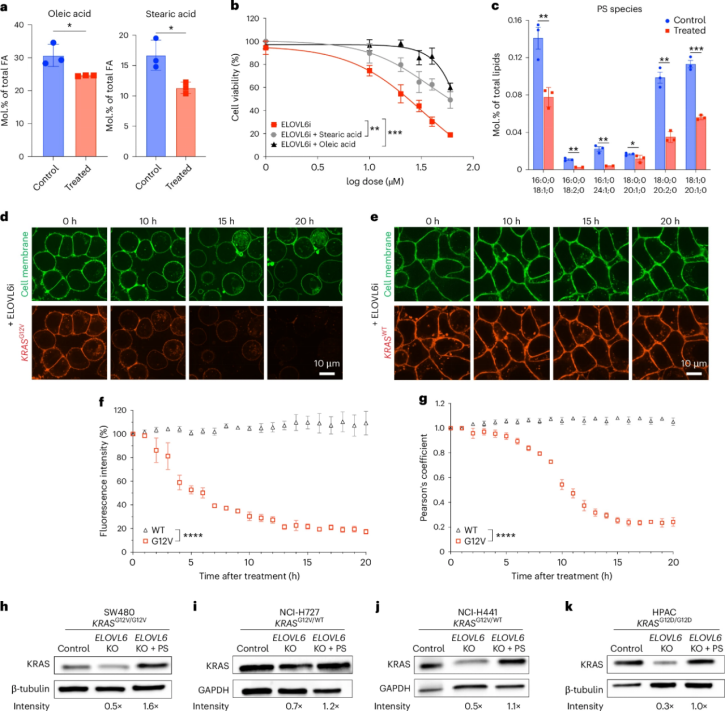
圖4. ELOVL6i通過改變細(xì)胞脂質(zhì)組成影響KRAS G12V突變體膜定位。
隨后,作者團隊用共聚焦顯微鏡觀察了溶酶體抑制劑Bafilomycin A1和ELOVL6抑制后胞內(nèi)KRAS分布情況。結(jié)果表明ELOVL6i處理導(dǎo)致KRAS G12V從膜上解離并進入胞質(zhì),聯(lián)合Bafilomycin A1處理后KRAS在胞質(zhì)中積累,表明其通過溶酶體途徑降解。綜合而言,ELOVL6抑制能夠顯著降低胞內(nèi)C18脂質(zhì)水平,從而使PS混合鏈的合成受阻,使KRAS無法成功識別上膜定位信號,最終形成內(nèi)體后被溶酶體降解。(圖5)
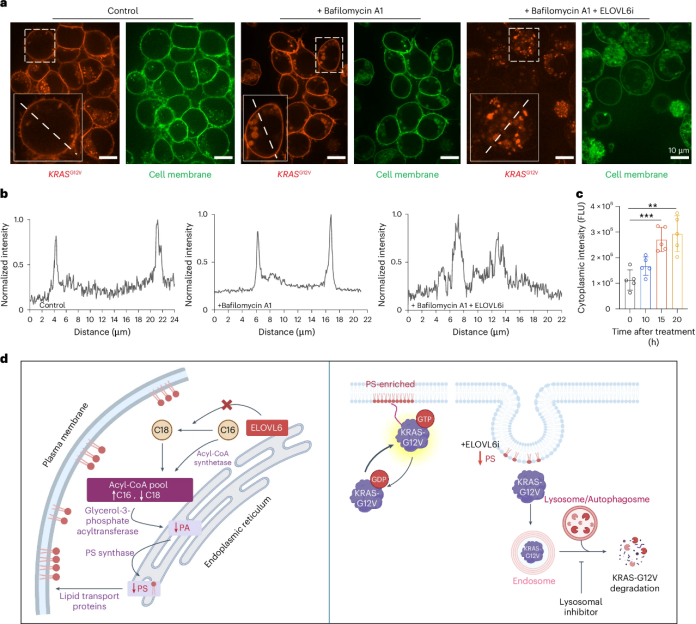
圖5. ELOVL6i通過溶酶體途徑將未定位的KRAS G12V突變體降解。
最后,作者團隊在KRAS G12V突變型異種移植小鼠模型(SW403、NCI-H441、CFPAC-1)中口服給予ELOVL6i,評估腫瘤生長和生存率。ELOVL6i顯著抑制腫瘤生長、延長小鼠生存期,并降低KRAS蛋白表達和ERK磷酸化水平。對30種KRAS突變細(xì)胞系的篩選顯示,ELOVL6i對多種KRAS突變(包括G12D、G13D等)均有效,尤其對KRAS依賴型細(xì)胞更敏感。(圖6)
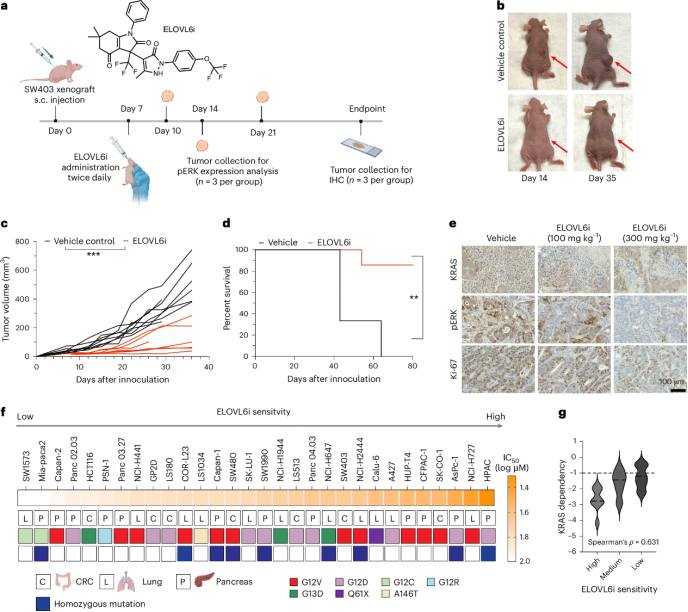
圖6. ELOVL6i能夠在多種動物模型中產(chǎn)生抗腫瘤和多種KRAS突變體靶向抑制活性。
綜上所述,本研究首次發(fā)現(xiàn)脂肪酸延長酶ELOVL6是KRAS G12V突變體蛋白水平的選擇性調(diào)控因子。ELOVL6通過調(diào)控脂質(zhì)代謝,特別是混合鏈磷脂酰絲氨酸的合成,維持KRAS G12V在細(xì)胞膜上的定位。抑制ELOVL6可導(dǎo)致KRAS G12V膜定位喪失,并通過溶酶體途徑降解,從而抑制其下游信號傳導(dǎo)和腫瘤細(xì)胞增殖。該研究不僅揭示了KRAS G12V的代謝依賴性調(diào)控機制,也為開發(fā)針對G12V及其他KRAS突變體的廣譜治療策略提供了新靶點和理論依據(jù)。
作者:DYH 審校:SYM
DOI: 10.1038/s41589-025-01998-x
Link: https://www.nature.com/articles/s41589-025-01998-x








