分享一篇發表在Cell Metabolism上的文章,標題為“Portal vein-enriched metabolites as intermediate regulators of the gut microbiome in insulin resistance”,通訊作者是來自哈佛大學醫學院的Ronald Kahn教授,他長期致力于糖尿病、胰島素信號傳導和代謝性疾病的研究并作出了卓越的貢獻。
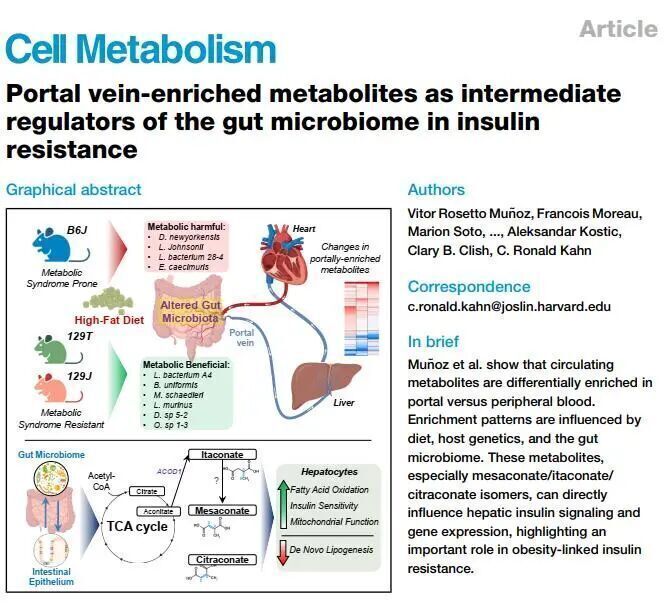
飲食和肥胖導致胰島素抵抗和二型糖尿病,其中一部分發病機制與腸道微生物組相關,因此抗生素治療能改善胰島素抵抗和葡萄糖耐受相關的疾病表型。腸道微生物代謝物通過門靜脈進入肝臟,基于此,作者對高脂飲食(high-fat diet, HFD)和抗生素處理小鼠的門靜脈代謝物和外周血代謝物進行研究,以期發現腸道來源的代謝物在這一過程中發揮的作用。
作者收集了四種條件飼養(正常飲食、HFD、HFD+萬古霉素、HFD+甲硝唑)的小鼠的門靜脈血和外周血(心臟血),并進行LC-MS分析,結果顯示,有111種代謝物在門靜脈中富集,有47種在外周血中富集。除脂質、膽汁酸以及來自細菌的代謝物外,作者發現,幾種與TCA循環相關的代謝物,包括烏頭酸、中康酸和2-羥基戊二酸在門靜脈中富集。HFD喂養的小鼠門靜脈和外周血富集的代謝物種類都有所下降,但TCA循環相關的代謝物并沒有變化,表明它們來源于腸道微生物或腸道,而非食物。隨后作者用兩種抗生素對小鼠進行處理,發現兩種抗生素都顯著影響了小鼠的腸道微生物組以及門靜脈代謝物的豐度。宏基因組分析也證實這幾種代謝物相關的微生物基因和腸道基因有所上調,表明微生物和腸道可能都有貢獻。通過對胰島素抵抗敏感性不同的小鼠腸道菌群進行研究,作者對代謝有益和有害的相關菌群進行了鑒定。
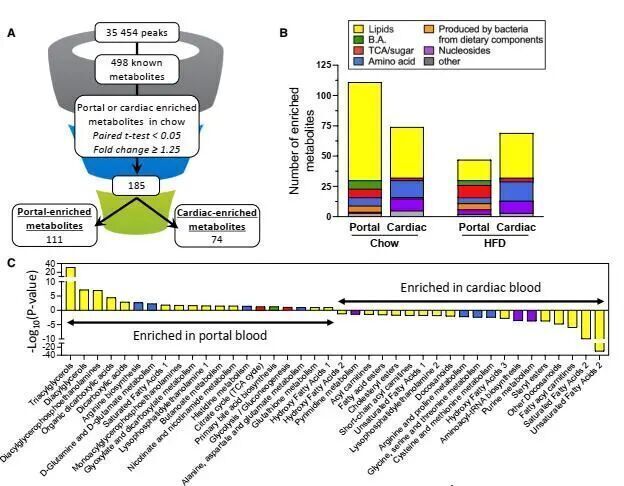
隨后,作者用中康酸和其同分異構體衣康酸及檸康酸對HepG2細胞進行處理,發現此類二羧酸可以抑制脂肪酸合成途徑并促進脂肪酸氧化途徑。小鼠活體實驗也證實了此類二羧酸小分子可以在調節脂肪酸代謝的同時恢復HFD小鼠原代肝細胞的胰島素抵抗。

總之,作者通過LC-MS分析,研究了高脂模型小鼠腸道微生物組相關的門靜脈代謝物與外周血代謝物變化,并研究了它們對肝臟代謝和高脂飲食相關的胰島素抵抗疾病的影響。
本文作者:ZCL
責任編輯:LZ
DOI:10.1016/j.cmet.2025.08.005.
原文鏈接:https://doi.org/10.1016/j.cmet.2025.08.005.








