分享一篇發表在Cell Metabolism上的文章,題目為:Genetics-nutrition interactions control diurnal enhancer-promoter dynamics and liver lipid metabolism. 本文通訊作者是廈門大學的張永有教授和美國貝勒醫學院的管棟印老師,張老師主要做表觀遺傳和腫瘤代謝等,管老師的課題組主要聚焦于晝夜節律基因表達與疾病風險的關聯研究。

哺乳動物的晝夜節律對維持生理穩態至關重要,其破壞是代謝疾病的重要風險因素。盡管核心生物鐘基因的機制已被初步闡明,但關于核心時鐘基因之外的遺傳變異如何影響外圍組織(如肝臟)的晝夜節律,以及它們如何與環境因素(如營養)相互作用,仍是領域內的一大空白。近年研究發現,表觀遺傳調控(如增強子-啟動子相互作用E-PIs)被證明能將環境信號與基因轉錄節律相連接。然而,遺傳變異對節律性E-PIs的影響及其在人類復雜代謝性狀與疾病中的作用機制遠未明確。
作者通過整合遺傳變異信息與人類肝臟RNA-seq數據,發現位于增強子和啟動子區域的單核苷酸多態性(SNPs)能夠個體化地調控附近基因的晝夜節律性表達——例如脂滴形成關鍵基因PLIN2的節律性表達僅出現在攜帶特定基因型(rs578602的AA型)的個體中,且這種調控獨立于對基因總體表達水平的影響。
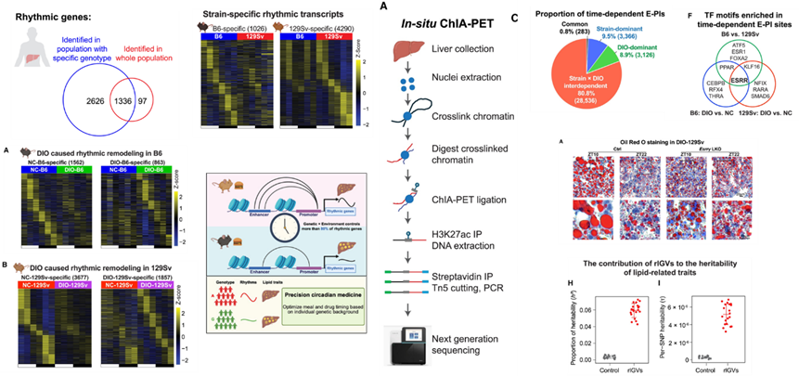
為深入探究其因果機制,本研究引入了小鼠模型。作者比較了不同遺傳背景的小鼠在不同飲食下的肝臟多組學動態響應。一個突破性的發現是:遺傳和營養這兩個因素并非獨立作用,而是相互交織,共同控制了超過80%的節律性基因和增強子-啟動子相互作用(E-PIs)。這意味著,相同的飲食會對不同基因型的個體產生截然不同的節律性代謝影響。通過轉錄因子motif分析,一個非經典的時鐘調控因子——雌激素相關受體γ(ESRRγ)——浮出水面。
接著,研究通過功能實驗驗證了ESRRγ的核心地位。肝臟特異性敲除Esrrγ基因后,原本由遺傳和飲食調控的、與脂滴形成和脂質代謝相關的節律性基因表達和E-PIs被顯著破壞,證明ESRRγ是執行這種遺傳-營養互作調控的關鍵分子樞紐。最后,研究回歸到人類疾病的臨床相關性。作者在肥胖患者的脂肪肝組織中發現,那些與節律基因表達相關的SNPs,同樣富集于動態的E-PI區域,并且與ESRRγ的結合模序相關,這些遺傳位點最終與人類的脂代謝性狀緊密相連。
總而言之,這項研究成功地描繪了一條從“個體遺傳變異”到“宏觀代謝表型”的完整調控通路:遺傳背景與營養信號通過調控核心轉錄因子(如ESRRγ),動態地重塑增強子-啟動子的三維互作網絡,從而決定組織特異性的基因表達節律,最終影響代謝穩態與疾病易感性。這一發現不僅革新了我們對生物鐘調控網絡復雜性的認知,更重要的是,它為解釋代謝疾病的個體差異提供了全新的“時間維度”視角,為未來針對個體生物鐘特點的“精準時序療法”奠定了堅實的理論基礎。
本文作者:JR
責任編輯:TZS
DOI:10.1016/j.cmet.2025.07.010
原文鏈接:https://doi.org/10.1016/j.cmet.2025.07.010








