分享一篇發(fā)表在Cell Chemical Biology上的文章:Discovery of a tau-aggregate clearing compound that covalently targets P4HB,通訊作者是來(lái)自Scripps的Christopher G. Parker教授和AbbVie公司的Shaun M. McLoughlin,Christopher G. Parker課題組致力于開(kāi)發(fā)化學(xué)策略來(lái)研究人類(lèi)生物學(xué)和疾病病理學(xué)。

神經(jīng)退行性疾病的發(fā)生發(fā)展和tau蛋白的異常折疊和聚集密切相關(guān),但人們對(duì)tau蛋白的發(fā)病機(jī)制知之甚少,有效的治療方法有限。近年來(lái),表型篩選已成為一種強(qiáng)大的藥物發(fā)現(xiàn)策略,可以高通量地發(fā)現(xiàn)不同疾病的特異性藥物。隨著化學(xué)蛋白質(zhì)組學(xué)的發(fā)展,它也可以結(jié)合表型篩選,用以加快靶標(biāo)識(shí)別。本文作者利用表型篩選和化學(xué)蛋白質(zhì)組學(xué)發(fā)現(xiàn)可清除tau聚集體的化合物,并解析了它的靶點(diǎn)。
作者首先構(gòu)建了表型篩選的模型。作者在SH-SY5Y細(xì)胞中穩(wěn)定表達(dá)C末端融合GFP的 tau單體,當(dāng)細(xì)胞在表達(dá)配對(duì)的螺旋片段sPHF時(shí)容易發(fā)生聚集。如此便能人工控制蛋白的聚集,用化合物庫(kù)對(duì)存在tau聚集的細(xì)胞進(jìn)行處理,然后通過(guò)細(xì)胞固定-顯微成像的方式對(duì)聚集體進(jìn)行觀察和定量。為了促進(jìn)命中化合物的下游靶標(biāo)鑒定,作者選擇了383個(gè)光交聯(lián)的全功能化探針組成的化合物文庫(kù)。在沒(méi)有細(xì)胞毒性的情況下,使用平均EC50<10μM和平均最大tau清除率>50%作為命中選擇標(biāo)準(zhǔn),作者篩選到命中分子1a。
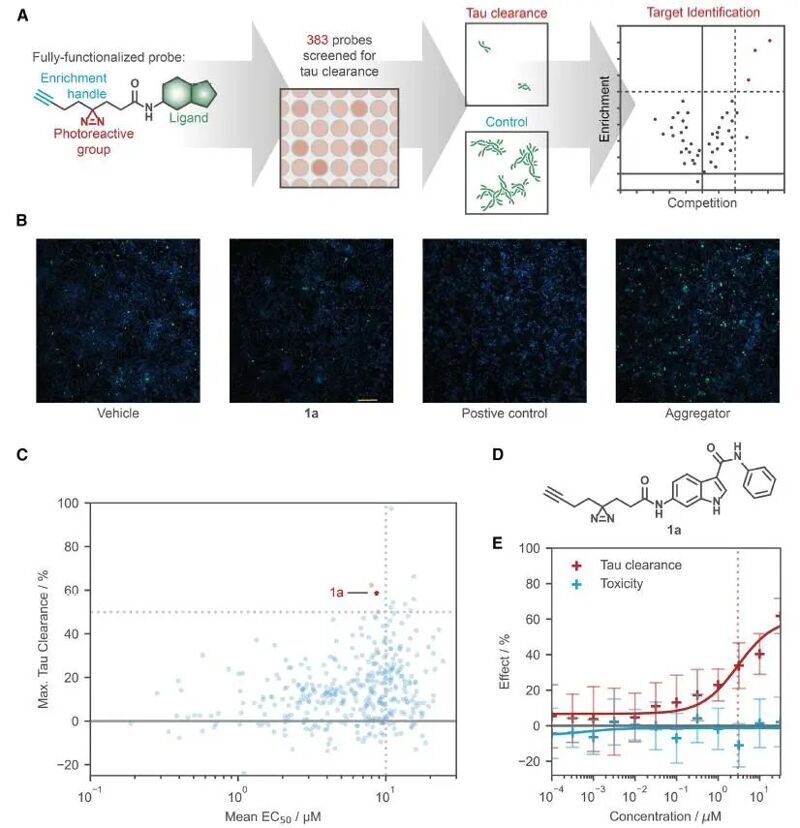
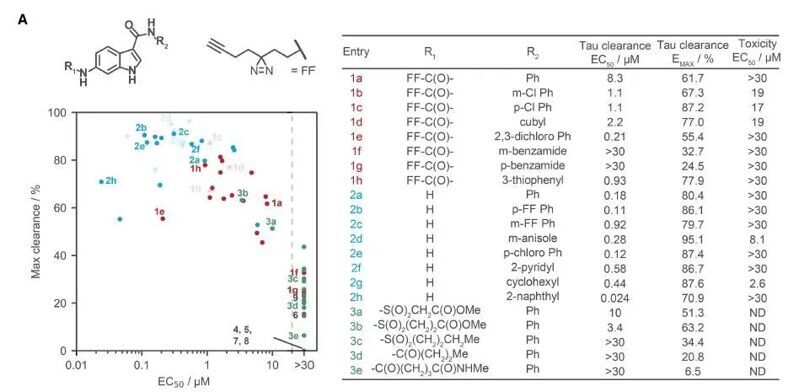
鑒于化合物1a的效力相對(duì)較低,并且原始文庫(kù)中的結(jié)構(gòu)類(lèi)似物有限,作者進(jìn)行了構(gòu)效分析,對(duì)化合物1a的芳基環(huán)進(jìn)行結(jié)構(gòu)優(yōu)化,獲得化合物2a,它的EC50 為0.31 μM,最大tau清除率為91%,沒(méi)有觀察到細(xì)胞毒性。
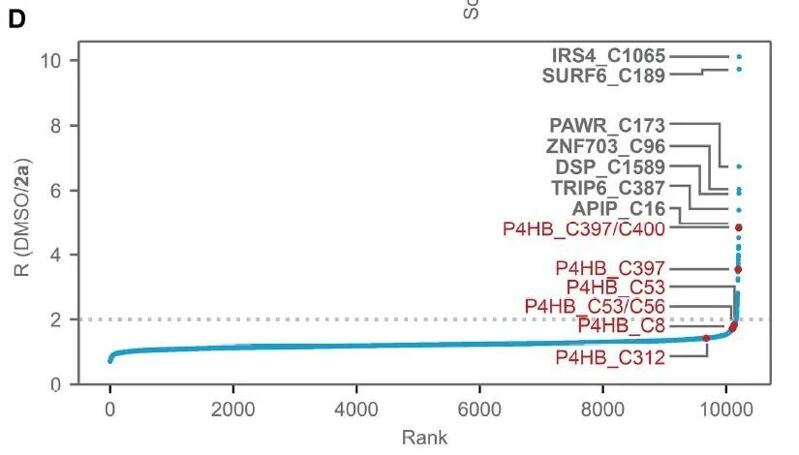
為了確定優(yōu)化化合物的機(jī)制相關(guān)靶標(biāo),作者使用了基于光親和力的化學(xué)蛋白質(zhì)組學(xué)探索了 2b 的相互作用組。通過(guò)此方法,作者篩選到一些靶點(diǎn),包括含硒代半胱氨酸的蛋白SELK、SELT、SELS 和TXNRD1、含硫氧還蛋白結(jié)構(gòu)域的蛋白TMX1和P4HB、氧化還原活性蛋白HMOX2和細(xì)胞遷移蛋白MIEN1。隨后,作者在細(xì)胞模型中進(jìn)行了靶點(diǎn)敲低實(shí)驗(yàn),發(fā)現(xiàn)只有P4HB是陽(yáng)性靶點(diǎn)。雖然P4HB在細(xì)胞內(nèi)具有多種功能,但研究最充分的是它通過(guò)兩個(gè)催化活性硫氧還蛋白結(jié)構(gòu)域在二硫鍵斷裂和重形成中的作用,這些結(jié)構(gòu)域以CxxC基序為特征。作者用碘乙酰胺-去硫代生物素探針(IA-DTB)處理,與化合物2a進(jìn)行競(jìng)爭(zhēng),結(jié)果表明C397/C400位點(diǎn)的P4HB肽段是競(jìng)爭(zhēng)最強(qiáng)的肽,說(shuō)明2a可能經(jīng)歷代謝激活以形成共價(jià)修飾C397的半胱氨酸反應(yīng)物質(zhì)。
總而言之,本文作者通過(guò)表型篩選發(fā)現(xiàn)可清除tau聚集體的化合物,優(yōu)化的氨基吲哚可有效清除多種tau蛋白病模型中的聚集體,并用化學(xué)蛋白質(zhì)組學(xué)揭示了內(nèi)質(zhì)網(wǎng)酶P4HB是共價(jià)靶點(diǎn)。
本文作者:MB
責(zé)任編輯:LZ
DOI:10.1016/j.chembiol.2025.09.006
原文鏈接:https://doi.org/10.1016/j.chembiol.2025.09.006








