摘 要:轉錄組測序技術是一種新發展的轉錄組學研究方法。在物種基因組信息未知的情況下,進行測序得到遺傳信息,轉錄組測序技術是很重要的分子生物學方法,已經被廣泛應用于各個研究領域。而藥用植物遺傳信息匱乏,對藥用植物的轉錄組進行測序在基因組學是比較活躍的領域,可以了解植物的基因表達并分析其功能和調控機制。對藥用植物的轉錄組學研究有助于解決遺傳育種、篩選優良抗性基因等問題。介紹了轉錄組測序的發展,并從功能基因挖掘和次生代謝產物途徑探索等方面綜述了近年來轉錄組測序在藥用植物研究中的應用,為藥用植物的研究提供了更多基礎數據。
轉錄組測序(transcriptome sequencing)是對某一物種的mRNA進行高通量測序,而轉錄組測序的結果反映了特定條件和特定時間點的基因表達情況。隨著時間或外部的環境變化,轉錄組也會隨之變化,除了轉錄衰減和mRNA降解現象,轉錄組包括了細胞內所有能轉錄出的mRNA,而轉錄組測序的結果反映了特定條件和特定時間點的基因表達情況[1]。在參考基因組序列存在的情況下,轉錄組測序可以實現序列的變異鑒定[2-4]、空間和時間表達譜測定[5-6]、基因模型結構的驗證和鑒定[7-8]。在沒有參考基因組的情況下,轉錄組測序也可以挖掘基因[9-12],進行對比分析[13],計算其表達豐度[14-15]。
轉錄組研究的方法比較多,如基因表達序列分析(serrial analysis of gene expression)、表達序列標簽(expressedsequence tag,EST)、基因芯片、高通量測序等[16-17]。而現階段轉錄組學研究主要依靠高通量測序技術。但是,對于非模式生物來說,大多數植物的基因組信息較為匱乏,而高通量測序的優勢在于無需參考基因組,在沒有獲得物種的基因組信息的情況下仍可以進行轉錄組測序。另外,高通量測序獲得的數據可以覆蓋全部轉錄本,這對于挖掘功能基因是十分有利的。
1 轉錄組測序技術
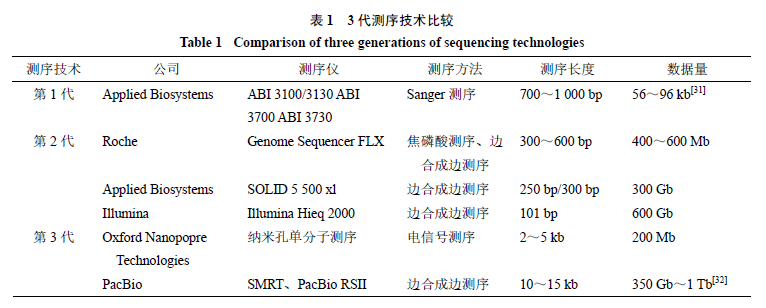
1.1 第1代測序技術
沃森和克里克在1953年發現了雙螺旋結構[18],了解核酸的空間結構后,人們開始研究對應的序列信息,測序技術也開始發展。1964年,Holley完成了對酵母丙氨酸轉移tRNA的測序[19],自此核酸測序才正式出現。隨后測序技術迅速發展。1977年,生物化學家Sanger發明了鏈終止測序法,一種基于T4 DNA聚合酶和大腸桿菌DNA聚合酶的快速DNA測序方法[20-21]。同年,Gilbert發明了化學降解測序法[22]。這2種測序技術被認為是第1代測序技術。而后Sanger測序法漸漸占據了主要地位,現在普遍認為第1代測序技術為Sanger測序法。
1.2 第2代測序技術
人類基因組的測序工作結束后,人們想通過測序的方法來獲得其他物種的基因信息[23-24]。而傳統的Sanger測序法比較費時費力、低通量且成本很高,不能滿足日益增長的測序需求。很快人們開發出了第2代測序技術(next-generationsequencing,NGS)。第2代測序技術成本低、速度快,而且覆蓋度較深,可以同時對數百萬個DNA進行測序,核酸測序技術進入自動化時代[25-27],漸漸取代了Sanger測序法。高通量測序目前可在5個主要商業平臺上獲得:Roche(454)、ABI-SOLi D、Illumina基因組分析儀、Ab I3730xl基因組分析儀以及Heli Scope。現今應用較多的為前3者。
1.3 第3代測序技術
隨著時間的推移,第2代測序技術的各種問題漸漸凸顯,隨后誕生了第3代測序技術,比較有代表性的測序技術:納米孔單分子測序技術(Oxford Nanopopre Technologies公司)和單分子實時測序(single-molecular real-time,SMRT,PacBio公司)。第3代測序技術使用的是單分子測序技術,通量高和測序讀數長。近年來應用較為廣泛的是PacBio RSII測序平臺,無需進行PCR擴增即可完成測序。平均讀長可以達到10~15 kb,而最大讀長可達64.5 kb[28]。而第3代測序的準確率明顯比前2代低,PacBio公司的SMRT測序技術準確率只能達到85%左右[29]。這樣一來,為了控制錯誤率無形中增加了測序的技術難度和成本[30]。
2 轉錄組測序技術在藥用植物中的應用
藥用植物合成了無數的次級代謝產物,而這些次生代謝產物是研發新藥的重要來源,如青蒿素(artemisinin)、人參皂苷(ginsenoside)、紫杉醇(taxol)等,但是它們的含量并不是很高。所以造成了藥用植物的無序開發,資源日益減少。通過克隆關鍵酶基因及代謝工程生產藥用植物藥效成分已經成為藥物生產和新藥開發的主要研究方法[33]。
相比已經完成基因組測序的模式生物,藥用植物缺少基因組數據,遺傳背景不清晰,發展緩慢。藥用植物高通量轉錄組測序技術的出現,可以挖掘藥用植物有效成分生物合成的功能基因并分析其表達規律,探索有效成分的生物合成途徑及其調控機制,從而提高藥用植物有效成分的含量。藥用植物高通量測序為挖掘功能基因、探索藥用植物有效成分的生物合成途徑與調控機制、探索藥材道地性分子機制、闡明基因功能提供了新工具。通過測序得到的信息,還可以挖掘參與植物生長發育、抗病抗逆等優良性狀的基因。對于藥用植物的保護具有極其重大的意義[33-37]。
2.3 次生代謝產物生物合成途徑挖掘
三萜皂苷是遠志Polygala tenuifolia Willd.重要的藥用成分之一。對不同年份的遠志進行轉錄組測序[66],有176個Unigenes參與萜類化合物骨架生物合成,參與其他次級代謝產物的生物合成的Unigenes有522個。杠柳Periplocasepium Bunge中主要的生物活性物質C21類固醇和杠柳毒苷均來自類固醇合成途徑,對杠柳葉、根、不定根及愈傷組織進行轉錄組測序[67],篩選到24個參與類固醇生物合成途徑的基因。貫葉金絲桃Hypericum perforatum L. 中的金絲桃素和褪黑激素是其主要的活性成分,具有抗抑郁、抗炎、抗病毒、抗癌和抗菌作用,測序結果[12]顯示,2359個Unigenes與次生代謝產物通路有關,與金絲桃素和褪黑激素合成有關的Unigenes有260個。對虎杖Polygonum cuspidatum Sieb. et Zucc. 根部進行轉錄組測序[68],獲得86 418個Unigenes,總共有22 572個Unigenes注釋到了119個KEGG通路。分別有12、18、60、54個Unigenes分別注釋到甲羥戊酸(MVA)、甲基- D-赤蘚糖醇-4-磷酸(MEP)、莽草酸和白藜蘆醇生物合成途徑。
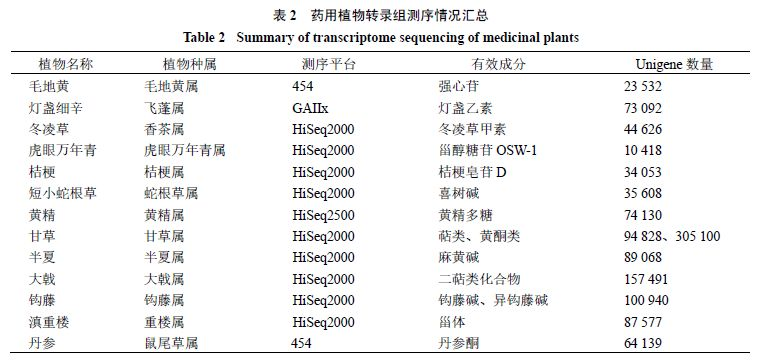
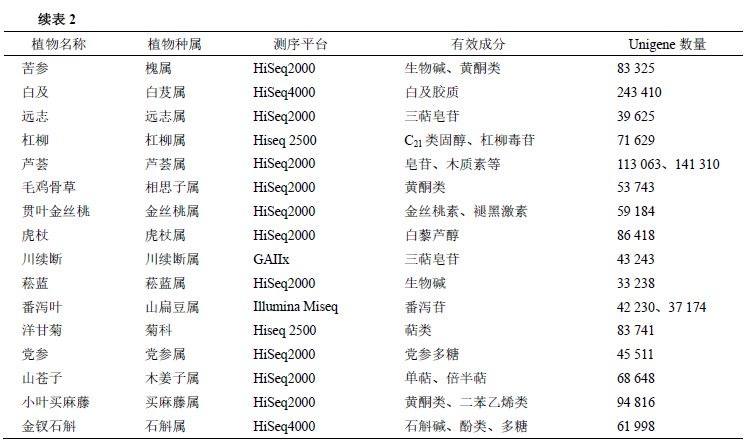
轉錄組測序技術應用于藥用植物的研究情況見表2。
3 結語
本文綜述了轉錄組測序技術在藥用植物中的研究進展,轉錄組測序技術是一種轉錄組學的研究方法,遺傳信息可以通過測序獲得,在物種基因組信息未知的情況下,通過測序可得到遺傳信息。由于藥用植物遺傳信息的匱乏,轉錄組測序技術逐漸應用于藥用植物轉錄組的研究中。為了保護重要的藥用植物及瀕危藥用植物的多樣性及其可持續利用,在轉錄組水平上進行測序是非常必要的。
本文從功能基因挖掘、SSR分子標記開發和次生代謝產物生物合成途徑探索3個方面闡述了轉錄組測序技術在藥用植物中的應用。除了以上應用以外,轉錄組學的應用推進了藥用植物中天然產物發現。植物可合成無數次級代謝產物,而這些次生代謝產物可以作為藥物開發的新來源,研究藥用植物有效成分的生物合成及其遺傳機制有助于大規模生產這些有效成分。轉錄組測序技術還可以應用于某些有毒中藥的減毒研究,它的出現有助于選育品質產量皆優的藥用植物,闡明藥用植物遺傳信息及調控網絡,探索中藥防病治病的分子機制。轉錄組測序技術在藥用植物研究領域必將擁有廣闊的應用前景。
參考文獻(略)
來 源:慧 芳,劉秀巖,李宗諭,劉福順,楊世海. 轉錄組測序技術在藥用植物研究中的應用 [J]. 中草藥, 2019, 50(24):6149-6155.








