烯烴的均相催化加氫,氫順式加成。另外、炔也可用同樣的方法得到烷烴。均相體系有利于反應條件更加溫和和實現良好的化學選擇性。另一方面,后處理上稍微比非均相反應要麻煩一些。
利用DIPAMP,實現了L-DOPA的工業化生產的W.S.Knowles、以及BINAP的發明者野依良治已經獲得了2001年的諾貝爾化學獎。
基本文獻
?Wilkinson catalyst: (a) Osborn, J. A.; Jardine, F. H.; Young, J. F.; Wilkinson, G. J. Chem. Soc. A 1966, 1711. doi:10.1039/J19660001711 (b) Harmon, R. E.; Gupta, S. K.; Brwon, D. J. Chem. Rev. 1973, 73, 21. DOI: 10.1021/cr60281a003
?Birch, A. J.; Williamson, D. H. Org. React. 1976, 24, 1.
?Crabtree catalyst: (a) Crabtree, R. H. Acc. Chem. Res. 1979, 12, 331. DOI: 10.1021/ar50141a005 (b) Crabtree, R. h.; Davis, M. W. J. Org. Chem. 1986, 51, 2655.DOI: 10.1021/jo00364a007
?Asymmetric Hydrogenation: (a) Ojima, I.; Clos, N.; Bastos, C. Tetrahedron 1989, 45, 6901. doi:10.1016/S0040-4020(01)89159-6 (b) Gridner, I. D.; Imamoto, T. Acc. Chem. Res. 2004, 37, 633. DOI: 10.1021/ar030156e
反應機理
Wilkinson配體的情況、烯的插入是決定反應速率的階段、因此容易配位的底物更容易發生反應。反應能力遵循以下順序:
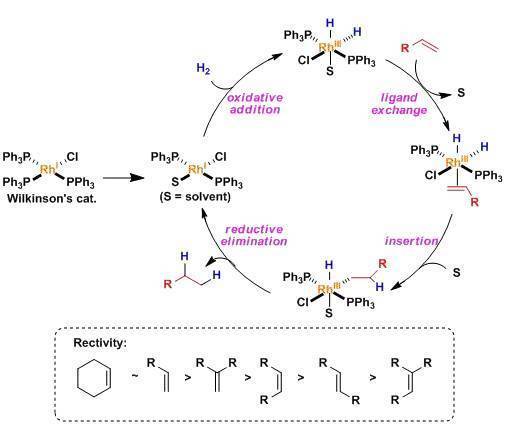
反應實例
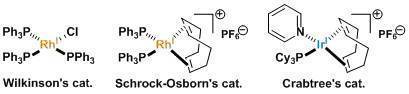
Schrock-Osborn催化劑或Crabtree催化劑那樣的陽離子催化劑、近旁有能配位的官能團存在的話,能定位催化劑達到立體選擇性還原。[1]
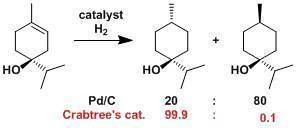
選擇性還原烯烴的例子。硝基,氰基,羰基等不會被還原。有醛的存在會發生脫羰基化,因此不能做底物使用。

L-DOPA的工業不對稱加氫

Taxol的合成[2]

加入二氮配體的話、化學選擇性會發生大的改變。這可以由胺上的氫和羰基的氧相互作用的中間態來解釋。(參照野依不對稱氫遷移反應)。
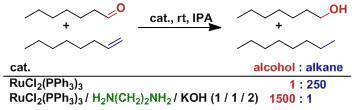
實驗步驟
硝基烯烴的還原[3]
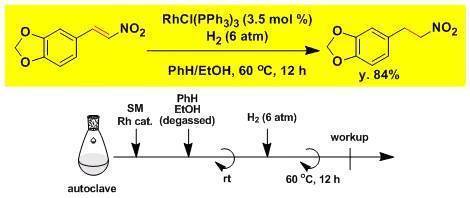
實驗技巧
通常被稱為Wilkinson配體的Rh配體是首選、反應活性較低的四取代烯烴不發生反應。用Ir做中心的Crabtree催化劑能使四取代的烯烴發生還原反應。
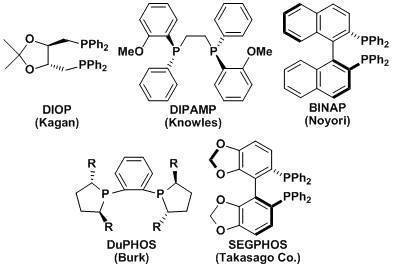
使用不對稱的雙齒磷配體的不對稱加氫技術,到現在有了高速的發展、多種加氫過程已經被應用于工業生產。在這之中,以下的配體都是具有非常的歷史價值和實用性的。
參考文獻
[1] (a) Crabtree, R.H. Davis, M. W. J. Org. Chem. 1986, 51, 2655. DOI: 10.1021/jo00364a007 (b) Brown, J. M.; Hall, S. A.Tetrahedron Lett. 1984, 25, 1393. doi:10.1016/S0040-4039(01)80167-2
[2] Wender, P. A. et al. J. Am. Chem. Soc. 1997, 119, 2755 & 2757. DOI: 10.1021/ja9635387 DOI: 10.1021/ja963539z
[3] Harmon, R. E.; Parsons, J. L.; Cooke, D. W.; Gupta, S. K.; Schoolenberg, J. J. Org. Chem. 1969, 34, 3684. DOI:10.1021/jo01263a122
轉自“化學空間”








