木藜蘆烷二萜天然產(chǎn)物(-)-Rhodomollanol A全合成的簡介
杜鵑花科(Ericaceae)植物中富含結(jié)構(gòu)復(fù)雜且生物活性的萜類產(chǎn)物,其中已確定結(jié)構(gòu)的grayanane型二萜天然產(chǎn)物就多達(dá)150種,絕大多數(shù)的木藜蘆烷類毒素(Grayanoid)家族分子在特征性的[5,7,6,5]四環(huán)碳骨架基礎(chǔ)上分布著7?10個(gè)手性中心以及多個(gè)羥基官能團(tuán),這種高度氧化的多環(huán)結(jié)構(gòu)分子一般都具有良好的生物活性,例如免疫調(diào)節(jié)(immunomodulatory)、抗癌(anticancer)、抗病毒(antiviral)、鎮(zhèn)痛(antinociceptive)以及鈉離子通道拮抗(sodiumchannel antagonistic)等。代表性的天然分子如下圖1所示:
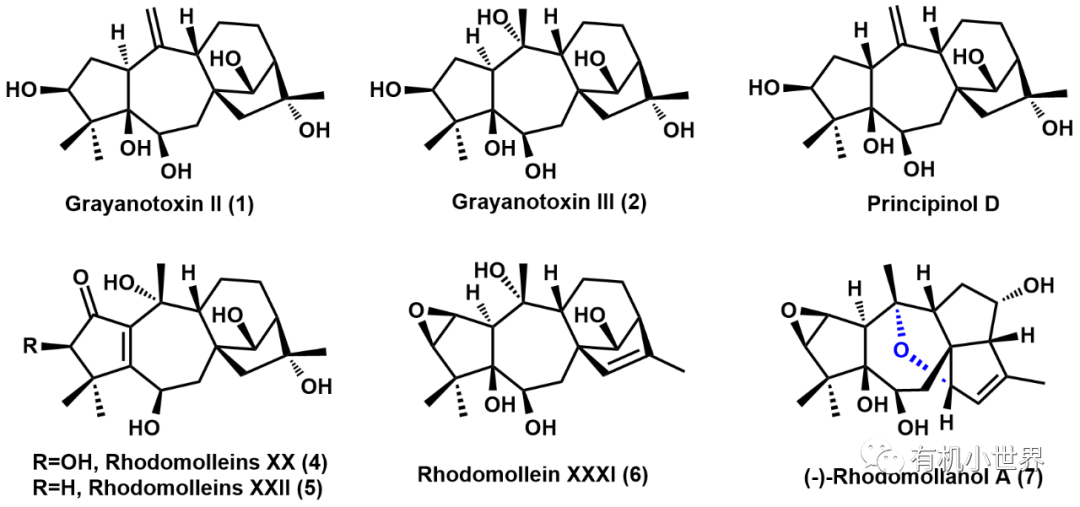
圖1.Grayanane型二萜天然產(chǎn)物
Grayanane型二萜天然產(chǎn)物Rhodomollein XXXI (6)是從具有藥用價(jià)值的杜鵑花科植物黃杜鵑(rhododendron molle)的葉子中分離得到的,同時(shí)分離得到了少量(–)-Rhodomollanol A (7)。(-)-7具有更加復(fù)雜的[3,5,7,5,5,5] 六環(huán)骨架結(jié)構(gòu),碳骨架上有11個(gè)連續(xù)手性中心,7-oxabicyclo[4.2.1]nonane核心上并有三個(gè)環(huán)戊烷環(huán)系;初步研究表明(-)-7對PTP 1B具有中度抑制活性。有研究表明,在生物體內(nèi)(-)-7可以從6經(jīng)過一系列轉(zhuǎn)化得到,如下圖2:
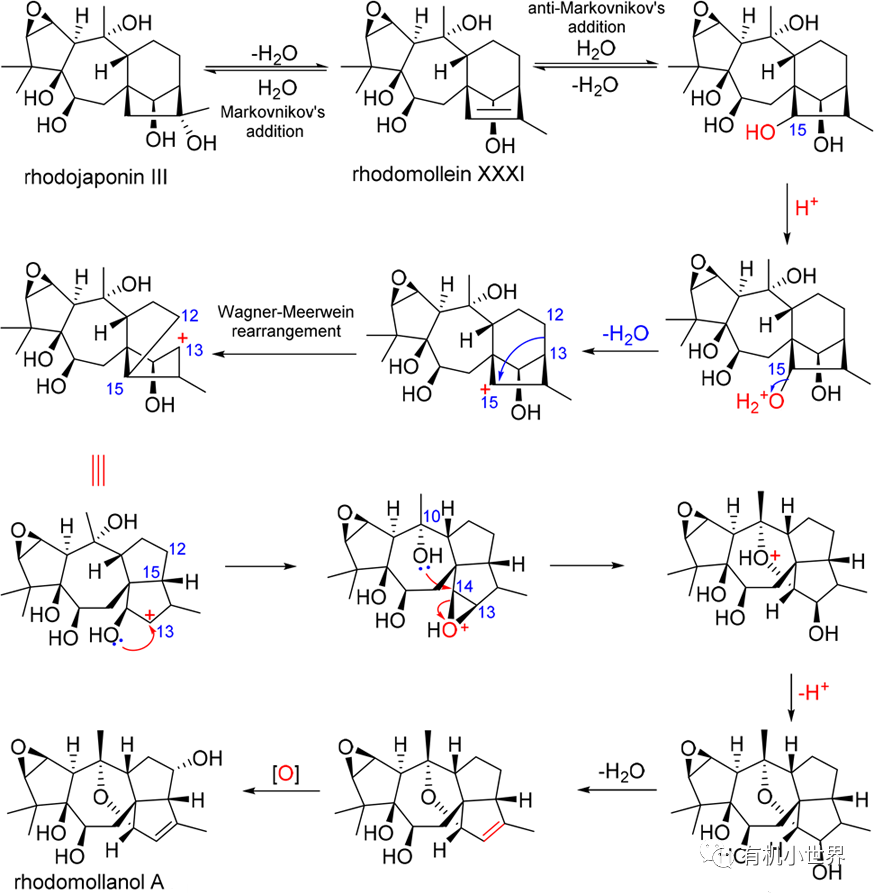
圖2.(–)-Rhodomollanol A的生源合成路徑
Timothy R. Newhouse課題組合成Principinol D。
J. Am.Chem. Soc. 2019,141, 8088-8092. Doi:10.1021/jacs.9b03751.
耶魯大學(xué)(Yale University)的Newhouse課題組主要從事于計(jì)算化學(xué)輔助的天然產(chǎn)物全合成和合成方法學(xué)的研究,聚焦于具有優(yōu)異神經(jīng)活性的天然產(chǎn)物骨架,期望此類化學(xué)小分子探針能夠用于神經(jīng)功能的基礎(chǔ)研究,從而解決神經(jīng)功能障礙;同時(shí)也在研究羰基化合物α,β-脫氫反應(yīng)。Newhouse課題組于2019年首次完成了Principinol D的全合成,具體的合成路線如下圖3:
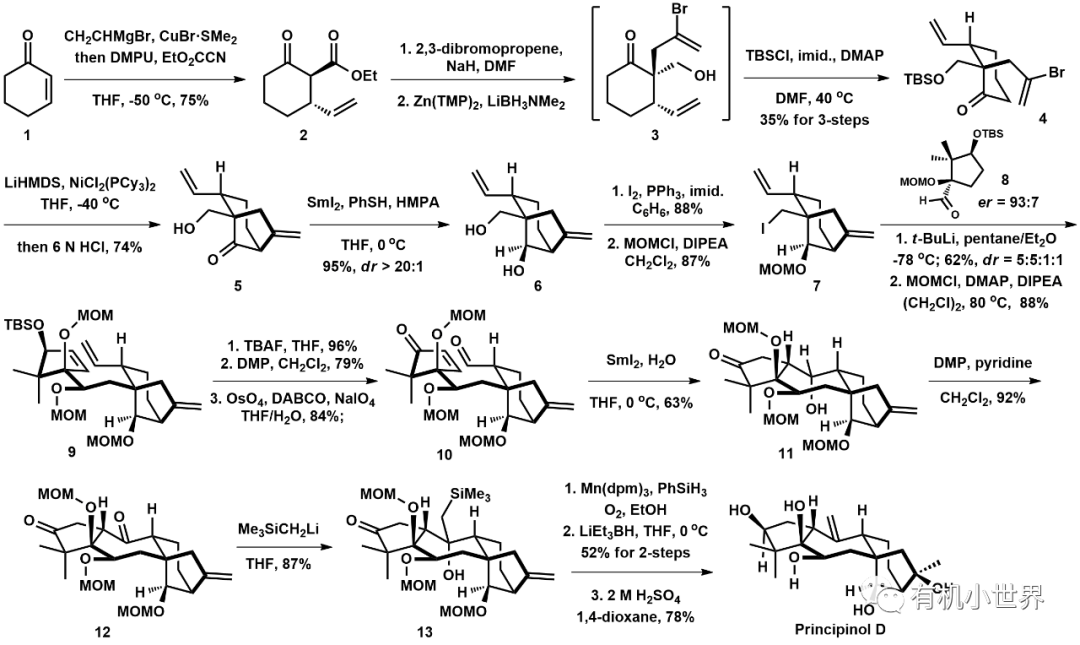
圖3.Newhouse課題組合成Principinol D
整體采用匯聚式的合成路線,第一階段是合成[3.2.1]橋環(huán)碘代物7。作者以環(huán)己烯酮1為原料,通過六元環(huán)構(gòu)象控制的立體選擇性的1,4-加成和羰基α-位的親核取代反應(yīng),引入構(gòu)建并環(huán)結(jié)構(gòu)所需的側(cè)鏈;堿性條件下Ni催化的C-vinylation構(gòu)建[3.2.1]橋環(huán)結(jié)構(gòu),SmI2高立體選擇性的還原羰基(HMPA提高SmI2的還原電勢;PhSH作為H atom donor,提高dr),然后碘代后得到碘代物片段7。
第二階段是完成5-7-6-5并環(huán)骨架的構(gòu)建。外消旋的碘代物7經(jīng)過鋰鹵交換后加成到enantioenriched的醛8上,得到四個(gè)非對映異構(gòu)體(dr = 5:5:1:1,需要的單一非對映異構(gòu)體產(chǎn)率為26%),其中新生成的羥基的手性中心可以通過Felkin-Anh模型進(jìn)行解釋;將末端雙鍵轉(zhuǎn)化成醛后,還原偶聯(lián)反應(yīng)連接烯酮和醛兩部分,構(gòu)建中心的七元環(huán)結(jié)構(gòu);后期再通過多步立體選擇性的還原反應(yīng)引入分子中多個(gè)羥基,堿性條件下的Peterson olefination反應(yīng)引入雙鍵單元,最終完成Principinol D的全合成。
采用匯聚式的合成策略使整個(gè)合成路線大為縮短,在[3.2.1]橋環(huán)結(jié)構(gòu)的基礎(chǔ)上引入帶有五元環(huán)結(jié)構(gòu)的片段,通過高立體選擇性的還原偶聯(lián)反應(yīng)構(gòu)建中心七元環(huán)結(jié)構(gòu);合成過程中每一步立體選擇性還原都經(jīng)過大量的條件篩選,非常規(guī)的反應(yīng)條件得到最優(yōu)的實(shí)驗(yàn)結(jié)果。雖然實(shí)現(xiàn)了Principinol D的不對稱合成,但由于參與反應(yīng)的碘代物7是外消旋的,整體的合成效率不高,雖然理論上在合成第一步通過手性Lewis參與的不對稱1,4-加成可以實(shí)現(xiàn)手性化合物7的合成,但作者并未給出解釋。木藜蘆烷類毒素家族分子全合成研究由來已久,該合成工作極為精巧,合成路線中所用的很多反應(yīng)手段對于解決相關(guān)的化學(xué)問題重要的指導(dǎo)作用。
浙江大學(xué)丁寒鋒課題組合成木藜蘆烷二萜。
Angew.Chem. Int. Ed. 2019,58, 8556. Doi: 10.1002/anie.201903349.
J. Am.Chem. Soc. 2017,139, 6098-6101. Doi:10.1021/jacs.7b02746.
J. Am.Chem. Soc. 2020, 142, 4592-4597. Doi: 10.1021/jacs.0c00308.
浙江大學(xué)丁寒鋒課題組研究領(lǐng)域主要是重要生物活性天然產(chǎn)物全合成及藥物化學(xué)研究以及導(dǎo)向天然產(chǎn)物(藥物)的新合成方法學(xué)研究。早在2019年,該課題組發(fā)展了一類Ti(III)介導(dǎo)的環(huán)氧還原開環(huán)/Beckwith-Dowd重排串聯(lián)反應(yīng),在復(fù)雜體系中實(shí)現(xiàn)了從雙環(huán)[2.2.2]辛烷骨架向雙環(huán)[3.2.1]辛烷骨架的高效轉(zhuǎn)化,并以此為關(guān)鍵步驟高效完成了木藜蘆烷二萜Rhodomolleins XX和XXII的首次全合成,具體的合成路線如下圖4:
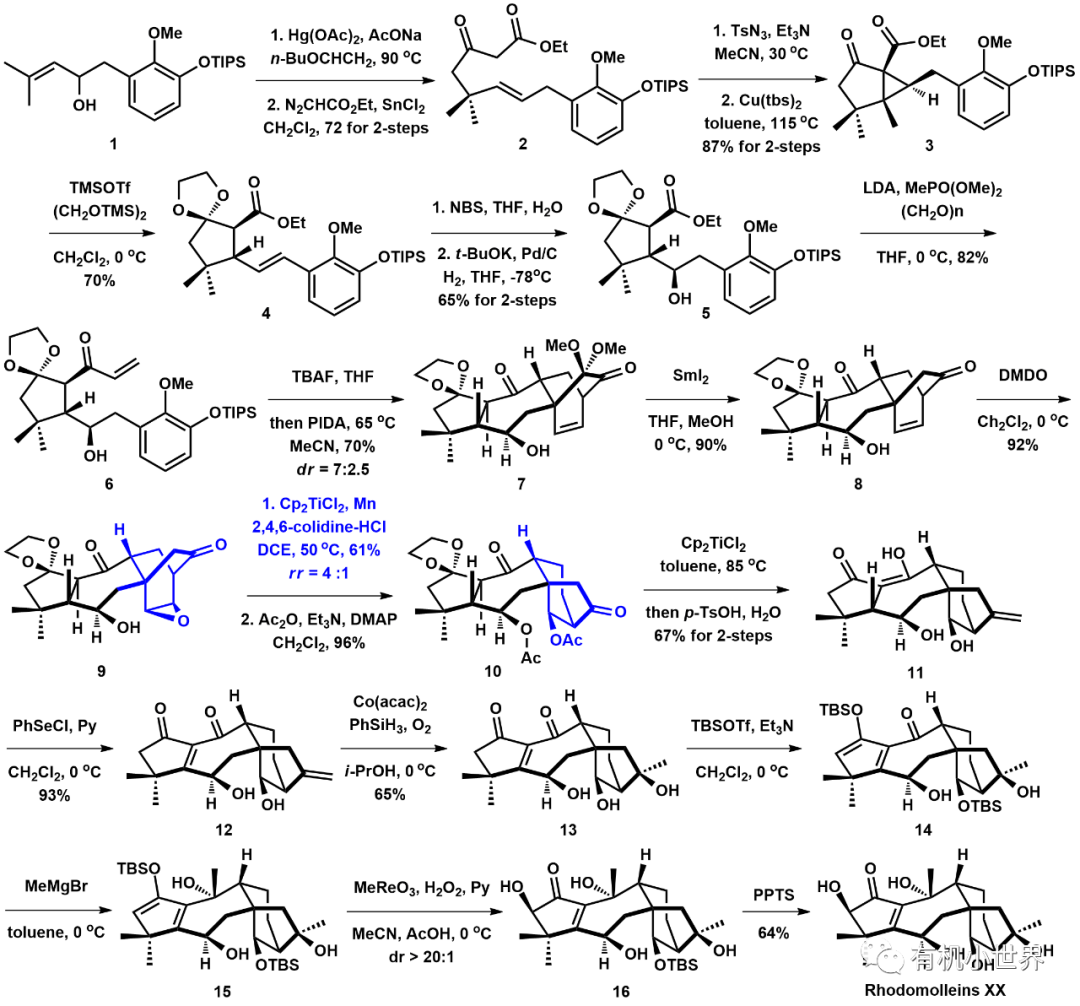
圖4.丁寒鋒課題組合成Rhodomolleins XX和XXII
此外,丁寒鋒課題組在2017年發(fā)展了一種全新的氧化去芳構(gòu)化分子內(nèi)[5+2]環(huán)加成/頻哪醇重排串聯(lián)反應(yīng)。從簡單易得的烯基苯酚出發(fā),以六氟異丙醇為溶劑,在有機(jī)三價(jià)碘試劑(如PIFA)氧化下,可一步生成3個(gè)環(huán)和3個(gè)立體中心,快速構(gòu)建出雙環(huán)[3.2.1]辛烷骨架結(jié)構(gòu)。以該串聯(lián)反應(yīng)作為關(guān)鍵步驟,該課題組從已知的手性萘烷衍生物出發(fā),并結(jié)合Eschenmoser?Tanabe裂解、逆-Aldol/Aldol串聯(lián)反應(yīng)和Schenck Ene反應(yīng),以14?16步實(shí)現(xiàn)了高氧化態(tài)的貝殼杉烷二萜Pharicin A、Pharicinin B、Pseurata C和7-O-Acetylpseurata的首次不對稱全合成,具體的合成路線如下圖5:
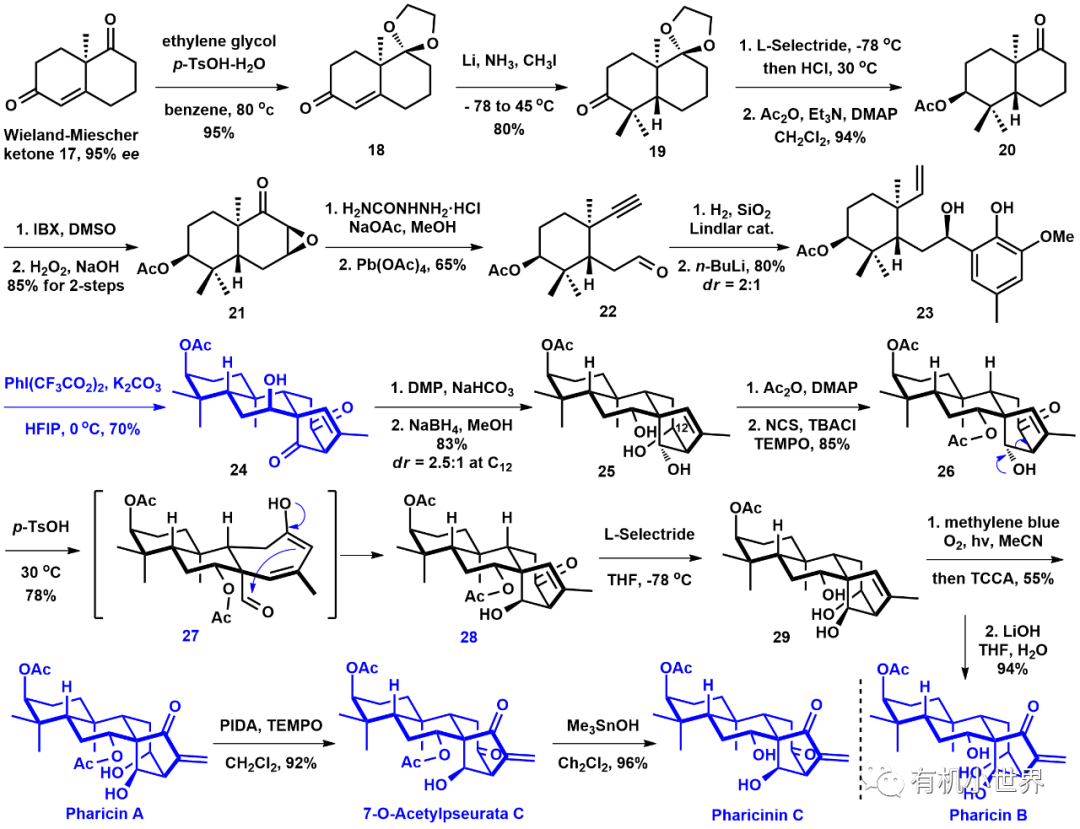
圖5.丁寒鋒課題組合成高氧化態(tài)的貝殼杉烷二萜
與經(jīng)典的木藜蘆烷二萜不同,(-)-Rhodomollanol A具有更高合成挑戰(zhàn)性的[3,5,7,5,5,5]六環(huán)體系,其中包含一個(gè)獨(dú)特的7-氧雜雙環(huán)[4.2.1]壬烷核心骨架和11個(gè)連續(xù)的手性中心。在之前工作的啟發(fā)之下,丁寒鋒課題組設(shè)計(jì)了如下的合成策略,如下圖6:以Wieland-Miescher酮為起始原料,利用氧化去芳構(gòu)化分子內(nèi)[5+2]環(huán)加成反應(yīng)快速構(gòu)建四環(huán)核心骨架;通過Lewis催化的開環(huán)、逆Dieckmann裂解以及vinylogous Dieckmann環(huán)化反應(yīng)引入順式5-5并環(huán)結(jié)構(gòu);雙烯酮32在光照下發(fā)生Nazarov環(huán)化反應(yīng)生成高張力的5-3-7并環(huán)結(jié)構(gòu),通過分子內(nèi)的環(huán)化反應(yīng)實(shí)現(xiàn)中心的七元環(huán)和氧橋環(huán)結(jié)構(gòu)的構(gòu)建;最后在核心骨架的基礎(chǔ)上進(jìn)行一系類的官能化操作,立體選擇性的引入(-)-Rhodomollanol A分子中多個(gè)羥基單元。
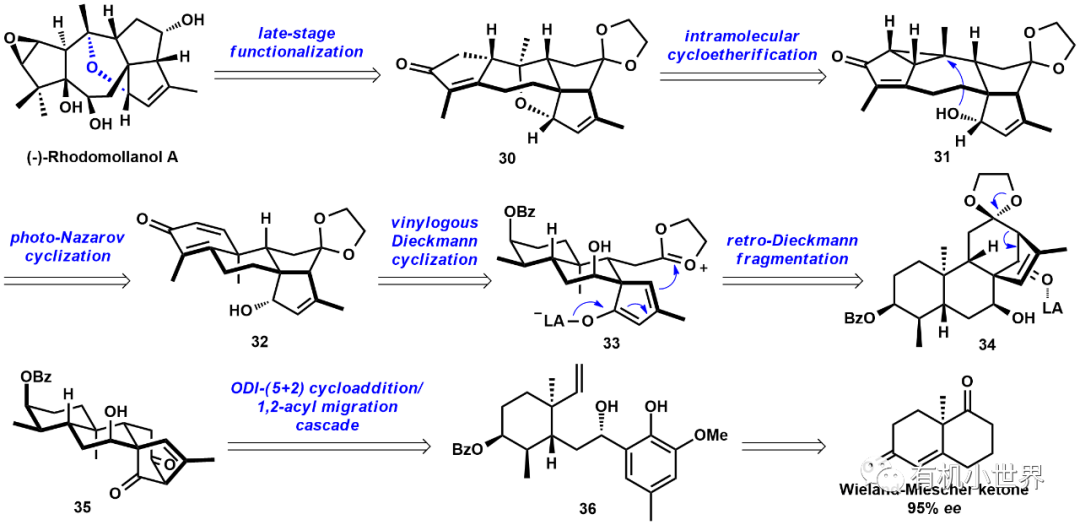
圖6.丁寒鋒課題組合成(-)-Rhodomollanol A的逆合成分析
具體的合成路線如下圖7所示:
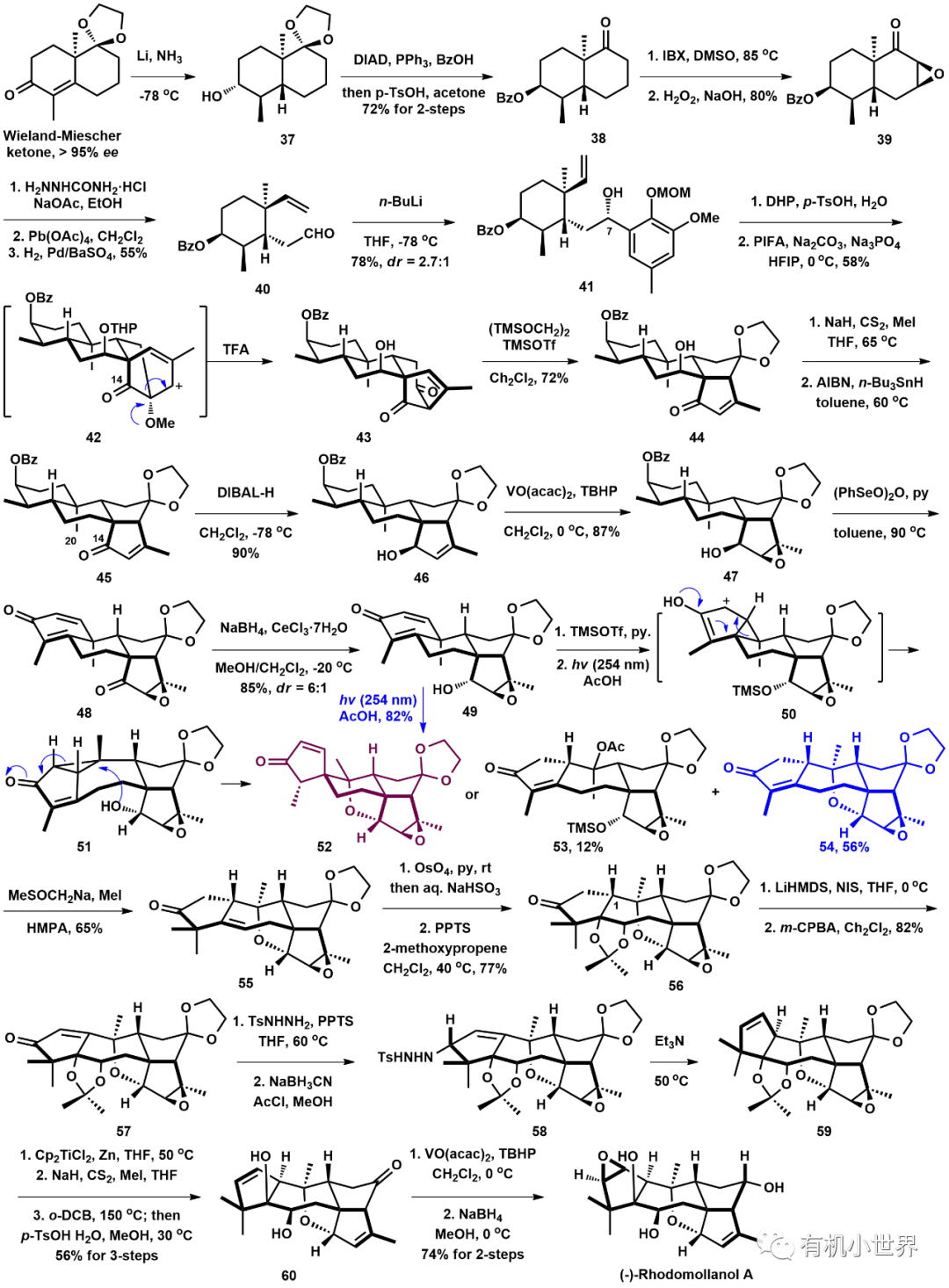
圖7.丁寒鋒課題組合成(-)-Rhodomollanol A的路線
在合成過程中也出現(xiàn)了一些問題,作者通過“曲線救國”的策略進(jìn)行逐一解決:
1.醛40被芳基鋰加成得到二級醇41,dr=2.7:1,雖然C7位羥基最終通過Barton脫氧反應(yīng)去掉,但是羥基的手性中心會影響氧化去芳構(gòu)化分子內(nèi)[5+2]環(huán)加成反應(yīng)的立體化學(xué)(facial-selectivity);經(jīng)過篩選大量條件后,將C7位羥基用DHP保護(hù)也是必須的,C7-OTHP與C14-酮羰基之間的1,3-斥力作用會影響反應(yīng)過渡態(tài);如果C7-羥基不保護(hù),反應(yīng)將經(jīng)歷活潑的鄰亞甲基醌中間體,從而誘發(fā)一系列環(huán)化,轉(zhuǎn)化為其他副產(chǎn)物。詳細(xì)見原文獻(xiàn)。
2.對C14-酮羰基進(jìn)行立體選擇性還原很困難,超過50余種不同的還原條件均無法獲得α-羥基,可能是由于C20-角甲基的存在,使C14-酮羰基的β-面具有較大的空間位阻。因此,作者首先將β-烯丙醇49進(jìn)行誘導(dǎo)環(huán)氧化,得到β-環(huán)氧化合物47,再經(jīng)過氧化后得到環(huán)氧酮48,由于此時(shí)D環(huán)的構(gòu)象發(fā)生了變化,而且可能由于環(huán)氧的導(dǎo)向作用,進(jìn)行1,2-還原時(shí)以dr=6:1的比例得到重排前提化合物49,環(huán)氧結(jié)構(gòu)則在合成后期通過單電子還原去掉。
3.在嘗試Nazarov環(huán)化-重排反應(yīng)時(shí),如果C14位α-羥基不保護(hù),光照條件下只能得到螺環(huán)產(chǎn)物52,說明裸露的羥基進(jìn)攻環(huán)丙烷的速率要快于重排反應(yīng);因此將羥基用TMS保護(hù)后,可以抑制環(huán)丙烷開環(huán)的反應(yīng),同時(shí)在酸性條件下TMS脫除后會緩慢釋放出游離的羥基,發(fā)生后續(xù)所的分子內(nèi)環(huán)醚化串聯(lián)反應(yīng);反應(yīng)后也分離到醋酸進(jìn)攻環(huán)丙烷的產(chǎn)物53。
4.在合成的后期,通過氧化再1,4-還原的方式翻轉(zhuǎn)C1位的立體化學(xué)都失敗了,作者通過將烯酮57轉(zhuǎn)化成腙58,溶劑中加熱進(jìn)行“alkene walk”得到烯烴59;最后再經(jīng)過立體和區(qū)域選擇性的氧化和還原,得到天然產(chǎn)物(-)-Rhodomollanol A。
小結(jié):作者以商業(yè)可得的Wieland-Miescher酮為起始原料,通過30步極具挑戰(zhàn)的反應(yīng)完成了具有重排骨架的復(fù)雜木藜蘆烷二萜(-)-Rhodomollanol A的首次不對稱全合成,合成中的關(guān)鍵步驟包括:ODI-[5+2]環(huán)加成/頻哪醇重排串聯(lián)反應(yīng)、逆-Dieckmann裂解/插烯-Dieckmann環(huán)化串聯(lián)反應(yīng)和“緩釋保護(hù)基”參與的光Nazarov環(huán)化/重排反應(yīng)/分子內(nèi)環(huán)醚化串聯(lián)反應(yīng)。該課題組開發(fā)的ODI-[5+2]環(huán)加成/頻哪醇重排串聯(lián)反應(yīng)在構(gòu)建復(fù)雜天然產(chǎn)物的分子骨架上具有巨大潛力,同時(shí)也為探究(?)-Rhodomollanol A可能的生源合成途徑提供了關(guān)鍵證據(jù)。
文中所述內(nèi)容源于以下文獻(xiàn):
J. Am. Chem.Soc. 2020, 142, 4592-4597. Doi: 10.1021/jacs.0c00308.
Org. Lett. 2017, 19, 3935-3938. Doi: 10.1021/acs.orglett.7b01863.
J. Org. Chem. 1994, 59, 5532–5534. Doi: 10.1021/jo00098a009.
Angew. Chem.Int. Ed. 2019, 58, 8556. Doi: 10.1002/anie.201903349
J. Am. Chem.Soc. 2019, 141, 8088-8092. Doi:10.1021/jacs.9b03751.
J. Am. Chem. Soc. 2017, 139, 6098-6101. Doi: 10.1021/jacs.7b02746.








