推薦一篇發表在Cell上的文章,題目為“SPIDR enables multiplexed mapping of RNA-protein interactions and uncovers a mechanism for selective translational suppression upon cell stress”,通訊作者是來自哥倫比亞大學的Marko Jovanovic,加州理工學院的Mitchell Guttman和密歇根大學的Jailson Brito Querido。他們的研究方向集中于RNA結合蛋白的功能研究和RNA-蛋白互作的動態調控。

RNA結合蛋白(RBP)調節了mRNA生命周期的所有階段,但目前的方法通常一次繪制一種RBP的RNA靶標,為了克服這一限制,本文作者開發了SPIDR(split-and-pool identification of RBP targets),這是一種多重鑒定的split-and-pool策略,可以同時分析數十個RBP的結合位點。
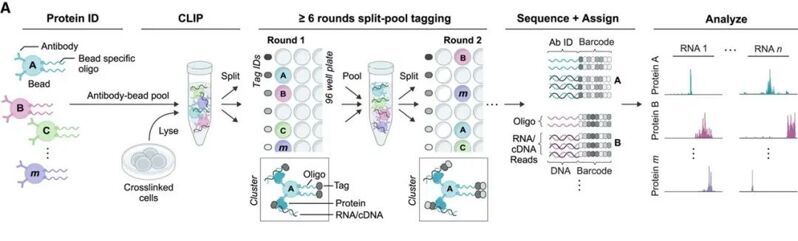
SPIDR的流程包含三個部分:(1)通過將單個beads寡核苷酸偶聯物與特異性抗體偶聯來生成高度多樣化的抗體beads庫(每個蛋白抗體所偶聯的寡核苷酸序列都是特異性的,因此可以通過測序時讀出這一序列從而確定目標蛋白),(2)在UV交聯細胞裂解物中使用這些抗體beads池進行 RBP-RNA復合物的純化,以及(3)使用split-and-pool策略將核苷酸barcode連接到各個蛋白的交聯RNA和beads上的特異寡核苷酸。在測序時,只有對應barcode的序列才可以指數型擴增,從而可以一步讀出beads上偶聯的目標蛋白和其結合的RNA.
利用這一技術,作者成功揭示了LARP1與18S rRNA在40S核糖體mRNA進入通道的精確相互作用,并通過冷凍電鏡(cryo-EM)解析了其結構,分辨率達到2.8 ?。這一發現為LARP1在翻譯抑制中的功能提供了結構基礎。此外,SPIDR還用于研究mTOR信號通路抑制條件下RBPs的動態變化。實驗發現,mTOR抑制劑Torin1處理后,4EBP1優先與翻譯抑制的mRNA 5'非翻譯區(UTR)結合,而LARP1則持續結合TOP motif mRNA和18S rRNA。這些結果表明,LARP1和4EBP1可能協同作用,通過mTOR依賴的機制選擇性抑制特定mRNA的翻譯。
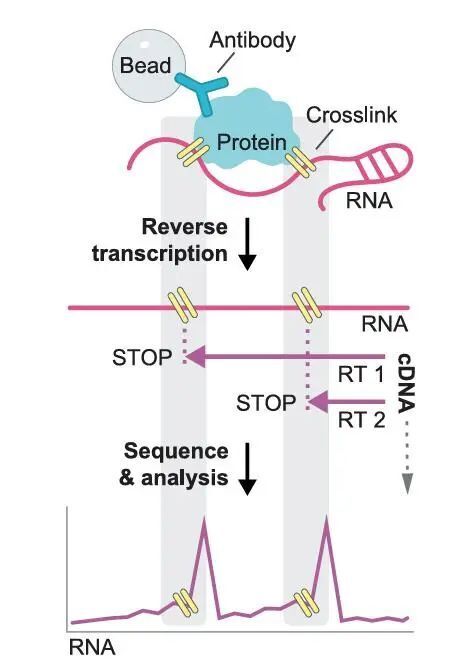
SPIDR的另一個重要應用是單核苷酸分辨率下的RNA-蛋白互作定位。通過分析cDNA截斷位點,SPIDR能夠精確識別RBPs(如HNRNPK、PTBP1和LARP1)的結合位點,并與已知的RNA結合基序高度一致。此外,該方法還鑒定了多個新型核糖體結合蛋白及其在rRNA上的結合位點,例如SLBP與18S rRNA螺旋16區的結合,這可能參與組蛋白mRNA的高效翻譯調控。
SPIDR的高通量特性使其能夠同時分析多種RBPs在RNA生命周期各階段的作用,包括剪接、加工和翻譯等過程。例如,實驗驗證了DROSHA和DGCR8在microRNA前體上的結合模式高度一致,而TARDBP(TDP43)與U6 snRNA和scaRNAs的結合可能為神經退行性疾病的機制研究提供新線索。此外,SPIDR還揭示了超過40%的RBPs通過結合自身mRNA實現表達水平的自我調控。
總之,SPIDR作為一種高效、可擴展的技術,不僅能夠快速生成高質量的RNA-蛋白互作圖譜,還為研究細胞應激、疾病模型和稀有細胞類型中的RNA調控機制提供了強大工具。其應用潛力包括解析RBP在翻譯抑制、剪接調控和RNA代謝中的功能,為RNA生物學和疾病研究開辟了新的研究方向。
本文作者:LYC
責任編輯:MB
DOI:10.1016/j.cell.2025.06.042
原文鏈接:https://doi.org/10.1016/j.cell.2025.06.042








