分享一篇發表在Nature Chemical Biology上的文章,題目為“Site-selective protein editing by backbone extension acyl rearrangements”,通訊作者是來自UC Berkeley的Alanna Schepartz教授和Matthew B. Francis教授,研究方向分別為嘗試利用核糖體生物合成化學聚合物以及利用細胞骨架蛋白進行藥物遞送;來自耶魯大學的Scott J. Miller教授,研究方向為立體化學合成。

常規多肽主鏈骨架以α構型為主,而其他非α主鏈多肽或蛋白例如β、γ、σ等構型能夠增加酶解穩定性和促進細胞通透性等,更適合于某些應用場景。但目前這些非經典多肽或蛋白通常難以在細胞中使用遺傳密碼子拓展技術進行生物合成,僅有少數實例通過核糖體體外翻譯系統實現這類非天然多肽的合成。在此,文章報道了一種基于分子內酰基重排反應的活細胞新型位點特異性蛋白質編輯策略。
作者從天然化學連接技術(NCL)中獲得靈感,當蛋白骨架上反應性較強的親電集團(酯鍵、硫酯鍵)與側鏈親核基團氨基在空間上鄰近時,會發生分子內重排反應。基于此,作者通過正交的氨酰tRNA合成酶——吡咯賴氨酰tRNA合成酶(PylRS)將側鏈含有隱蔽基團的α-羥基酸單體引入翻譯得到的蛋白質中,隨后通過光脫籠或者化學脫籠方法使羥基酸側鏈的親核基團得以暴露,隨后發生熱力學上有利的分子內主鏈延伸酰基重排反應(BEAR),該反應能被用于生成含有β、γ和σ主鏈的多肽和蛋白質。
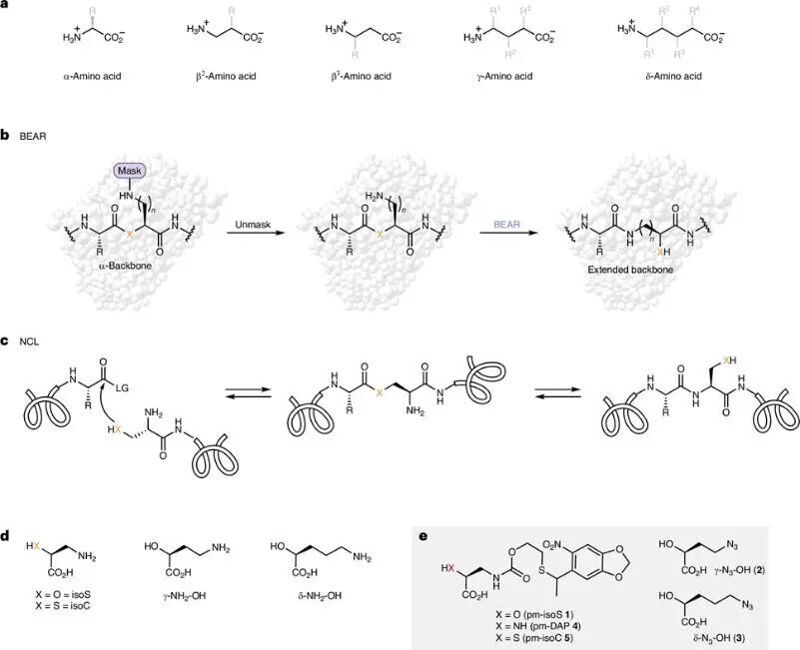
接下來,作者首先基于密度泛函理論評估了這種主鏈上酰基重排反應所需的能量,發現對于幾種不同長度側鏈的酯鍵和硫酯鍵骨架而言,它們反應后的酰胺形式處于的能壘更小更加穩定,即它們在熱力學上有利發生。隨后利用短肽在體外條件下測試了酯鍵和硫酯鍵的反應效率,發現硫酯底物的重排反應受到水解的干擾,而酯鍵則呈現出更好的結果。
隨后,作者將上述策略應用到GFP的活細胞編輯中,首先分別測試了不同種類的大腸桿菌底盤接受摻入非天然氨基酸的能力,并通過質譜等方式確認了摻入疊氮保護羥基酸的蛋白成功表達,且分子量正確。隨后,作者利用不同的化學還原劑進行疊氮掩蔽基團的脫籠處理,通過GluC酶解消化,在質譜上解析包含插入位點的肽段結構,最終優化出在pH為8.2條件下使用PTA作為還原劑能夠得到產率最高的γ-骨架蛋白產物。通過LC共流出和MS2離子比對,作者再次確認了該分子內重排反應成功發生。
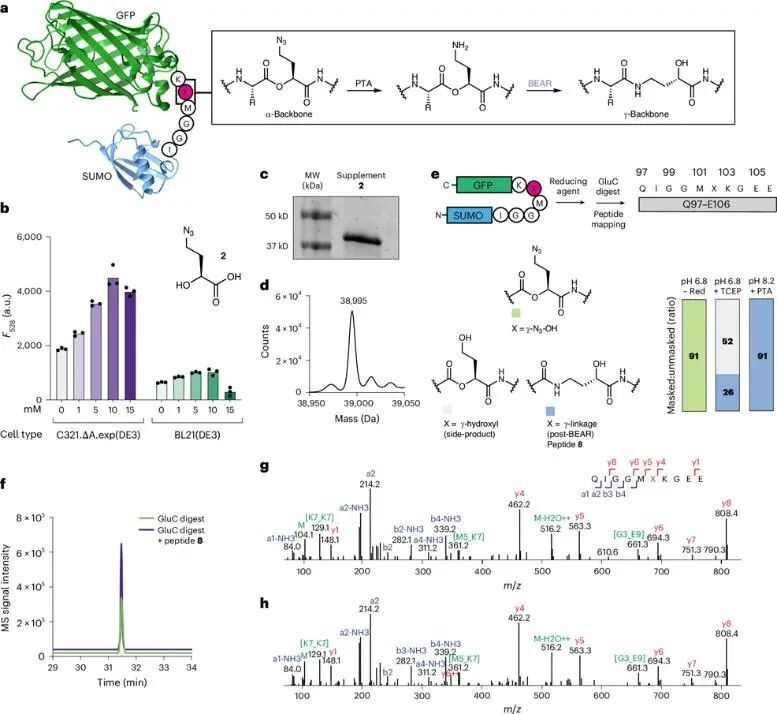
總的來說,本文開發了一種基于非天然氨基酸插入和酰基重排反應的、能夠在活細胞中完成的位點特異性蛋白質編輯技術,用于將蛋白質骨架種類從α主鏈拓展到碳鏈更長的β、γ主鏈等。
本文作者:SHL
責任編輯:WYQ
DOI:10.1038/s41589-025-01999-w
原文鏈接:https://doi.org/10.1038/s41589-025-01999-w








