分享一篇發(fā)表在Advanced Science上的文章,題目為"DeepSecMS Advances DIA-Based Selenoproteome Profiling Through Cys-to-Sec Proxy Training"。通訊作者是中國(guó)科學(xué)院上海有機(jī)化學(xué)研究所的張耀陽(yáng)研究員,課題組專(zhuān)注于蛋白質(zhì)組學(xué)新方法開(kāi)發(fā)。

硒代半胱氨酸(Sec)作為第21種蛋白源氨基酸,在氧化還原酶(如GPX4)中發(fā)揮關(guān)鍵作用,但其在人類(lèi)蛋白質(zhì)組中僅有25種已知硒蛋白。傳統(tǒng)質(zhì)譜方法因Sec的稀有性(僅占蛋白組0.02%)和與半胱氨酸(Cys)的相似性面臨檢測(cè)瓶頸。

本研究創(chuàng)新性地提出"半胱氨酸代理訓(xùn)練"策略:利用Sec與Cys相似的物理化學(xué)性質(zhì),首先使用IodoAPB探針標(biāo)記HEK 293T細(xì)胞中的Cys,構(gòu)建含34,996個(gè)Cys肽段的大型實(shí)驗(yàn)譜庫(kù);隨后在AlphaPeptDeep框架下將這些肽段中的Cys虛擬替換為Sec,生成偽Sec譜庫(kù)訓(xùn)練深度學(xué)習(xí)模型。該模型成功預(yù)測(cè)Sec肽段的三個(gè)關(guān)鍵特征:MS2譜圖(皮爾遜相關(guān)系數(shù)中位數(shù)0.907)、保留時(shí)間(R2=0.989)和離子淌度(R2=0.953),預(yù)測(cè)精度接近生物學(xué)重復(fù)水平。
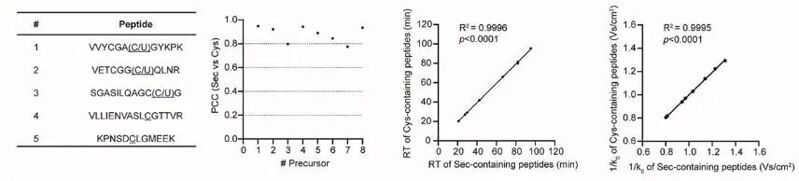
為驗(yàn)證DeepSecMS的實(shí)際效能,作者建立SCoSS數(shù)據(jù)庫(kù)——通過(guò)SECISBP2 RNA結(jié)合能力篩選的986個(gè)高置信度硒蛋白候選集,包含11,551個(gè)前體離子。針對(duì)該庫(kù)的假陽(yáng)性干擾問(wèn)題,創(chuàng)新性地引入Cys肽段作為緩沖肽(比例優(yōu)化至2:1),使HEK 293T細(xì)胞中硒蛋白鑒定數(shù)從15種提升至23種,接近理論最大值。
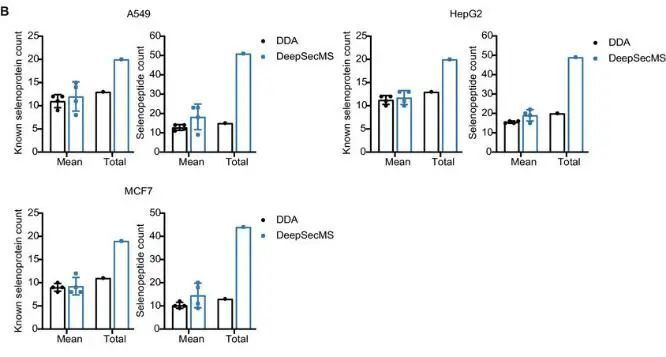
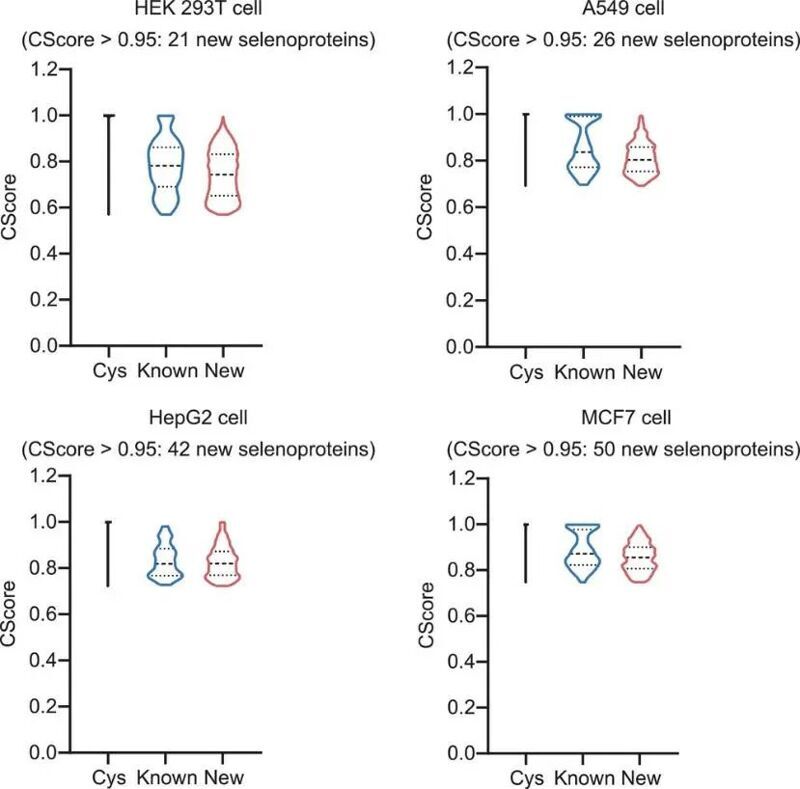
在多種細(xì)胞系(A549、HepG2、MCF7)和10種小鼠組織(腦、肝、心等)的DIA數(shù)據(jù)分析中,DeepSecMS顯著提升已知硒蛋白鑒定深度:如在睪丸組織中鑒定到26種硒蛋白,較傳統(tǒng)DDA方法增加68%;更發(fā)現(xiàn)42個(gè)新型硒蛋白候選,其置信度評(píng)分(Cscore)與已知硒蛋白相當(dāng)。該方法突破硒蛋白研究的三大障礙:稀有性導(dǎo)致數(shù)據(jù)不足、Cys干擾標(biāo)記特異性、數(shù)據(jù)庫(kù)假陽(yáng)性干擾,為GPX4等硒蛋白相關(guān)疾病機(jī)制研究提供新工具。
值得注意的是,這種"常見(jiàn)修飾代理訓(xùn)練"策略具有普適性移植價(jià)值。例如可利用大規(guī)模乙酰化數(shù)據(jù)預(yù)測(cè)其他稀有賴氨酸酰化修飾,為磷酸化、糖基化等稀有翻譯后修飾研究開(kāi)辟新路徑。
本文作者:TZS
責(zé)任編輯:WYQ
DOI:10.1002/advs.202504109
原文鏈接:https://doi.org/10.1002/advs.202504109








