分享一篇發表在Nat Chem Biol上的文章,文章題目為“An unbiased proteomic platform for ATE1-based arginylation profiling”,本文通訊作者為華盛頓大學的Benjamin A. Garcia教授,他們課題組的研究方向是基于定量蛋白質組學和相關計算方法,研究翻譯后修飾在調節疾病發展進程中的作用。

精氨酸化修飾是一種重要的翻譯后修飾,在哺乳動物中,該修飾由精氨酸轉移酶(AET1)催化產生,AET1是哺乳動物中唯一已知的能催化該翻譯后修飾產生的酶。精氨酸化修飾的缺失會導致許多疾病的發生。但是因為精氨酸化修飾與蛋白中正常精氨酸殘基具有相同的質量,因此在質譜上鑒定精氨酸化修飾較為困難。
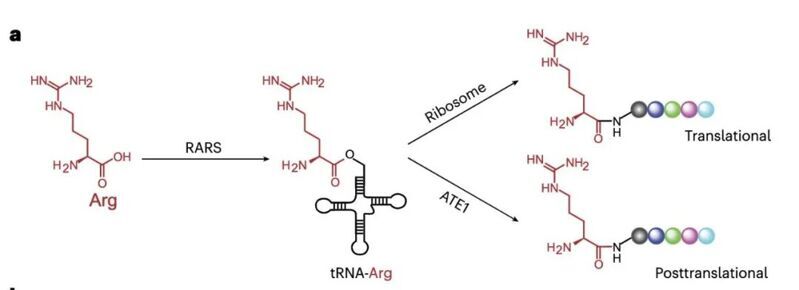
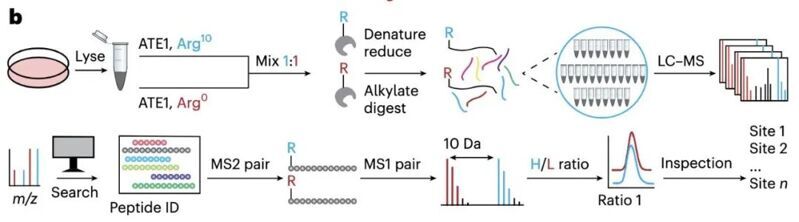
本文作者提出了一種無偏的蛋白質組平臺,可以用于發現ATE1催化產生的精氨酸化修飾,并鑒定該修飾發生的位點。該方法的工作流程是:使用ATE1敲除的細胞,裂解細胞之后,作者添加ATE1酶、Arg0和同位素標記的Arg10(輕重標的Arg比例為1:1),以及產生該修飾所需的的ATP、tRNA、RARS等,在ATE1的催化作用下,其底物蛋白上會產生輕重標比例為1:1的精氨酸化修飾,通過確認該修飾特征,即可區分精氨酸化修飾和精氨酸殘基。
作者先在模式肽上驗證了該催化反應可以在體外構建,并且在模式肽上觀察到了預期中的H/L=1的ratio,之后作者開發了一個用于處理質譜數據的小工具,可以提取具有相同肽序列切Arg上具有10.008269 Da的MS2譜圖,并提取它們對應的MS1,計算它們的H/L,最后導出MS2及其對應的MS1譜圖,用于可視化。
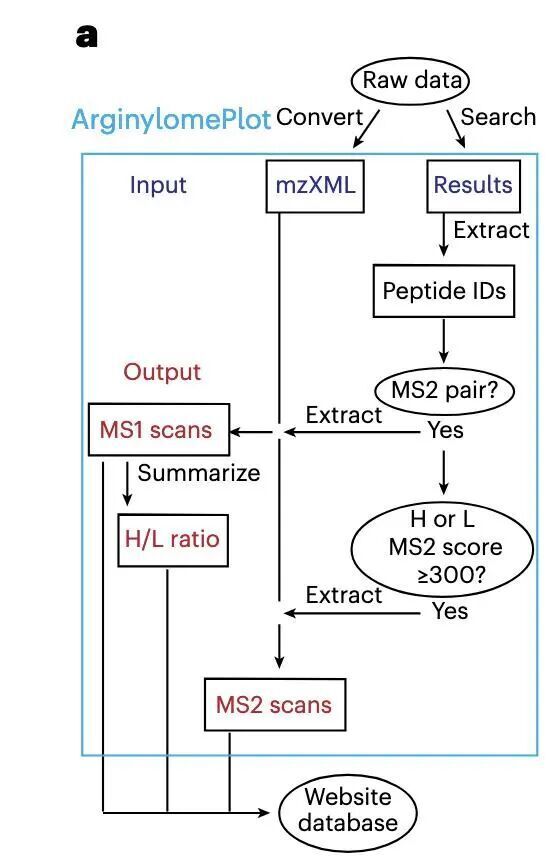
建立了工作流程之后,作者在細胞、病人樣本、小鼠樣本中進行了精氨酸化位點的檢測,并對發現的精氨酸化位點進行了驗證,對蛋白質組數據分析發現,精氨酸化大部分發生在蛋白N端,少部分發生在側鏈上,且精氨酸化修飾大部分發生在D或者E的N端。

綜上所述,作者開發了一個用于蛋白質精氨酸化修飾無偏標記的方法,可以鑒定精氨酸化修飾發生的位點,與肽段中的精氨酸殘基區分。
本文作者:LZ
責任編輯:WYQ
DOI:10.1038/s41589-025-01996-z
原文鏈接:https://doi.org/10.1038/s41589-025-01996-z








