分享一篇發(fā)表在Angew上的文章,標(biāo)題為“Fragment-Based Drug Discovery of Novel High-affinity, Selective, and Anti-inflammatory Inhibitors of the Keap1-Nrf2 Protein-Protein Interaction”,通訊作者為來(lái)自哥本哈根大學(xué)的Anders Bach,主要研究方向?yàn)樗幬镌O(shè)計(jì)與開發(fā)。

Keap1-Nrf2蛋白-蛋白相互作用(protein-protein interaction, PPI)是調(diào)控細(xì)胞抗氧化應(yīng)激和炎癥反應(yīng)的關(guān)鍵通路。抑制該相互作用可激活Nrf2,進(jìn)而促進(jìn)抗氧化基因表達(dá)。傳統(tǒng)共價(jià)激活劑存在脫靶毒性和非特異性的問(wèn)題。因此,作者希望設(shè)計(jì)非共價(jià)小分子抑制劑選擇性地抑制Keap1-Nrf2相互作用。
基于片段的藥物發(fā)現(xiàn)(fragment-based drug discover, FBDD)是一種先篩選化學(xué)復(fù)雜性較低的藥物片段,再根據(jù)片段與靶蛋白結(jié)合的結(jié)構(gòu)數(shù)據(jù)進(jìn)行進(jìn)一步優(yōu)化的藥物發(fā)現(xiàn)策略,適用于靶向PPI的藥物發(fā)現(xiàn)。作者首先利用X射線晶體學(xué)篩選了來(lái)自DSI文庫(kù)的768個(gè)片段,并得到了80個(gè)能與Keap1-Nrf2結(jié)合表面產(chǎn)生相互作用的片段,作者重點(diǎn)關(guān)注了可與Keap1-Nrf2結(jié)合子口袋P3和P5產(chǎn)生相互作用的13個(gè)片段,其中5個(gè)片段在分子對(duì)接中表現(xiàn)出與晶體數(shù)據(jù)類似的結(jié)合模式。通過(guò)對(duì)這5個(gè)片段進(jìn)行合成和SPR測(cè)試,作者選擇了其中結(jié)合最強(qiáng)的片段1作為起點(diǎn)進(jìn)行進(jìn)一步優(yōu)化。

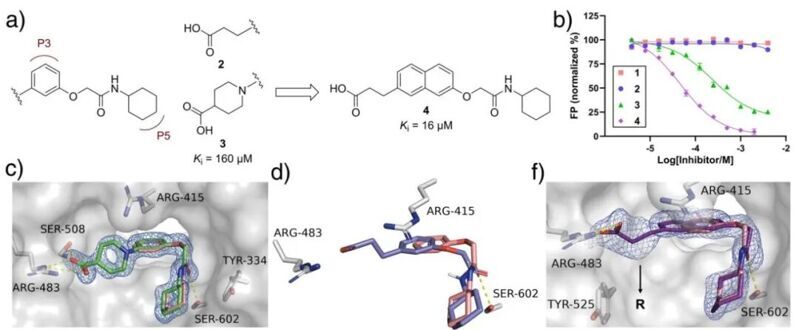
作者首先在片段1中引入2種酸性脂肪鏈與Arg483形成鹽橋,得到對(duì)PPI具有抑制效果的化合物3,Ki值為160 μM,化合物2 無(wú)抑制效果。進(jìn)一步在化合物2中引入萘環(huán)延長(zhǎng)連接鏈并保留核心結(jié)合模式,得到化合物4,Ki值為16 μM。
隨后,作者在酸連接子中引入芳香族取代基,使其與Tyr525的側(cè)鏈發(fā)生額外的π-π堆疊相互作用,以及添加甲氧基引入氫鍵受體,得到了納摩爾級(jí)別的抑制劑化合物13,Ki值為32 nM。最后,通過(guò)合成并測(cè)試36個(gè)類似物,得到了抑制性最強(qiáng)的化合物44,Ki值為3.9 nM,并通過(guò)X射線衍射證明了結(jié)合模式與之前一致。
接下來(lái),作者用熱位移實(shí)驗(yàn)證明了包括化合物44在內(nèi)的幾種候選抑制劑對(duì)KEAP1的高度選擇性。并證明了這些抑制劑能在在HaCaT和BEAS-2B細(xì)胞中顯著激活Nrf2的下游基因,發(fā)現(xiàn)化合物24和28是最有效的。除此之外,作者篩選的抑制劑還能在THP-1巨噬細(xì)胞中抑制NLRP3炎癥小體活化、IL-1β釋放和STING信號(hào)通路。
最后,作者對(duì)化合物24和28對(duì)轉(zhuǎn)錄組造成的影響進(jìn)行了分析,發(fā)現(xiàn)與共價(jià)Nrf2激活劑相比, 24和28同樣能夠激活Nrf2控制基因和關(guān)鍵的免疫信號(hào)通路,且非Nrf2的脫靶效應(yīng)更少。
總之,作者通過(guò)基于結(jié)構(gòu)片段的藥物設(shè)計(jì)策略開發(fā)了有效的選擇性非共價(jià)Keap1-Nrf2抑制劑,能激活Nrf2控制基因,通過(guò)NLRP3和STING通路抑制炎癥,且脫靶效應(yīng)更少,特異性更強(qiáng)。
本文作者:ZCL
責(zé)任編輯:LZ
DOI:10.1002/anie.202508121
原文鏈接:https://doi.org/10.1002/anie.202508121








