分享一篇發(fā)表在Nature Chemistry上的文章,題目為“Photocatalytic labelling-enabled subcellular-resolved RNA profiling and synchronous multi-omics investigation”,通訊作者是來自北京大學的樊新元、劉君和陳鵬三位老師,研究方向為光催化鄰近標記和RNA修飾的調控機制。

解讀亞細胞轉錄組的時空變化能夠幫助我們更好地理解疾病進程。已有多種傳統(tǒng)研究轉錄組的方法,例如密度梯度離心后裂解提取RNA會損失原位信息,而酶法介導的鄰近標記方法則需要對細胞進行轉染處理,限制了其應用場景。此前研究人員報道了一種蛋白質反應性warhead亞甲基醌,并將其應用于光催化的蛋白質標記。在本文中,作者則通過調整這一反應彈頭的化學活性,實現了RNA特異性亞細胞分辨率的光催化標記。
首先,作者測試了一系列亞甲基醌結構的化合物衍生物的反應活性,探針結構包括紫外激活的保護基團和用于富集的生物素標簽,在體外實驗證明了對于RNA模板具有一定的反應活性并且在單核苷酸的水平上測試了主要的標記靶標為胞嘧啶。將反應warhead更改為適用于銥催化劑和藍光激活的系統(tǒng)中,同樣能夠對RNA進行標記,并且發(fā)現這一標記嚴格依賴于體系中每個組分并有較強的正相關關系。
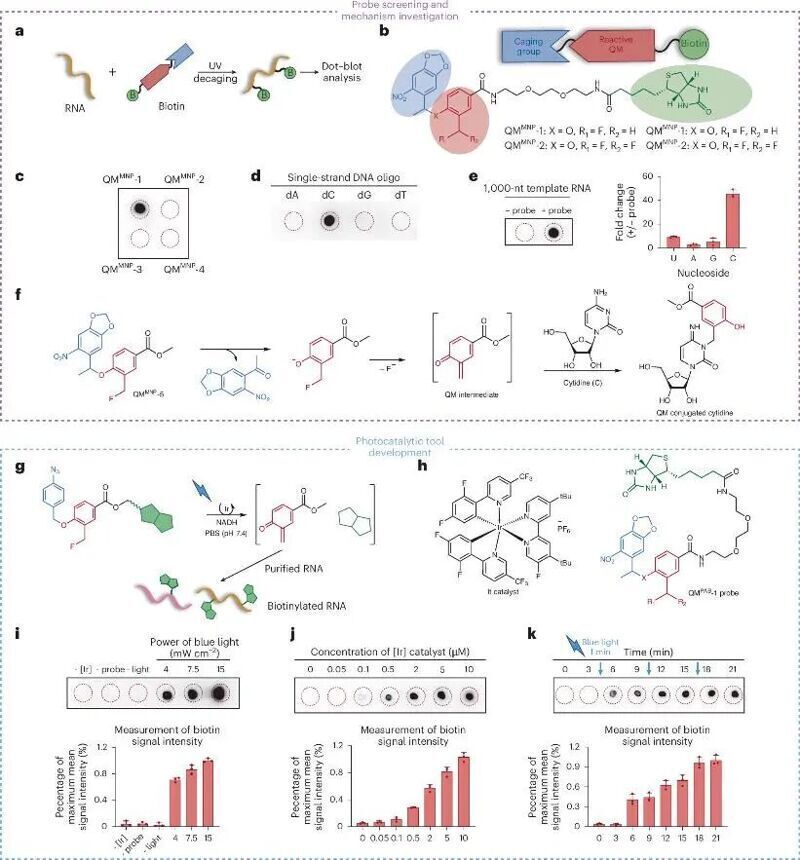
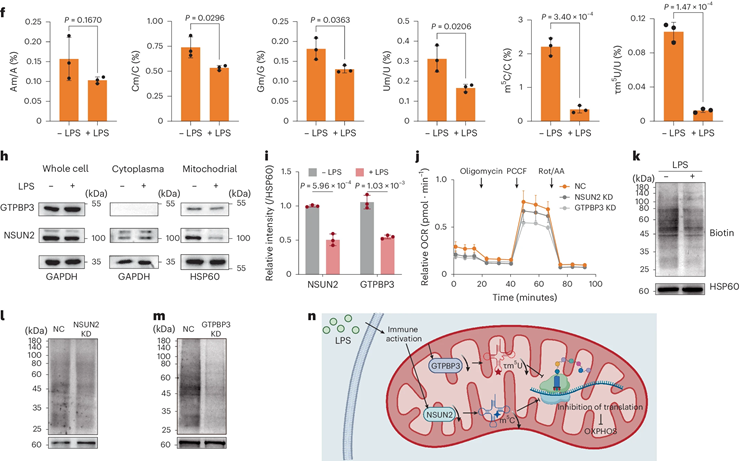
隨后,作者通過向探針上裝載三苯基膦基團,實現了優(yōu)異的線粒體靶向性。該探針能夠多次重復、高置信地鑒定到多種線粒體mRNA,并且能夠富集到許多tRNA,實現了無偏富集的同時分析線粒體RNA中的胞苷比例。他們將這一體系應用到LPS處理的Raw264.7巨噬細胞上,比較了線粒體轉錄組在細胞極化過程中的動態(tài)變化。作者發(fā)現RNA的豐度并無并無顯著變化,因此將目光轉向了調控RNA活性的幾種修飾上。最終發(fā)現在極化細胞中,小于200堿基長度的小RNA群體上的τm5U和m5C兩種修飾豐度明顯下降。作者使用此前對蛋白質光催化標記的技術解析了蛋白組的動態(tài)變化,發(fā)現了上述兩種tRNA修飾的writer蛋白豐度降低,結合LPS處理細胞中線粒體內新生蛋白大量減少,提出了受到LPS刺激后,線粒體中兩種tRNA修飾寫入蛋白豐度降低導致tRNA豐度減少,穩(wěn)定性降低進而降低線粒體翻譯效率的機制。
除此之外,出于光催化蛋白標記和RNA標記不同warhead之間不同的化學反應性,此方法為在同一體系中同時分析蛋白組和轉錄組提供了可能。實驗結果表明,QM-1探針主要標記RNA,而QM-4探針主要標記蛋白質。作者利用這種正交的同步標記系統(tǒng),解析了原代T細胞從初始T細胞向細胞毒性T細胞轉變過程中轉錄組和蛋白組的動態(tài)變化,最大限度減少了樣品異質性帶來的影響。
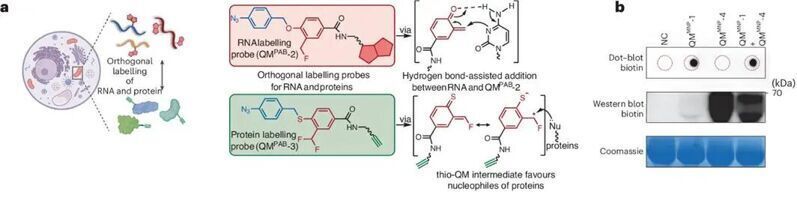
總的來說,本文開發(fā)出一種針對RNA特異性的光催化標記探針,能夠實現多種不同樣品中亞細胞分辨率的轉錄組的無偏分析,并且能夠實現與蛋白組正交的多組學分析。
本文作者:SHL
責任編輯:WYQ
DOI:10.1038/s41557-025-01946-1
原文鏈接:https://doi.org/10.1038/s41557-025-01946-1








