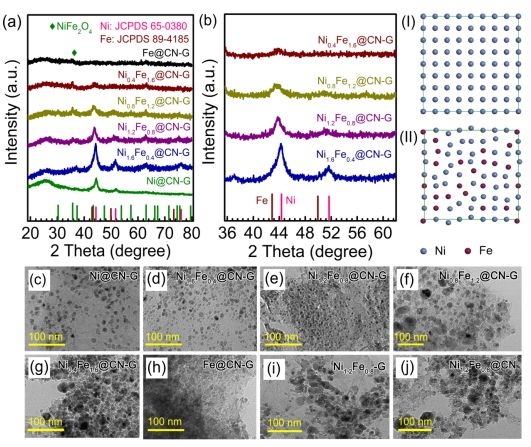
論文DOI:10.1016/j.apcatb.2020.118612為了通過非貴金屬催化反應更加清潔高效地得到可用于燃料電池的氫氣,設計了一系列負載在還原氧化石墨烯上氮摻雜碳包覆 NiFe 合金納米顆粒。Fe 在 Ni 中的摻雜有效地調控晶格應力并優化電子結構。Ni1.2Fe0.8 合金納米顆粒在室溫下催化儲氫材料 NH3BH3 水解產氫的轉化頻率(TOF)值可達 86 min–1(基于金屬分散度計算)。接近貴金屬材料的高催化活性起源于合金中金屬 Ni 與 Fe 協同作用。本文展現了通過催化活性中心工程實現使用非貴金屬替代貴金屬催化材料的前景。A. 氫作為一種可持續的清潔能源載體,是新一代社會生活中的替代燃料之一。但是,氫的儲存和運輸是氫能技術發展的關鍵問題。在各種新型儲氫材料中,氨硼烷(NH3BH3)具有高氫含量、無毒性、在空氣和水溶液高的穩定性等優點,有望作為一種有應用潛力的儲氫材料。現今性能最好的催化劑都是基于貴金屬材料制備的。高成本、資源稀缺的突出缺點,阻礙了其商業應用。因此,合成廉價、高效且穩定的催化劑是推進硼氫化物制氫所需要解決的問題。Ni、Fe 在地殼中的儲量遠遠高于貴金屬、Co 等元素,是催化劑設計的良好選項。然而,其明顯低于貴金屬的催化活性亟待通過新的催化劑活性中心設計和調控策略得到提升。B. 根據 d 電子催化理論,過渡金屬的d電子軌道性質是影響催化活性中心活性的關鍵因素之一,在化學反應中未配對d電子與反應物分子的 s 電子或 d 電子相互作用。在這種情況下,是否可以通過與其他金屬元素形成合金來顯著改變過渡金屬元素的電子結構和提升其催化活性是一個有待探索回答的問題。由于雙氫氧化物(LDHs)中金屬物種的廣譜可調變性,將具有相似離子半徑的 Ni2+ 和 Fe3+ 的過渡金屬離子引入到 LDHs 層中,為我們在原子尺度上調節和設計表面催化劑活性中心的結構從而對催化 NH3BH3 水解活性的調控提供了一種有效途徑。本文考察了 Ni/Fe 摩爾比對催化劑本征活性的影響。有趣的是,當加入不同含量的 Fe 時對 Ni 本征催化活性的影響并不相同,精心調控尋找到具有最高本征活性的最佳 Ni/Fe 比例,結合實驗和理論模擬,建議了催化活性中心結構。結果發現,加入一定含量的 Fe 也明顯優化了 Ni 的晶格應變和 d 電子結構并且能有效提高Ni的催化活性,成功的在原子尺寸上實現了對活性中心的調控。另一方面,在合成過程中加入載體(氧化還原石墨烯),并且加入多巴胺形成碳包覆納米顆粒的結構對于提高催化活性中心的利用率和穩定性也具有重要的影響。采用簡便的兩步合成方法制備 NiFe 合金納米顆粒。首先通過多巴胺在堿性下的自聚合過程和反應物的水熱反應合成出前驅體 Ni2-xFex-LDH@PDA-GO(x:Fe 物質的量,NiFe 總物質的量為 2 mmol)。在這一過程中,通過尿素水解,在載體上沉積了 Ni2+ 和 Fe3+。然后前驅體在惰性氣氛下煅燒形成 NiFe 合金納米顆粒(Ni2-xFex@CN-G)。通過 XRD 分析(Fig. 1a,b)發現隨著 Fe 含量的增加,部分衍射峰向較低的 2θ 角移動,表明 Fe 被成功摻雜在 Ni 晶格結構中。此外,這種轉變趨勢是由于與 Ni 相比,Fe 的半徑較大,在 Fe 摻雜后,Fe 取代了 Ni 的位置,從而改變 Ni 的晶胞參數。采用 TEM 觀察了 Fe 含量對合成的 Ni2-xFex@CN-G 材料形貌的影響。結果表明最佳 Fe 含量催化劑(加入 Fe 的物質的量為 0.8 mmol 時)顆粒尺寸較小并且對比材料表明氧化還原石墨烯與氮摻雜碳包覆的結合促進小顆粒 NiFe 合金的形成。▲Fig. 1. (a) XRD patterns of Ni2-xFex@CN-G, (b) partial enlarged XRD patterns of Ni2-xFex@CN-G ((I), (II) the crystal structure of Ni and Ni2-xFex@CN-G), (c-h) TEM images of Ni2-xFex@CN-G, (i) TEM image of Ni1.2Fe0.8-G, (j) TEM image of Ni1.2Fe0.8@CN.
接下來,通過 HRTEM 證明了 Ni 和 Fe 不是以單原子分散的形式分散在石墨烯載體上,并且通過晶格間距表明鎳鐵合金間距在金屬 Ni (0.204 nm)和金屬鐵 Fe (0.210 nm)的(111)晶面之間,確認 NiFe 合金的形成(Fig. 2)。▲Fig. 2. (a) TEM images (inset: the corresponding particle size distribution curve) and (b) HRTEM images of Ni1.2Fe0.8@CN-G, (c) TEM images of Ni1.2Fe0.8@CN-G at higher magnification, (d) EDX elemental mappings of Ni1.2Fe0.8@CN-G.
通過譜學表征手段(Raman、XPS, Fig. 3),進一步確定了催化劑中碳的石墨化程度和表面化學成分與電子狀態。對 XPS 譜圖進行分析,我們發現相對于 Ni@CN-G、Fe@CN-G,Ni1.2Fe0.8@CN-G 中 Ni 2p 峰和 Fe 2p 峰的位置發生了偏移,表明由于Ni和Fe的合金化,使得 Ni 和 Fe 的電子結構發生變化,進一步確定了合金結構的形成。▲Fig. 3. (a) Raman spectra, (b) XPS spectra of the survey spectra of Ni1.2Fe0.8@CN-G, (c) Ni 2p, (d) Fe 2p high-resolution spectra of Ni1.2Fe0.8@CN-G, Ni@CN-G, and Fe@CN-G (e) N 1s, (f) C 1s of Ni1.2Fe0.8@CN-G.
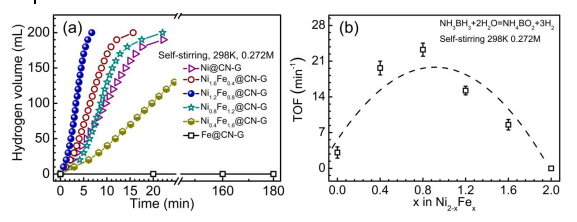
進一步探究了在加入不同 Fe 含量情況下的 Ni 納米顆粒在催化 NH3BH3 水解活性差異。只加入 Fe 時,Fe@CN-G 催化劑沒有表現出任何活性。這表明Ni原子是反應的催化活性中心,加入 Fe 后,Fe 作為助催化劑提高催化劑的活性。所得結果表明 Ni/Fe 比例對 NiFe 合金催化活性有明顯關聯。在所制備的 NiFe 合金催化劑中, Ni1.2Fe0.8@CN-G 的本征催化活性最高,可媲美部分貴金屬催化材料。使用其他金屬代替 Ni、Fe 中的一種得到合金結構,無法實現顯著的催化活性提升,排除了單原子催化效應(Fig. 4)。▲Fig. 4. Hydrogen evolution for NH3BH3 hydrolysis (a) plot of volume of hydrogen evolution catalyzed by Ni2-xFex@CN-G at 298 K with NaOH 1 M and (b) corresponding TOF value for NH3BH3 hydrolysis.
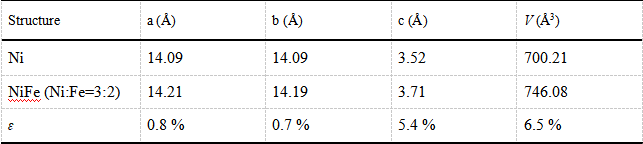
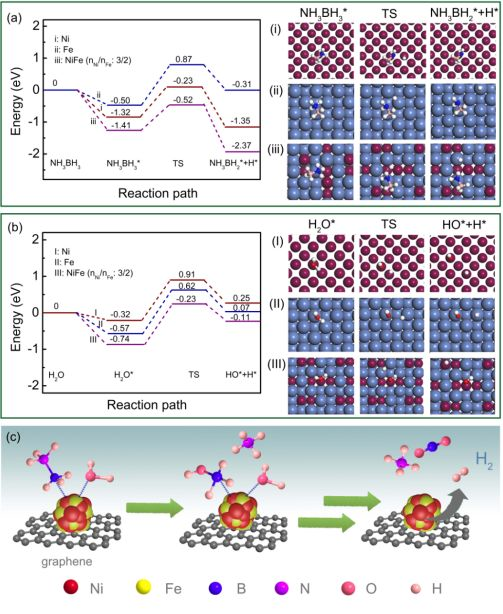
A. 利用密度泛函理論(DFT)計算研究了加入Fe后形成NiFe合金的應力變化。在 NiFe 合金體系中,應力對原子尺度的影響導致晶格參數和Ni 與 Fe 原子間距離的變化。在 DFT 計算中,以 Ni@CN-G 和 Ni1.2Fe0.8@CN-G 為對象。結果表明,晶格參數、晶胞結構和體積改變,NiFe 合金相對于Ni應力改變量為 6.5 %。B. 通過 DFT 計算,探究了 Ni@CN-G、Fe@CN-G 和Ni1.2Fe0.8@CN-G 催化劑上反應的催化活性中心結構(Fig. 5)。Fe 的加入對提高 Ni 對 NH3BH3 水解產氫的催化活性是有效的。分別計算了 NH3BH3 和水分子在三種催化劑表面的吸附和解離過程。NH3BH3 分子的反應勢壘順序為:Ni1.2Fe0.8<Ni<Fe;H2O 分子的反應勢壘順序為:Ni1.2Fe0.8<Fe<Ni。計算結果表明,Fe 的加入改變了Ni的電子結構,促進了催化劑對反應物分子的吸附解離,特別是水分子的吸附和解離。與 Ni@CN-G 和 Fe@CN-G 催化劑相比,NiFe 催化劑降低了反應總的勢壘,使 Ni1.2Fe0.8@CN-G 具有優異催化性能。在 NiFe 體系中,Ni 中心對 NH3BH3 的解離反應略強于Fe,而 Fe 中心對水的解離反應略強于 Ni,表明 Ni 和 Fe 在催化過程中通過協同作用提高了催化活性中心本征活性。基于上述討論,提出了 Ni2-xFex@CN-G對NH3BH3 水解的可能雙元素協同催化反應機理(Fig. 5c)。▲Fig. 5. (a) Energy profiles of NH3BH3 and (b) water dissociated on Ni (111), Fe (111), NiFe (111) (nNi/nFe=3/2) surface. (i-iii) and (I-III) are the optimized 3D models. Ni, Fe, B, N, O and H are represented as purple, blue, pink, royal, red and white sphere, respectively. Configuration diagrams of reactants, transition states (TS), and products correspond to the structures. (c) A proposed reaction mechanism for hydrolysis of NH3BH3 on Ni2-xFex@CN-G.
通過合金化在原子尺寸上調控Ni的d電子結構,從而實現 Ni 對NH3BH3 水解產氫的催化活性大幅提升。實驗表征驗證了 Fe 成功地摻雜到 Ni 晶格中,從而調節Ni的晶格和電子結構。與 Ni、Fe 單金屬催化劑相比,NiFe 合金催化劑的本征活性有了很大提高。得到的 Ni1.2Fe0.8@CN-G 催化劑在 298 K 下對 NH3BH3 水解產氫的催化活性顯著提升,TOF 值為 86 min-1。探討了不同 Fe 含量對催化活性提升的作用機理,催化活性的提升主要是由于 Ni 和 Fe 之間的協同作用,加速了催化反應過程中的分子解離步驟。在合成過程中添加高表面積載體被證明是提高催化活性中心利用率和穩定性的關鍵因素。本工作為獲得經濟實用、可媲美貴金屬的高效制氫非貴金屬催化劑提供了一種具有吸引力的方法,也為通過組合不同元素實現催化活性中心結構和性能調控提供新的思路。