▲第一作者:朱用洋 ;通訊作者:歐陽柳章、邵懷宇、黃振國論文DOI:http://dx.doi.org/10.1002/anie.201915988 硼氫化鈉(NaBH4)是最受廣泛研究的儲/制氫材料之一,其水解副產(chǎn)物的再生是限制其規(guī)模化應用的主要障礙。在本工作中,利用水解產(chǎn)物(NaBO2)水溶液自發(fā)吸收空氣中CO2形成的Na2B4O7?10H2O和Na2CO3為原料,在常溫常壓下與Mg粉進行球磨,獲得了約80%的再生產(chǎn)率,實現(xiàn)了NaBH4水解與再生的閉合循環(huán)。與以往研究相比,該新方法避免了昂貴還原劑(如MgH2等氫化物)、高壓氫氣的使用和Na2B4O7?10H2O高溫脫水的耗能與繁瑣工藝過程。因此,該方法大大降低了NaBH4再生成本,有望廣泛應用于氫能領域。氫能的規(guī)模應用包括氫的制備、存儲和應用三大關鍵技術,而氫的存儲與運輸是目前氫能規(guī)模應用的瓶頸。NaBH4水解制氫,具有高理論儲/制氫密度、低放氫溫度、反應過程可控、氫氣純度高和環(huán)境友好等優(yōu)點,被認為是最接近實用化的制氫方法。但是由于NaBH4價格高昂,而且NaBH4水解反應并不可逆及再生困難等缺點,美國能源部給予“NaBH4水解制氫在車載上不推薦應用”的建議。因此,而NaBH4的簡易、高效及廉價的合成與再生是實現(xiàn)向?qū)嵱没年P鍵,需要開創(chuàng)制/儲氫一體化新技術。從企業(yè)生產(chǎn)和獻報導資料來看,NaBH4制備/再生通常采用無水偏硼酸鈉(NaBO2)或無水硼砂(Na2B4O7)與MgH2/Na/Mg等還原劑,通過高溫高壓 (如550℃、7MPaH2)實現(xiàn)NaBH4再生與合成;要么高能球磨NaBO2或Na2B4O7與昂貴的MgH2/CaH2來實現(xiàn)再生過程。這些方法都無一例外的采用了無水NaBO2和Na2B4O7,這些原材料的獲得均需要對NaBO2?xH2O和Na2B4O7?10H2O分別在350℃和600℃進行高溫脫水處理;而且制備過程中均需要額外引入H2(H0)或昂貴的金屬氫化物(H-)作為氫源。而H2需要單獨制備過程,且目前95% H2來自于化石燃料重整制備,不可持續(xù);金屬氫化物需要金屬與H2在高溫下進一步合成,成本高。本工作是朱敏課題組NaBO2?xH2O(x=2,4)再生NaBH4前期工作的延伸,是NaBH4再生的新思考與新方法。前期工作發(fā)現(xiàn),NaBH4真正水解產(chǎn)物是水合偏硼酸鈉(NaBO2?xH2O),創(chuàng)新性的將結晶水中的正氫(H+)在還原劑的作用下直接轉變?yōu)镹aBH4中負氫(H-),從而發(fā)展了氫氣的制/儲一體化技術并闡明了再生的機理(Adv. Energy Mater.,2017,7,1700299)。因此,本文提出以NaBO2水溶液吸收空氣中CO2轉變的Na2B4O7?10H2O為原材料,將其結晶水中的H+作為氫源合成NaBH4中的H-,實現(xiàn)了氫的制儲用閉環(huán)并避免了氫的氣態(tài)運輸與高壓存儲,且再生過程無需外加氫源,解決了合成NaBH4的高能耗和高成本問題。無論是NaBH4水解制氫還是通過直接硼氫化物燃料電池(DBFCs)負極氧化供電,最終均可得到NaBO2水溶液,其易吸收空氣中CO2轉變?yōu)镹a2B4O7?10H2O與Na2CO3。Na2B4O7?10H2O與Na2CO3混合固體在低于54℃下低溫干燥即可獲得,實現(xiàn)了CO2固化。朱敏課題組前期開展將儲氫材料與CO2甲烷化結合起來,利用其儲氫特性,吸收廢氫并將其與CO2反應,同時反應過程中既作為氫源也作為催化劑(Int. J. Hydrogen Energy., 2019, 44(55): 29068-29074)。研究發(fā)現(xiàn),CO2甲烷化過程中,其先轉變?yōu)樘妓猁},隨后再生成甲烷。本工作同樣將其中的Na2CO3為原材料,在實現(xiàn)NaBH4再生的同時實現(xiàn)CO2甲烷化。二氧化碳甲烷化反應是放熱,熱力學有利,但其動力學受限于催化劑,催化溫度通常在250-600℃之間,且常出現(xiàn)積碳現(xiàn)象而導致催化劑失活。該工作在室溫下簡單球磨Na2B4O7?10H2O與Na2CO3,在再生NaBH4過程中可同時實現(xiàn)CO2的還原。盡管本文中CO2甲烷化部分并沒有突出介紹,但在文中反應方程式表明了該方法在室溫下實現(xiàn)NaBH4再生的同時也實現(xiàn)了CO2甲烷化。為實現(xiàn)NaBH4水解制氫的規(guī)模化應用,降低采用天然硼砂礦(Na2B4O7?10H2O)合成NaBH4成本并克服現(xiàn)有工藝復雜的問題。本工作采用NaBH4水解溶液經(jīng)CO2自然處理的混合物(Na2B4O7?10H2O與Na2CO3)與廉價Mg單質(zhì)進行室溫球磨再生NaBH4,Na2B4O7?10H2O與Na2CO3混合物中Na:B的原子比恰為目標產(chǎn)物NaBH4的原子比(1:1),H恰為生成NaBH4和CH4所需量,實現(xiàn)了Na2B4O7?10H2O中H+存儲在NaBH4中H-的氫制儲閉合循環(huán)。該方法還拓展了采用天然硼砂礦加廉價的Na2CO3合成NaBH4新技術,值得一提的是NaBH4再生過程中可同時實現(xiàn)了CO2的還原。該工藝與傳統(tǒng)工藝相比,還去除了Na2B4O7?10H2O高溫(600℃)脫水過程,Na2CO3不僅無需分離還可充當補鈉劑,提高Na2B4O7?10H2O利用率。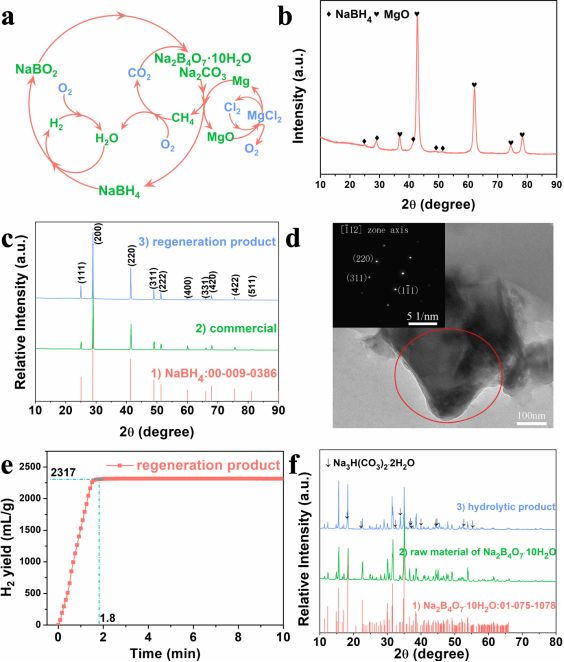 ▲Figure 1. (a) A closed system of NaBH4 hydrolysis and regeneration; (b) XRD pattern of products obtained via ball milling a mixture of Mg, Na2B4O7·10H2O, and Na2CO3 in 24.75:1:1 molar ratio for 20 h at 1000 CPM; (c) XRD patterns of standard PDF card of NaBH4, commercial and synthesized NaBH4; (d) TEM image and SAED pattern of synthesized NaBH4; (e) Hydrolysis curve of the regenerated NaBH4 in an aqueous solution loaded with 2 wt% CoCl2; (f) XRD patterns of standard PDF card of Na2B4O7·10H2O, raw Na2B4O7·10H2O, and compounds obtained after hydrolytic aqueous solution naturally dried up in air.
▲Figure 1. (a) A closed system of NaBH4 hydrolysis and regeneration; (b) XRD pattern of products obtained via ball milling a mixture of Mg, Na2B4O7·10H2O, and Na2CO3 in 24.75:1:1 molar ratio for 20 h at 1000 CPM; (c) XRD patterns of standard PDF card of NaBH4, commercial and synthesized NaBH4; (d) TEM image and SAED pattern of synthesized NaBH4; (e) Hydrolysis curve of the regenerated NaBH4 in an aqueous solution loaded with 2 wt% CoCl2; (f) XRD patterns of standard PDF card of Na2B4O7·10H2O, raw Na2B4O7·10H2O, and compounds obtained after hydrolytic aqueous solution naturally dried up in air.
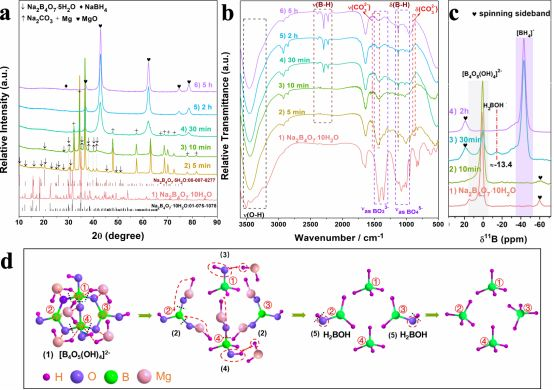
本工作開發(fā)了一種簡單低成本的NaBH4再生與合成新方法,如圖1a所示,實現(xiàn)了NaBH4的氫制儲閉合循環(huán)。Mg與 Na2B4O7·10H2O和Na2CO3混合物室溫球磨后,獲得與商業(yè)購買NaBH4一樣的晶體學特征、微觀結構及純度。再生過程實現(xiàn)了CO2還原為CH4。制備的NaBH4水解性能優(yōu)異,空氣中的CO2對水解產(chǎn)物的自然處理經(jīng)低溫干燥獲得Na2B4O7·10H2O和Na2CO3混合物。該循環(huán)中的Mg通過商業(yè)方法再生,即MgO轉化為MgCl2,通過電解MgCl2獲得Mg。根據(jù)XRD、FTIR、MS結果(文章里有介紹,這里不多做贅述),再生反應的步驟如下:Na2B4O7·10H2O → Na2B4O7·5H2O + 5H2O (1)2H2O + Mg → Mg(OH)2 +H2 (2)Mg + Mg(OH)2 → 2MgO + H2 (3)Na2B4O7·5H2O + Na2CO3 + 15MgH2 → 4NaBH4 + 15MgO + CH4 + 10H2 (5)總反應:Na2B4O7·10H2O + Na2CO3 + 20Mg → 4NaBH4 + 20MgO + CH4 (6)根據(jù)化學結構,Na2B4O7·5H2O和Na2B4O7·10H2O的實際分子式分別為Na2B4O5(OH)4·3H2O和Na2B4O5(OH)4·8H2O。為了進一步闡明反應機理,對球磨產(chǎn)物進行半原位固態(tài)核磁測試,首次觀察到中間產(chǎn)物H2BOH。因此,[B4O5(OH)4]2-的反應轉變,如圖2d所示。[B4O5(OH)4]2-結構單元包含兩個BO4四面體(sp3雜化)和兩個BO3平面三角形(sp2雜化),如圖2d(1)所示。BO3平面三角形中B-O鍵(平均鍵長1.3683 ?)比BO4四面體B-O鍵(1.4418 ?)強,因此BO4四面體B-O鍵優(yōu)先斷裂,B與中間產(chǎn)物MgH2中的H成鍵,O與Mg成鍵。可以合理地假設形成了三種含B化合物中間體(圖2d(2-4))。熱力學上,Mg更可能與氧結合形成更穩(wěn)定的化合物MgO(ΔGfo of MgO: -569.3 kJ/mol oxygen; ΔGfo of B2O3: -398.1 kJ/mol oxygen)。因此,在B-O-Mg-H中間體中的B-O和Mg-H斷裂形成MgO和B-H(圖2d(2,4))。在圖2d(5)中(B)-O-H(O與B是以sp2雜化鍵合)的斷裂導致中間“H2BOH”的形成,這在核磁共振譜中檢測到(圖2c(3))。據(jù)文獻報道,“H2BOH”中的B是Lewis酸的,可以接受MgH2中的Hˉ。因此,“BH4ˉ”和MgO生成。此外,與B是以sp3雜化結合的“OHˉ”(圖2d(3,4))被MgH2中被Hˉ所取代,形成“BH4ˉ”,這與課題組的前期研究一致。▲Figure 2. (a) XRD patterns and (b) FTIR spectra of commercial Na2B4O7·10H2O and products obtained after ball milling Mg, Na2B4O7·10H2O, and Na2CO3 mixtures (in 18:1:1 molar ratio) at 1200 CPM for different durations; (c) Solid-state 11B NMR spectra of commercial Na2B4O7·10H2O and products obtained after ball milling for different durations; (d) Proposed reaction mechanism between Mg, Na2CO3, and Na2B4O7·10H2O to form NaBH4.
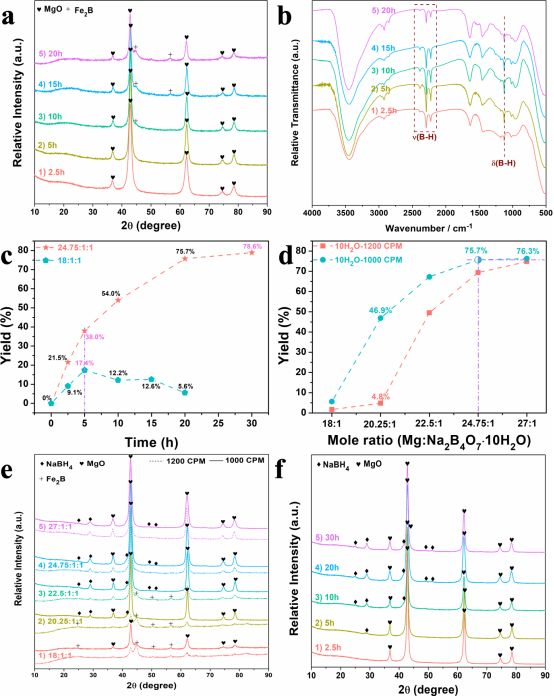
通過優(yōu)化高能球磨再生NaBH4工藝,最高產(chǎn)率為78.9%,高于課題組前期報道的NaBO2·2H2O-Mg體系的產(chǎn)率(68.6%)。產(chǎn)率提高主要原因包括:一是通過熱力學計算,Na2B4O7·10H2O-Na2CO3-Mg體系化學驅(qū)動力較NaBO2·2H2O-Mg體系更大(ΔGor的值更負);二是Na2B4O7·10H2O-Na2CO3-Mg體系中Na2CO3可以起到分散劑的作用提供堿性條件,防止原材料(特別是Mg)團聚與粘罐及NaBH4分解,從而獲得較好的球磨效率和良好的產(chǎn)率;三是相比NaBO2,Na2B4O7具有更高的反應活性;四是,球磨工藝的優(yōu)化,提高了B源的利用率。為驗證該方法的普適性,將Na2B4O7·10H2O與Na2B4O7·5H2O混合物與Na2CO3和Mg球磨成功合成了NaBH4,其中的Mg也可以被其他還原劑如Ca或Al等取代或者部分取代。此外,其他金屬硼氫化物也可以采用類似方法合成與再生[2]。▲Figure 3. (a) XRD patterns and (b) FTIR spectra of the products obtained after ball milling Mg, Na2B4O7·10H2O, and Na2CO3 mixtures (in 18:1:1 molar ratio) at 1000 CPM for different durations; (c) Yields of NaBH4 with reactants in different molar ratios at 1000 CPM for different durations; (d) Yields of NaBH4 and (e) XRD patterns of the products obtained after ball milling Mg and Na2B4O7·10H2O in different molar ratios (Na2B4O7·10H2O and Na2CO3 were fixed at 1:1 molar ratio) for 20h at 1000 CPM and 1200 CPM, respectively; (f) XRD patterns of the products obtained via ball milling Mg, Na2B4O7·10H2O, and Na2CO3 in a molar ratio of 24.75:1:1 at 1000 CPM for different durations.
提出了一種簡單低成本的NaBH4再生與合成新方法,實現(xiàn)了NaBH4的氫制儲閉合循環(huán),即通過NaBH4常溫常壓水解實時供氫,避免了氫氣的高壓存儲與運輸;而再生時無需氫氣和氫化物,避免了氫氣使用過程中的潛在風險。NaBH4水解產(chǎn)物經(jīng)空氣中CO2自然處理后低溫干燥,產(chǎn)物可直接與Mg在常溫下球磨實現(xiàn)了NaBH4的簡易、高效及廉價的再生及CO2甲烷化,為NaBH4大規(guī)模商業(yè)化應用奠定了理論基礎并開發(fā)了實用技術。采用該方法再生與合成NaBH4,無需高能耗的高溫、高氫壓過程及昂貴氫源的使用,使得能耗和價格大大降低(僅原材料價格可下降24倍)。本工作闡明了結晶水中H+再生為NaBH4中H-的反應機制,揭示了再生反應的機理,建立再生/合成反應的機理模型。項目工作通過將結晶水中的氫制取并原位儲存于NaBH4中,開拓了結晶水作為氫源再生Li/NaBH4的氫制儲運新概念,發(fā)明了NaBH4再生/合成的制/儲氫一體化新技術,為氫能的應用開辟了新途徑。