(本文轉自ICH工作辦公室)
國際人用藥品注冊技術協調會
ICH三方協調指導原則
新原料藥中的雜質
Q3A(R2)
ICH 第四階段的版本
本文件旨在為那些尚未在任何地區或成員國注冊的化學合成的新原料藥在注冊申報時,對雜質研究的內容和限度確定提供指導。本指導原則不適用于臨床研究期間所用的新原料藥。本文件不涵蓋生物/生物制品、肽、寡聚核苷酸、放射性藥物、發酵和半合成產品、草藥以及來源于動、植物的粗制品。
新原料藥中的雜質應分兩個方面闡述:
化學方面:包括對雜質的分類和鑒定、檢測報告的形成、在質量標準中列出雜質以及對分析方法的簡要討論。 安全性方面:對用于安全性研究和臨床研究的新原料藥批次中不存在或含量很低的那些雜質的界定提供專門的指導。
有機雜質(與工藝和藥物結構有關的)。
無機雜質
殘留溶劑
起始物料
副產物
中間體
降解產物
試劑、配體、催化劑
無機雜質 可能來源于生產過程,它們通常是已知的和結構已鑒定的,包括:
試劑、配體、催化劑
重金屬或其他殘留金屬
無機鹽
其他物質(例如:助濾劑、活性炭等)
溶劑 是在新原料藥合成過程中作為載體用于制備溶液或混懸液的有機或無機液體,由于他們一般具有已知毒性,故較易選擇控制方法(見ICH 指導原則Q3C殘留溶劑)。
不包括 在本文件中的雜質為:
⑴ 外源性污染物:不應該存在于新原料藥中,可以用 GMP 來控制的;
⑵ 多晶型;
⑶ 對映異構體雜質。
申請人應對新原料藥在合成、精制和儲存過程中那些實際存在的和最可能產生的潛在雜質進行綜述。該綜述應建立在對合成所涉及的化學反應、由起始物料引入的雜質及可能的降解產物進行合理的、科學的評估基礎之上。可以局限于根據化學反應以及相關條件下可能會產生的雜質進行討論。
此外,申請人還應對新原料藥中雜質檢測的實驗室研究工作進行綜述。其內容包括對采用研制工藝的和擬上市工藝生產的所有批次產品的試驗結果,以及為鑒定在儲存期間可能產生的潛在雜質而進行的強制降解試驗結果(見ICH 指導原則Q1A 穩定性項下)。同時應對那些擬上市的原料藥批次和研制開發過程的原料藥批次中的雜質譜進行比較,并就任何不同之處進行討論。
申報資料中應對那些在新原料藥中實際存在的、含量大于(>)附件1 中鑒定限度的雜質(例如:以原料藥的響應因子計算)的結構進行確證。應該注意的是,對于采用擬上市工藝生產的批次,所有出現的大于鑒定限度的雜質的結構都應確證;另外,對于在推薦的儲存條件下進行穩定性研究中發現的大于(>)鑒定限度的降解產物,也同樣應對其結構進行確證;當某個雜質的結構無法確證時,申報資料中也應提供對該雜質所進行的不成功的研究工作的綜述。如果已嘗試確證過含量不大于(≤)鑒定限度的雜質的結構,那么在申報資料中提交這些研究結果也是很有用的。
通常沒有必要對表觀含量在鑒定限度以下(≤)的雜質進行鑒定。然而,對那些含量不大于(≤)鑒定限度但可能產生不尋常功效或毒性藥理作用的潛在雜質,則應當研發出合適的分析方法。所有雜質均應按照本指導原則后續章節中的要求來界定。
無機雜質通常按藥典或其他適當的方法來檢測和定量。在新藥的研制過程中應對遺留在新原料藥中的催化劑進行評估。對新原料藥質量標準中是否收載無機雜質檢查項目,應進行討論。其限度應根據藥典標準或已知的安全性數據來制定。
3.3 溶劑
應按ICH Q3C“殘留溶劑”指導原則的要求,對新原料藥生產過程中所用溶劑的殘留量的控制進行討論和申報。
注冊申請中應提供書面文件,證明分析方法是經過驗證并適用于雜質的檢測和定量(見ICH Q2A 及Q2B 分析方法論證指導原則項下)。技術因素(如生產能力與質控方法)可作為部分依據來論證可以基于擬上市生產工藝獲得的生產經驗選擇其他的雜質限度。限度采用兩位小數(見附件 1)并不代表常規質量控制中分析方法所需達到的精度。因此,只需經過合適的驗證和論證,可以使用較低精度的技術(如薄層色譜法)。如果研發中所采用的分析方法和準備上市產品的分析方法不同,在申報資料中應予以討論。
分析方法的定量限度應不大于(≤)報告限度。
可用各種技術測定有機雜質的含量,這些技術包括把雜質的響應值與適當的對照品的響應值比較或與藥物本身的響應值比較。應根據使用目的,對分析過程中用于控制雜質的對照品進行定性和定量。可用原料藥作為標準物質來估計雜質的量,如果原料藥和雜質的響應因子不接近,只要應用了校正因子或測得的雜質量高于實際的雜質量,該方法仍是可行的。用于估計已鑒定或未鑒定雜質的限度和分析方法可基于分析方法學上的假設(例如:相同的檢測響應等)。但這些假設的合理性應在申報資料中加以討論。
注冊申請應提供用于臨床、安全性研究、穩定性試驗的所有新原料藥批次產品以及采用擬上市工藝生產的代表性批次產品的分析結果。測定結果應數字化,不應用“符合規定”,“符合限度”等一般性術語。在新原料藥的所有批次中,應報告檢測到的大于(>)報告限度(見附件1)的任何雜質和總雜質的含量,并附所用的分析方法。若雜質含量低于 1.0%,結果應報告至小數點后兩位(如0.06%,0.13%),若大于或等于1.0%,結果報告至小數點后一位(如1.3%)。結果應按傳統規則修約(見附件2)。建議使用數據表格(如電子數據表),各雜質均應以編號或適當的描述表示(如:保留時間)。如果采用其它較高的報告限度,應充分論證其合理性。所有大于(>)報告限度的雜質應進行累加,并作為“總雜質”予以報告。
若在研制期間,分析方法發生了變化,報告的測試結果應標明所用的分析方法,并提供相應的方法學驗證資料。應提供有代表性的色譜圖。方法學驗證中,顯示雜質分離度和檢測靈敏度的、具有代表性批次(例如:加樣試驗)的色譜圖和常規雜質檢測得到的色譜圖,可以反映出有代表性的雜質譜,應在申報資料中予以提供。同時申請人應保證:如需要,可提供每個批次產品的完整的雜質譜(例如:色譜圖)。
另外,申請人還應提供相應的表格,說明在每個安全性研究和臨床研究中使用的新原料藥的批次。
對每批新原料藥,報告內容應包括:
批號與批量
生產日期
生產地點
生產工藝
單個雜質和總雜質的含量
批次的用途
所涉及的分析方法的說明
在新原料藥的質量標準中應包括雜質檢查項目。穩定性研究、化學方面的開發研究以及日常批次分析檢驗的結果有助于預測在上市產品中可能出現的雜質。在新原料藥質量標準中收載的雜質應根據在采用擬上市工藝生產的批次中所發現的雜質來加以取舍。在本指導原則中,對列入新原料藥質量標準中、具有特定限度要求的各個雜質稱為特定雜質。特定雜質可以是已鑒定雜質,也可以是未鑒定雜質。
申報資料應對質量標準中納入哪些雜質提供合理的依據。該依據應包括對用于安全性和臨床研究中批次中所發現的雜質譜進行討論,同時也要考慮采用擬上市工藝生產的原料藥中的雜質譜情況。標準中應納入特定的已鑒定雜質與特定的其含量估計大于(>)鑒定限度(附件1)的未鑒定雜質。對于那些具有特殊功效或產生毒性或未預料到的藥理作用的雜質,其分析方法的定量限或檢測限必須與該雜質應被控制的量相當。對于未鑒定的雜質,所使用的檢測方法和確定雜質量時所采用的假設應予明確說明。特定的未鑒定雜質應采用適當應用適當的方法來標示(例如:“未鑒定雜質 A”,“相對保留時間為0.9 的未鑒定雜質”)。一般來說,任何一個非特定雜質的合理限度應不大于(≤)鑒定限度(附件 1),對總雜質也應建立一個合理的限度要求。
建立的雜質合理限度不能高于經安全性資料界定合理的水平,并且必須與生產工藝和分析能力所能達到的水平一致。如果沒有安全性方面的問題,雜質限度應根據采用擬上市工藝生產的新原料藥批次測定的數據來建立,并應為常規生產和分析上的正常變異及藥物的穩定性特性留有足夠的余地。盡管常規生產中的變化是可以預料的,然而批與批之間雜質水平的顯著變化可能預示著新原料藥的生產工藝尚未得到充分的控制和驗證(見ICH Q6A“質量標準”決策樹1,建立新原料藥中的特殊雜質的認可標準)。限度的兩位小數(見附件1)并不代表特定雜質和總雜質認可標準的精度。
總之,新原料藥質量標準中應包括以下雜質檢查項:
有機雜質:
每種特定的已鑒定雜質
每種特定的未鑒定雜質。
任何不大于(≤)鑒定限度的非特定雜質。
雜質總量。
殘留溶劑
無機雜質
雜質的界定是獲得和評價某些數據的過程,這些數據可用于確保單個雜質或在特定的含量下的一系列雜質的生物安全性。申請人應對所確定的雜質限度提供包括安全性研究在內的理由。對于一個通過充分的安全性研究和臨床研究的新原料藥,其中任何一個雜質的水平應被認為是已經通過合理界定的。對于是動物和/或人體中的重要代謝物的雜質,通常也視為已通過界定。雜質的界定限量(水平)如果高于藥物實際所含的雜質量,則同樣可以根據對已完成的安全性研究中使用藥物中的實際雜質量來判斷其合理性。
如果可獲得的數據不能界定某一雜質擬定的限度,而且當該限度超過了附件 1 所列的界定限度時,則必須做進一步研究,以獲得必要的數據來支持該限度的合理性。
對于某些藥物,可以根據科學原理和認知水平(如藥物的類別和臨床經驗),對其雜質界定限度進行適當調整。例如,某些雜質在一些藥物中或治療類別中已證明與病人的不良反應有關,則該雜質的界定是非常重要的。在這種情況下,應制訂更低的界定限度。反之,如果考慮相似情況(患者人群、藥物類別、臨床情況)后,對安全性的顧慮比通常情況小,那么這些藥物的界定限度可以高一些。總之,對限度的確定應具體情況具體分析。
雜質鑒定和界定的決策樹(附件 3)描述了當雜質含量超過限度時所應考慮到的事項。在一般情況下降低雜質含量使其低于限度要比提供雜質的安全性數據來得簡單。或者當文獻資料中對某一雜質的安全性數據比較充分時,也可用于界定該雜質的限度。如果兩者均不可行,則應考慮進行額外的安全性試驗。如何合理地界定一個雜質將取決于許多因素,包括患病人群、每日劑量、給藥途徑與療程。這類試驗雖然可用分離出來的雜質進行研究,但通常是用含有被控制的雜質的新原料藥來進行研究。
雖然本指導原則在臨床研究階段并不適用,但在研究后期,本原則的限度對于評價擬上市新原料藥生產過程中的各批次中出現的新雜質是有用的。在研究后期,任何含量大于(>)附件 1 中鑒定限度(見附件3 雜質鑒定和界定的決策樹)的新的雜質均需鑒定。同樣,如果雜質量大于(>)附件1 中的界定限度,都應進行界定。界定某新雜質的安全性評價研究,可將含有一定代表量新雜質的原料藥與以前界定過的原料藥進行比較。也可考慮采用已分離出來的雜質樣品進行安全性評價研究。
附件 1:雜質限度
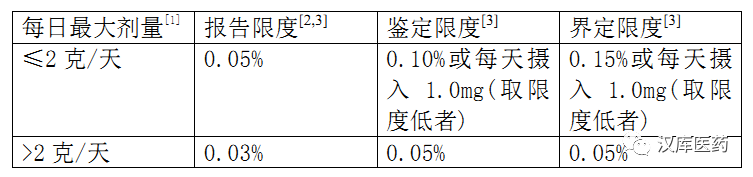
本附件僅用于示范,而不是作為在申報資料中應當如何呈現雜質研究結果的模板。具體的原始數據未展現。
報告限=0.05%
鑒定限=0.10%
界定限=0.15%
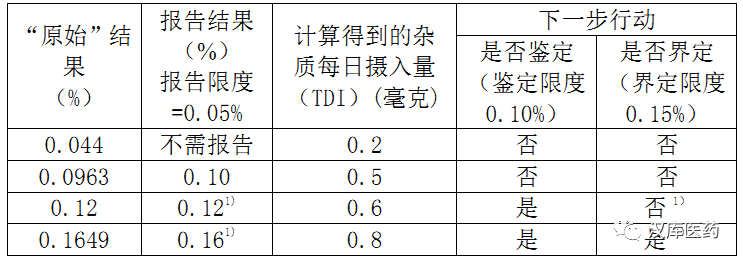
報告限=0.05%
鑒定限=0.10%
界定限=1.0mg TDI
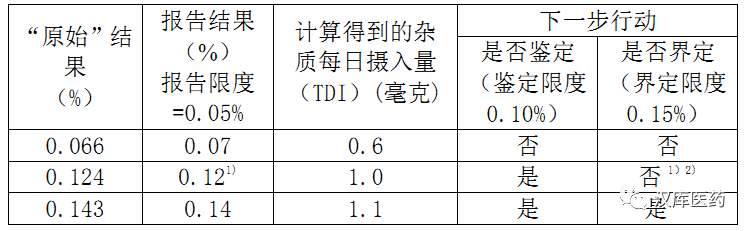
1) 雜質經鑒定后,如果確定的響應因子和原假設明顯不同,應重新檢測該雜質的實際含量,并根據界定限度(見附件1)重新考慮下一步的研究工作。
2) 為確證雜質含量是否超過限度,報告的結果應該根據以下原則進行評估:如果限度是以%表示,則報告的結果也應修約到與限度相同的小數點位數,并直接與限度值進行比較。如果限度是以TDI 表示,則報告的結果也需轉換為TDI表示,并修約到與限度相同的小數點位數,然后再與限度值進行比較。例如,含量為0.12%的某雜質所對應的TDI 值為0.96 毫克(絕對值),然后修約為1.0 毫克,經比較并未超過以TDI 表示的界定限度(1.0 毫克)。
附件 3:雜質鑒定和界定的決策樹
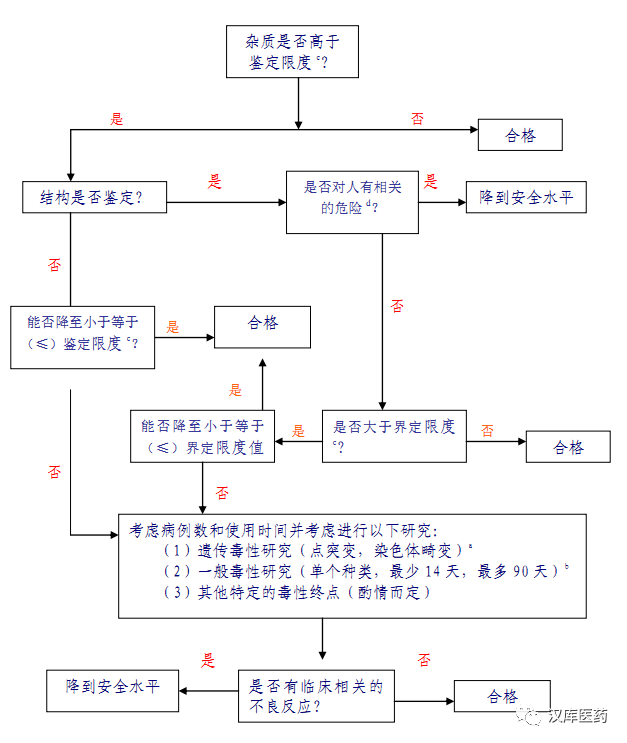
注:
a) 如需要,應進行最低限度的篩選試驗(如潛在致突變性),認為是合適的該類試驗包括:體外點突變和染色體畸變試驗。
b) 如需進行一般毒理研究,應將未界定的物質與界定的物質進行比較,研究時間應根據可用的相關信息而定,并使用最能反映某一雜質毒性的動物種屬。根據具體情況,單劑量藥物可進行單劑量試驗。一般最短14 天,最長90 天。
c) 如果雜質具有特殊毒性,可以采用較低的限度。
d) 例如,已知的該雜質的安全性數據或其結構的分類是否排除了人接觸該濃度雜質的可能?
(本文轉自ICH工作辦公室)








