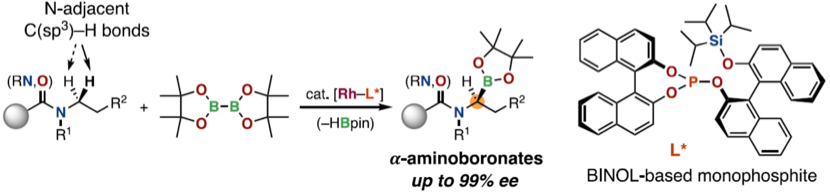
近年來,由于對具有藥物活性的含硼化合物的需求不斷增長,所以如何有效開發合成手性的α-氨基硼酸也成了一種必要的研究。因為烷基硼酸酯參與了許多轉化,這些通過各種碳硼鍵的轉化產生一系列的內源多功能性產物,使得人們對于高效合成這些化合物的需求也是很高的。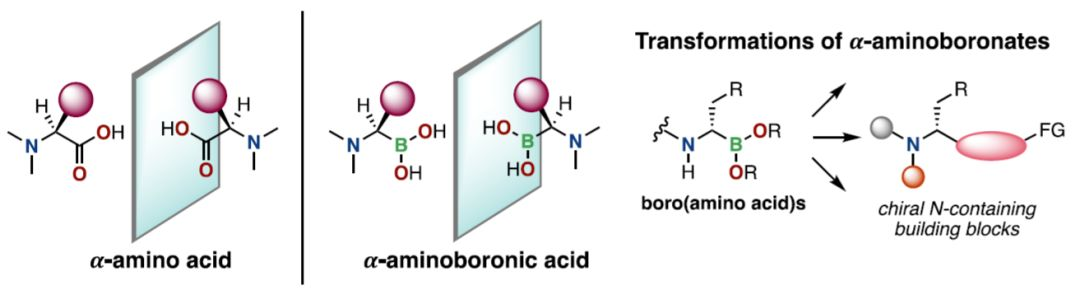
圖片來源:J. Am. Chem. Soc.
其中,硼酸及其衍生物作為合成的基本中間體,可以使用高度功能化的分子,包括中間代謝物、胺衍生的有機催化劑和N-α取代的化合物等。且這些化合物已在不對稱合成中廣泛用作為手性助劑。

圖片來源:J. Am. Chem. Soc.
近期,日本北海道大學的Masaya Sawamura教授報道了一種銠手性磷酸酯配體的催化體系,該體系能夠對2-(N-烷基氨基)雜芳基和烷酰基或芳酰基酰胺等化合物進行硼烷化反應。
圖片來源:J. Am. Chem. Soc.
該研究也對這種手性α-氨基硼酸酯應用在立體選擇性的轉化中,包括與芳基鹵化物Suzuki-Miyaura偶聯和與α-氨基酸的異氰酸酯衍生物進行銠催化的反應來提供了一種新的肽鏈延伸方法等。
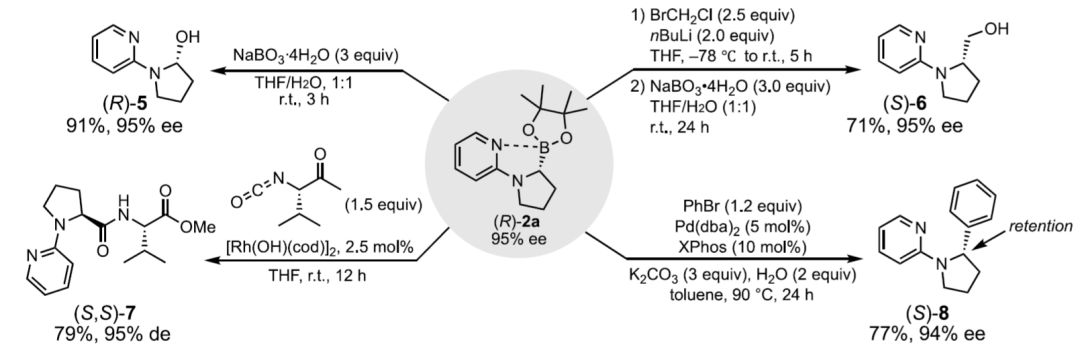
圖片來源:J. Am. Chem. Soc.
此外,作為這項工作的重點,該硼化方法成功應用于無保護的二肽化合物的位點選擇性和立體選擇性的C(sp3)-H硼化反應,可顯著的簡化抗癌藥物分子Bortezomib的合成。

圖片來源:J. Am. Chem. Soc.
參考文獻:Asymmetric Synthesis of α-Aminoboronates via Rhodium-Catalyzed Enantioselective C(sp3)-H Borylation
DOI: 10.1021/jacs.9b12013
原文作者:Ronald L. Reyes, Miyu Sato, Tomohiro Iwai, and Masaya Sawamura*