分享一篇發表在JACS上的文章,題目為“Warhead Strategy for Targeted Protein S-Nitrosation",通訊作者是來自中國藥科大學的黃張建和吳建兵研究員。該團隊聚焦于一氧化氮(NO)供體的藥物研發。

蛋白質S-亞硝化(S-nitrosation, SNO)作為一氧化氮(NO)介導的關鍵翻譯后修飾(PTM),通過調控蛋白質活性、蛋白質-蛋白質相互作用網絡以及與其他PTM的串擾,在多種生理病理過程中扮演著核心調控角色。然而,由于NO分子固有的氣態自由基特性導致的高度擴散性和反應非特異性,目前針對特定蛋白質的位點選擇性S-亞硝化調控仍面臨重大技術挑戰。
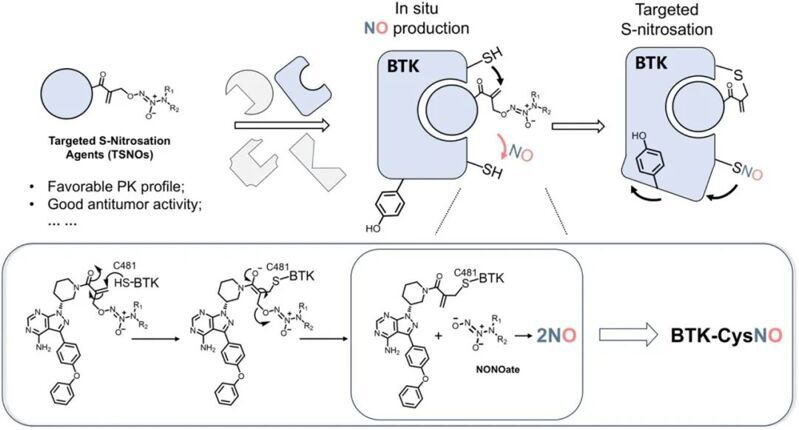
為解決這一關鍵科學問題,本研究基于伊布替尼(Ibrutinib)的分子骨架進行理性設計:選用α-甲基丙烯酰胺作為共價彈頭實現靶向結合,同時整合二醇二氮烯鎓鹽(NONOates)作為NO供體模塊,成功構建了8個具有雙重功能的亞硝化調控劑(TSNO1-8)。該系列化合物展現出獨特的雙機制協同作用:(1)通過丙烯酰胺基團與BTK活性位點C481殘基發生特異性邁克爾加成,實現靶向抑制;(2)在靶標結合后,NONOate基團經觸發釋放NO分子,誘導鄰近半胱氨酸殘基發生位點特異性S-亞硝基化修飾。
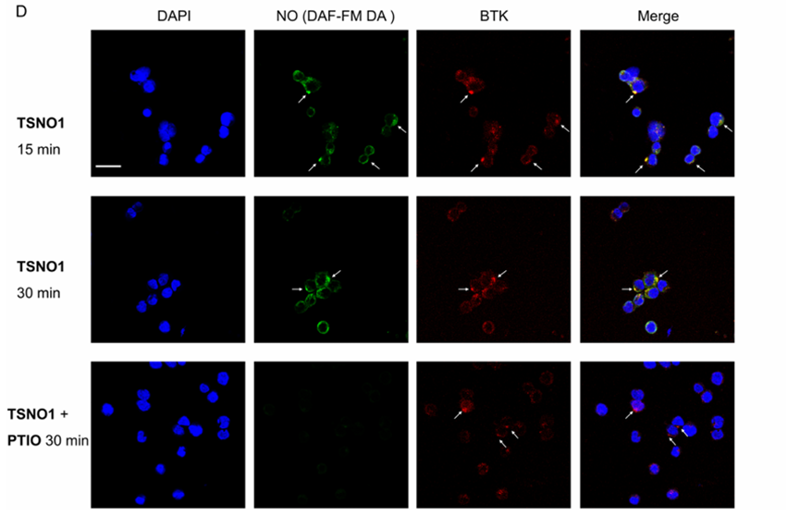
作者系統評估了TSNO1在不同生物環境中的穩定性。實驗結果顯示,TSNO1在含硫醇試劑的緩沖體系、大鼠血漿及肝微粒體等復雜生物環境中均表現出良好的穩定性,且其在BTK溶液中的NO釋放量顯著高于非靶向環境,證實了該化合物的靶向釋放特性。進一步的共聚焦顯微鏡分析表明,在表達BTK-mCherry的Daudi細胞中,TSNO1處理后的NO信號(綠色熒光)與BTK蛋白(紅色熒光)呈現顯著共定位,直觀驗證了其靶向遞送能力。在體外S-亞硝化效率評估中,TSNO1可特異性增強BTK的S-亞硝化修飾,而整體細胞S-亞硝化水平與依魯替尼處理組無顯著差異;相比之下,非靶向NO供體則引起廣泛的蛋白S-亞硝化,這一對比結果充分體現了TSNO1設計的精準修飾優勢。
通過對217種激酶的選擇性譜分析,作者發現TSNO1展現出顯著優于伊布替尼的靶向特異性。TSNO1對BTK的抑制率超過90%,而對EGFR、JAK等家族激酶的脫靶效應較伊布替尼顯著降低。這些發現不僅證實了TSNO1的高度選擇性,也為設計靶向蛋白翻譯后修飾的精準調控工具提供了重要理論依據。
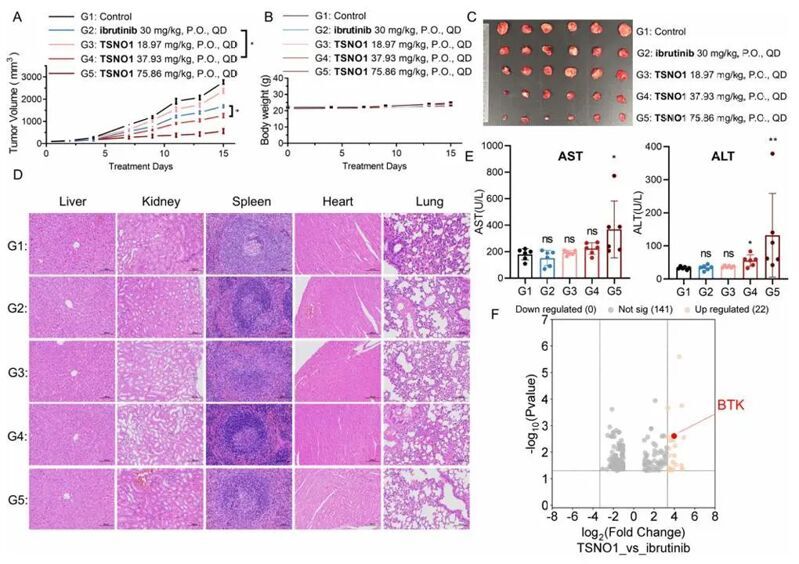
作者通過U937異種移植小鼠模型系統評估了TSNO1的體內抗腫瘤活性與靶向S-亞硝化特性。口服給藥(37.93 mg/kg)的TSNO1展現出顯著優于等摩爾劑量伊布替尼的腫瘤生長抑制作用,且其抗腫瘤效應呈現明顯的劑量依賴性。安全性評估顯示,經TSNO1處理的實驗組小鼠主要臟器(肝、腎、脾、心和肺)組織結構完整,H&E染色未觀察到壞死、炎癥或變性等病理改變,證實了該化合物的良好體內安全性。為闡明TSNO1的作用機制,作者對腫瘤組織進行了高分辨S-亞硝化蛋白質組學分析。定量結果顯示,與伊布替尼對照組相比,TSNO1處理組中BTK的S-亞硝化水平呈現特異性升高。值得注意的是,蛋白質組學數據揭示TSNO1具有高度靶向性:在檢測到的163種S-亞硝化蛋白中,141種蛋白的修飾水平維持穩定,僅22種蛋白發生修飾水平變化。與依魯替尼相比,Cys527的S-亞硝化誘導了BTK的進一步構象變化,將Tyr551嵌入內部,增強了對Tyr551的磷酸化抑制,阻礙了BTK的激活,并在共價抑制之外提供了額外的治療益處。
本研究創新性地提出了一種激酶靶向S-亞硝化調控策略,并成功開發了具有精準修飾能力的TSNOs分子體系,展現出優異的體外和體內抗腫瘤活性,同時具備理想的類藥物特性。
本文作者:THT
責任編輯:TZS
DOI:10.1021/jacs.5c07409
原文鏈接:https://doi.org/10.1021/jacs.5c07409








