分享一篇發表在Nature Metabolism上的文章,題目為:“An alternative route for β-hydroxybutyrate metabolism supports cytosolic acetyl-CoA synthesis in cancer cells”。 本文通訊作者是范安德爾研究所的Evan C. Lien教授,Lien教授的研究方向是探究飲食介導的營養變化如何影響腫瘤生長和代謝,從而為腫瘤治療提供新策略。

當我們禁食或低血糖時,肝臟會產生酮體,可以作為大腦、心臟和肌肉等組織的重要能量來源,而β-羥基丁酸(β-OHB)是最主要和最重要的酮體成分。最新研究表明,某些腫瘤細胞也能代謝β-OHB,β-OHB在線粒體中發生氧化,其中BDH1、OXCT1和線粒體硫解酶將β-OHB轉化為乙酰輔酶A,隨后進入三羧酸循環。

為了深入探究癌細胞中β-OHB的代謝途徑,作者首先評估了幾種癌細胞中BDH1和OXCT1的蛋白水平,發現這兩個蛋白在某些腫瘤細胞中顯著高表達。通過同位素示蹤實驗,作者發現β-OHB除了在線粒體中產生乙酰輔酶A外,還會通過與檸檬酸結合后輸出到胞質中,產生胞質乙酰輔酶A。胞質乙酰輔酶A有幾個下游去向,包括脂肪酸合成、膽固醇合成以及蛋白質和組蛋白乙酰化。作者發現β-OHB可以促進脂質缺乏條件下的腫瘤細胞增殖,說明胞質乙酰輔酶A是β-OHB的一個重要下游去向。
在同位素示蹤實驗中,作者驚喜地發現,在某些腫瘤細胞中,胞質乙酰輔酶A的標記程度比檸檬酸更高,說明除了檸檬酸途徑外,還有其他代謝途徑使β-OHB轉變為胞質乙酰輔酶A。作者通過敲除實驗驗證了BDH1對其代謝的重要性,而敲除OXCT1對其影響較小,因此作者推測β-OHB可能通過線粒體乙酰乙酸(OXCT1的底物)轉運到胞質,從而產生胞質乙酰輔酶A。通過敲除胞質酶AACS,確認了該代謝通路。最后,作者還在腫瘤小鼠模型中進行了BDH1、OXCT1和AACS的敲除實驗,證實了β-OHB的代謝途徑。
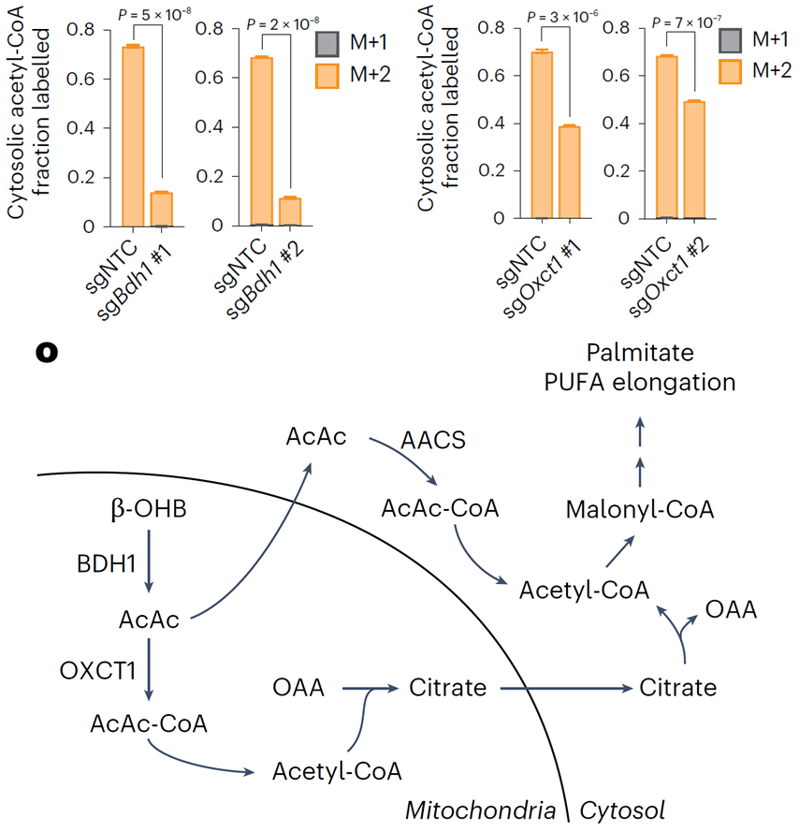
總之,作者證明了在能夠代謝β-OHB的癌細胞中,β-OHB是胞質乙酰輔酶A產生的主要來源。除了通過OXCT1依賴性從三羧酸循環產生檸檬酸的胞質乙酰輔酶A合成途徑外,作者還識別了一個替代途徑,即線粒體中β-OHB衍生的乙酰乙酸可以輸出到胞質,通過AACS和胞質硫解酶轉化為胞質乙酰輔酶A。作者對β-OHB衍生胞質乙酰輔酶A替代途徑的識別將有助于未來的相關研究。
本文作者:YSL
責任編輯:MB
DOI:10.1038/s42255-025-01366-y
原文鏈接:https://doi.org/10.1038/s42255-025-01366-y








