分享一篇發表在Analytical Chemistry上的文章,題目為“Selective Probing of Acidic Amino Acid Residues for Protein Structural Analysis by Covalent Labeling and Mass Spectrometry”,通訊作者是來自Texas大學的Saiful M. Chowdhury教授和Joseph A. Buonomo助理教授,研究方向為蛋白質的生物偶聯策略等。

蛋白質的表面大部分由親水性氨基酸所組成,這些氨基酸介導了蛋白質之間的相互作用,在這其中兩種酸性氨基酸天冬氨酸和谷氨酸扮演著重要的角色。此前傳統的碳二亞胺的標記方法雖然能夠激活羧基反應性,但受限于其非特異性和副產物的形成,并且會與多肽或蛋白上的其他親核殘基發生反應。因此尋找一種能夠化學選擇性修飾蛋白質表面酸性氨基酸殘基的標記方法,對于研究蛋白質結構和復合物功能十分重要。本文開發出一種二苯基重氮甲烷DPDAM試劑,能夠直接實現羧酸向酯鍵的轉化并且不會生成其他副產物。
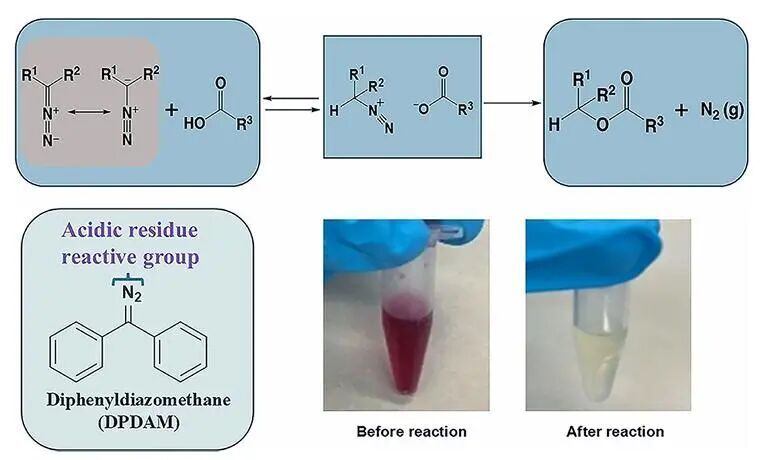
作為一種不可逆的標記反應,羧基直接進攻連接有偶氮基團的碳原子,形成共價鍵的同時,離去一分子氮氣。在反應前后,反應體系將會發生顏色的變化。使用標肽優化反應條件的過程中,作者發現,當反應體系的pH值由4降到2時,不再標記兩種酸性氨基酸,而僅對多肽的C端進行標記。這種pH值依賴的化學反應性被解釋為在較為酸性的環境中,側鏈上的酯鍵保護劑會因為更快發生的水解反應而脫除保護,從而形成僅對C端修飾的結果。通過DPDAM在不同pH條件下的化學反應性不同,能夠實現對蛋白質酸性氨基酸側鏈和C端的特異性標記,而不會對賴氨酸、組氨酸等發生脫靶標記。將該策略應用到純BSA蛋白上的標記,能夠成功鑒定出其表面上的酸性氨基酸殘基。
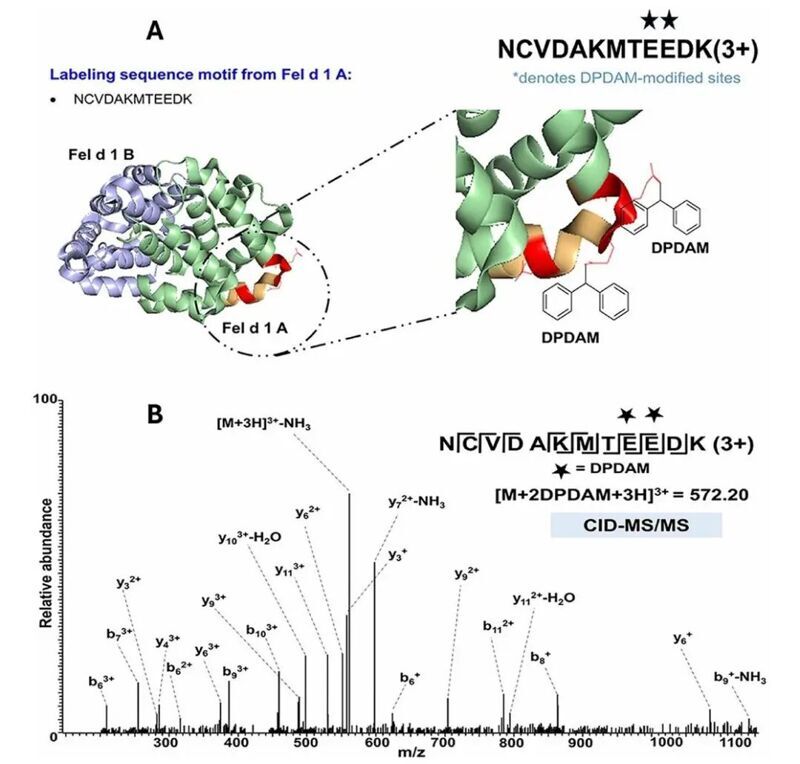
作者以一組蛋白復合物作為實例證明了上述標記策略的可行性。Fel d 1蛋白是一種貓源的過敏原,作者進行了酸性羧基的標記,對其中一條標記肽進行檢查,發現僅僅在蛋白質結構中暴露在表面的兩個酸性殘基被標記,而隱藏在內部的酸性殘基并未被標記,這成功證明了在這些標記條件下,蛋白質的結構信息和互作信息能夠得到保留,最終考慮到標記的低pH環境,作者認為這一策略在研究溶酶體中酸性氨基酸介導的蛋白互作上具有較大的優勢。
總的來說,本文開發了一種新型的標記酸性氨基酸殘基或者肽段C端的特異性重氮試劑,能夠實現不同pH條件下側鏈羧基或者C端羧基的選擇性標記,在研究蛋白質互作或者生物偶聯反應上有廣闊的應用前景。
本文作者:SHL
責任編輯:WYQ
DOI:10.1021/acs.analchem.5c03258
原文鏈接:https://doi.org/10.1021/acs.analchem.5c03258








