分享一篇發(fā)表在JACS上的文章,題目為“Indolequinone-Based Hypoxia-Activated Proteolysis Targeting Chimeras Selectively Degrade BRD4 in Hypoxic Cancer Cells”。通訊作者是來自University of Oxford和 University of California Los Angeles 的 Stuart J. Conway教授。他的研究興趣聚焦于化學與生物學的交叉領域,致力于運用合成有機化學技術推動生物系統(tǒng)的深入研究。

目前蛋白降解與鄰近誘導領域研究活躍,已有超過30種PROTACs進入臨床試驗,展現(xiàn)出巨大的治療潛力。
然而該技術仍存在局限,尤其在臨床轉(zhuǎn)化階段。首要問題是蛋白降解在健康組織中可能引發(fā)劑量限制性靶向毒性。此外,E3連接酶配體可能保留對其同源E3連接酶的基礎活性而導致脫靶效應。例如基于沙利度胺及其類似物等免疫調(diào)節(jié)藥物(IMiDs)的CRBN招募型PROTACs,仍能降解CRBN新底物IKZF1和IKZF3,這種脫靶活性會獨立于POI降解過程抑制細胞增殖并刺激免疫系統(tǒng)。
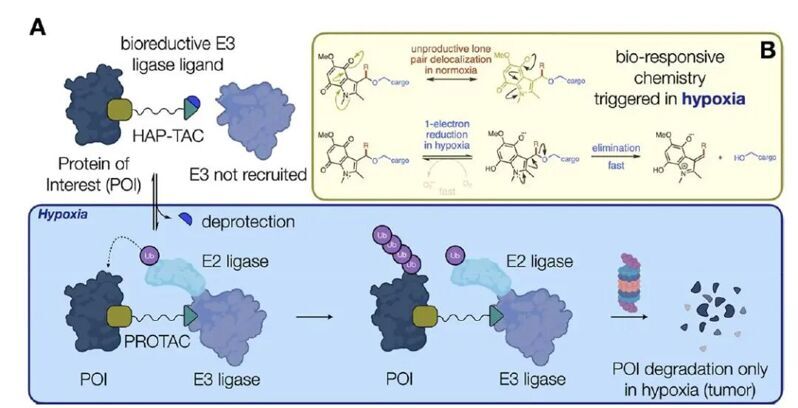
為解決這些問題,研究者開發(fā)了能在特定環(huán)境下選擇性激活的PROTACs前藥。最早實現(xiàn)的是光激活PROTACs:通過在VHL或CRBN配體上連接光裂解基團實現(xiàn)空間控制釋放,但治療應用受限于紫外光的組織穿透能力。低氧激活前藥(HAPs)是靶向腫瘤的有效策略。低氧是實體瘤標志性特征,由腫瘤快速生長導致代謝需求增加、血管結(jié)構異常及供血不足共同引發(fā)。利用這一機制,HAPs可以在常氧細胞中保持無活性前藥狀態(tài),在低氧環(huán)境中經(jīng)酶催化還原釋放活性藥物。
作者近期研究發(fā)現(xiàn)吲哚醌生物還原基團能在多種低氧條件下有效釋放熒光染料。本研究利用該觸發(fā)機制開發(fā)結(jié)構新穎的HAP-TACs:通過吲哚醌保護VHL或CRBN配體使其在常氧失活,在低氧環(huán)境中經(jīng)NQO1或細胞色素P450氧化還原酶生物還原后高效釋放活性PROTACs,實現(xiàn)環(huán)境依賴性蛋白降解。
先前研究表明, VHL配體(如VH032)中羥脯氨酸殘基的結(jié)構對于高親和力結(jié)合VHL至關重要。改變此位置立體構型或取代羥基會阻止與VHL的結(jié)合。因此,該官能團是連接生物還原基團以制備無活性前藥的理想位點。在此位置連接的基團經(jīng)生物還原和裂解后,將釋放出有活性的PROTAC。
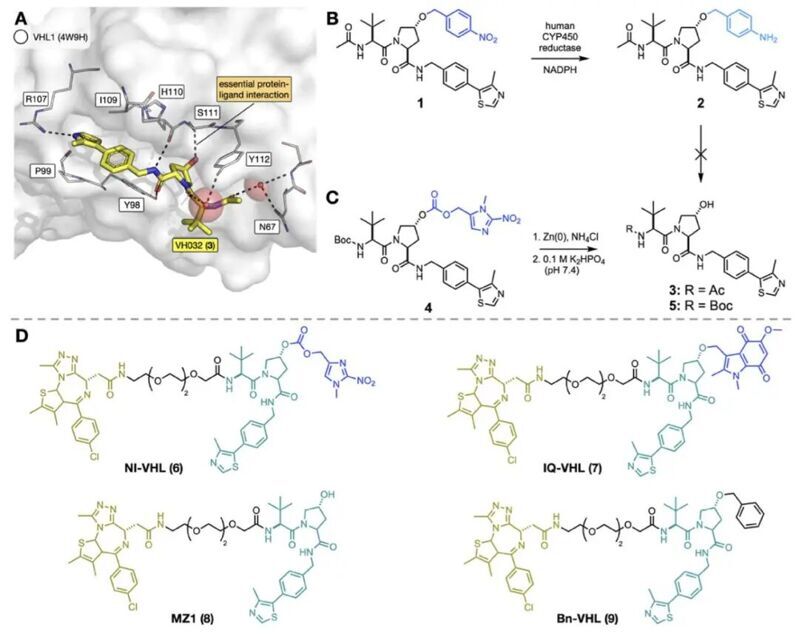
作者首先研究了在VH032的羥脯氨酸模擬物上連接硝基芳基生物還原基團(化合物1)。隨后,作者使用人源CYP450還原酶,在低氧條件下按照既定方案處理4-硝基芐基保護的VH032 (1)。雖然觀察到硝基被有效還原生成苯胺2,但該產(chǎn)物并未裂解生成自由的VH032配體3,這表明4-硝基芐基基團不適用于HAP-TACs的開發(fā)。接下來,作者研究了在Boc保護的VH032衍生物羥基上連接1-甲基-2-硝基咪唑基團的合成得到了化合物4,該基團在低氧下更易發(fā)生生物還原。用Zn(0)和NH?Cl處理化合物4,隨后用磷酸鹽緩沖液處理,得到了Boc保護的VH032衍生物 (5),這與還原及后續(xù)裂解過程一致。受此積極結(jié)果的推動,作者合成了MZ1 (8),然后將相同的基團應用到MZ1的VHL配體的羥基上,得到化合物6(NI-VHL)。
作者近期在生物還原性染料中應用了吲哚醌基團來成像低氧梯度,因此決定研究該基團是否也能用于制備低氧激活的PROTACs。得到了將吲哚醌直接連接到VHL配體上的化合物7(IQ-VHL)。為了給VHL招募型HAP-TACs提供陰性對照,還合成了在同一位置烷基化了無活性芐基的PROTAC (9, Bn-VHL)。
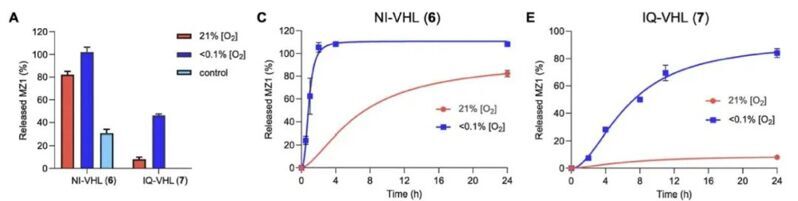
接下來,作者將化合物6和7、活性PROTACs MZ1 (8)、以及兩個陰性對照 Bn-VHL (9) 與NADPH–CYP還原酶在低氧(<0.1% O?)或常氧(21% O?)下孵育24小時。同時在低氧無還原酶的條件下進行平行孵育,以評估化合物的水解穩(wěn)定性。通過HPLC分析監(jiān)測測試化合物的殘余底物以及相應活性PROTACs的釋放情況。雖然NI-VHL (6) 在低氧條件下24小時后釋放了100%的MZ1,但它在常氧條件下也釋放了82%的MZ1,這意味著該化合物在低氧與常氧之間釋放MZ1的選擇性不佳。此外,在沒有酶的情況下,NI-VHL也釋放了31%的MZ1,表明該化合物在所用緩沖條件下易發(fā)生水解而不穩(wěn)定。相比之下,IQ-VHL (7) 在常氧條件下穩(wěn)定,僅釋放8%的MZ1;而在低氧條件下24小時后釋放了41%的MZ1。該化合物在無酶的低氧對照孵育中也保持穩(wěn)定,未觀察到MZ1的釋放。這些數(shù)據(jù)表明IQ-VHL (7) 能夠在低氧條件下選擇性釋放活性PROTAC。
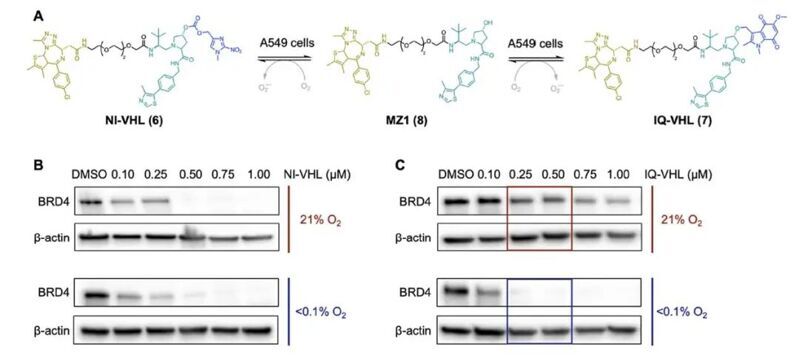
接下來,作者在A549細胞中評估了HAP-TACs在低氧(<0.1% O?)或常氧(21% O?)條件下誘導BRD4降解的能力。NI-VHL (6) 在常氧和低氧條件下的BRD4降解水平幾乎無選擇性。在1 μM濃度下,NI-VHL在常氧中誘導了94 ± 3%的BRD4降解,在低氧中降解了95 ± 6%的BRD4。而在更低濃度下,該化合物在兩種條件下均未對BRD4水平產(chǎn)生顯著影響。相比之下,IQ-VHL (7) 在常氧條件下幾乎不誘導或僅誘導極少量BRD4降解,但在低氧條件下能實現(xiàn)BRD4的幾乎完全降解。該化合物的最佳選擇性出現(xiàn)在0.5 μM濃度:低氧條件下誘導98 ± 2%的BRD4降解,而常氧條件下僅觀察到輕微降解。
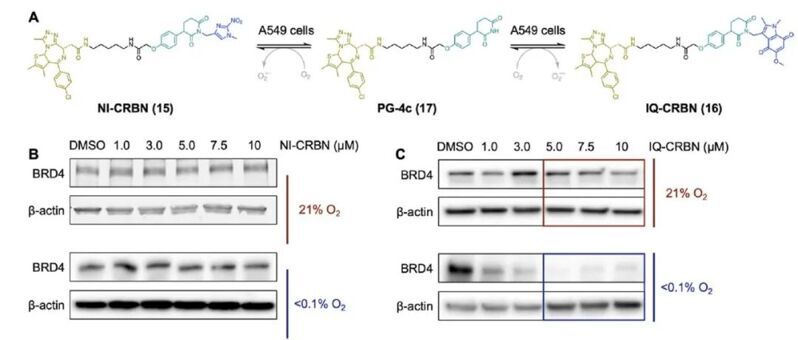
此外,作者將此策略也應用到CRBN配體上,也得到了類似的結(jié)果。
總之,作者首次將吲哚醌作為生物還原觸發(fā)器應用于PROTACs,解決了此前低氧激活PROTACs的穩(wěn)定性與選擇性難題,實現(xiàn)了低氧選擇性蛋白降解,為擴大PROTACs治療窗口、降低靶向毒性提供了創(chuàng)新策略,有望推動HAP-TAC在實體瘤治療中的臨床應用。
本文作者:CZH
責任編輯:LYC
DOI:10.1021/jacs.5c10240
原文鏈接:https://doi.org/10.1021/jacs.5c10240








