羰基化合物的轉化反應是有機反應的重要組成部分,通過α-位點的親核試劑對醛或酮進行加成反應被證明是非常好的合成方法。最近,通過單電子(SET)氧化方法能夠實現產生α-羰基自由基物種,進而反應生成各種取代碳基化合物。
在這些反應中,多種催化劑和多種策略被開發用于控制反應的選擇性和手性。比如,
1)MacMillian等發現SOMO催化經由(烯胺,enamine)自由基中間體生成烷基取代的醛(Nat. Chem. 2017, 9, 1037;J. Am. Chem. Soc. 2007, 129, 7004)。
2)α取代的羰基自由基在和Lewis酸的反應中展現較強的反應性,能夠通過手性Lewis酸對自由基進行活化。
3)Yang等發現鎂/雙惡唑啉(magnesium/bisoxazoline)作用的非對稱性分子內自由基-自由基級聯環化反應(intramolecular radical-radical cyclization cascade)(Angew. Chem. Int. Ed. 2006, 45, 255)。
4)此外,1,3-二羰基化合物和烯烴之間的自由基極化加成被發現是一種有效的構建雜環化合物的方法(Org. Lett. 2005, 7, 2997)。
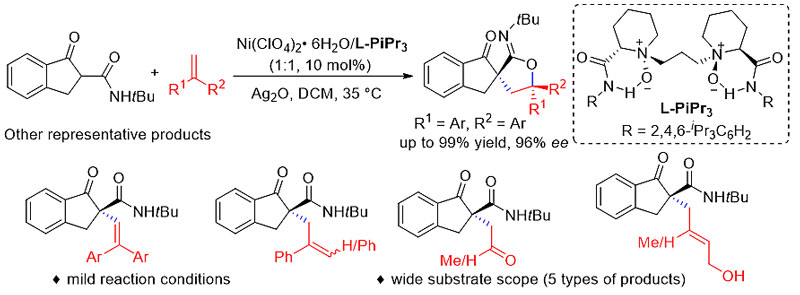
有鑒于此,四川大學馮小明、劉小華等人報道了通過手性N, N’-dioxide-NiII手性催化劑和Ag2O結合,在溫和條件中進行高效手性分子間的自由基交叉反應。對多種端基烯分子和茚滿酮甲酰胺/酯進行了拓展,該反應通過自由基加成/環化反應過程進行,能以較高的收率(高達99 %)和較高的手性產率(高達96 % ee)生成螺亞胺內酯(spiroiminolactones)或螺甾內酯(spirolactone)。
本文要點:
1)反應條件篩選。通過二苯基乙烯和1,3-二羰基化合物進行反應生成螺環產物的反應進行優化,并對反應條件進行優化。對Ni催化劑進行篩選,分別使用Ni(OTf)2,Ni(ClO4)2,NiCl2,Ni(acac)2作為Ni源,發現Ni(ClO4)2效果最好,對手性Lewis酸配體進行篩選,發現L-PiPr3和Ni(ClO4)2配合催化體系有最好的手性收率(95 % ee)和較好的反應產率(86 %)。
2)底物擴展。對13種茚滿酮甲酰胺/酯底物進行測試,發現能以中等到高收率獲得產物,并且產物的ee值大部分能達到95 %。對9種不同的1,1-二芳基烯烴底物進行拓展,能以中等到高收率獲得目標產物,并且大部分產物的ee值能達到90 %。
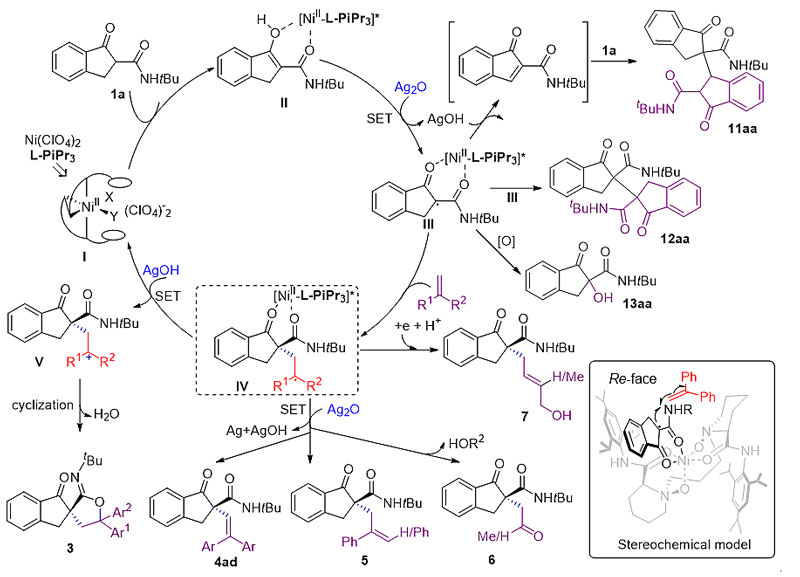
3)反應機理。通過TEMPO捕捉實驗對反應機理進行測試,通過帶有高張力環丙基取代基的烯分子進行了自由基控制實驗,得到了可能的反應機理。
參考文獻:
Xiying Zhang, Wangbin Wu, Weidi Cao, Han Yu, Xi Xu, Xiaohua Liu*, Xiaoming Feng*
Enantioselective Radical‐Polar Crossover Reactions of Indanonecarboxamides with Alkenes
Angew. Chem. Int. Ed., 2020, 59, 4846-4850 DOI: 10.1002/anie.201914151
https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201914151










