有立體中心的不飽和無環烴骨架的有效構造代表了有機化學中最具挑戰性的任務之一。在之前的科研工作者不斷探索,已證明過渡金屬催化的烯烴-炔烴偶聯反應為此提供了潛在的解決方案。在該反應中,陽離子釕配合物催化單取代烯烴與炔烴的順式加成,導致在各種復雜的生物活性化合物和天然產物中形成1,4-二烯,像(+)-山莨菪素A,兩性內酯P等等。但是,與單取代的烯烴不同,使用多取代的烯烴,特別是三取代的烯烴進行類似反應的成功相對較少。利用多官能團化的烯烴與炔烴偶聯,可以為構建分子的復雜性提供一條捷徑。因此,將底物范圍擴大到無活性的高階烯烴是一個非常重要的問題。
轉化過程通過釕烷基環戊烯中間體(II,方案1a)進行,該中間體可通過連續的β-H消除得到1,4-二烯產物。當以三取代烯烴為底物時,在環戊烯II的形成過程中,空間碰撞增加,β-氫化物消除所需的幾何構型也導致與支化取代基進一步的空間相互作用。到目前為止,只實現了釕催化的三取代烯烴與炔烴的分子內偶聯反應(方案1b)。三取代烯烴的分子間烯烴?炔烴偶聯反應仍然非常具有挑戰性,需要開發新的策略來快速獲得具有較大結構復雜性的目標。在Ru催化的烯烴?炔烴偶聯反應中,含三個烷基取代基的烯烴是無反應的,但在烯烴上使用可交換取代基,其空間位阻和電子性質提供了適當的反應性,將是一種有吸引力的替代方法。最近關于1,2-雙硼酸乙烯酯化合物的便捷獲取方法及其對連續C-C鍵形成反應的出色反應的報道使作者考慮將其用于Ru催化的反應中。盡管取代的乙烯基雙(硼酸酯)具有相當大的空間體積,它們仍可以用作三取代的烯烴等效物,從而提供了進入相應的(E,E)-3,4-二硼基-1,4-二烯的途徑(方案1 c) 。
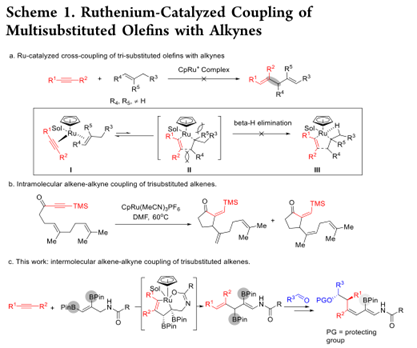
與簡單的三取代烯烴相比,取代的乙烯基雙(硼酸酯)顯示出更高的反應性。首先,硼的平面性質,三價性質和sp2雜化可以減輕中間體II和β-氫化物消除過程中的空間應變。其次,未填充的硼的p軌道通過降低烯烴的LUMO能量有助于促進釕與雙鍵的絡合。最后,在烯烴上引入定向基團進一步提高了反應性。底物的螯合活化和β-氫化物活化均可幫助降低取代基的抑制作用。此外,生成的雙(硼酸酯)化合物是用于復雜分子的簡明合成的通用構建基塊。硼酸酯部分可以迅速轉化為其他功能。例如,醛與烯丙基硼酸酯的立體選擇性烯丙基硼化提供了一種可靠的方法來獲得均烯丙基醇,后者是制造聚酮天然產物的重要組成部分。硼酸乙烯基酯也可用于引入各種官能團,例如羰基,鹵化物,烷基或芳基。
最初,選擇三取代的N-氨基甲酸酯烯丙基二硼烷基烯烴2a作為與炔烴偶聯的模型底物。在CpRu(CH3CN)3PF6存在下,將2a順式加成至2-丁炔(1a)可產生相應的3,4-二硼基-1,4-二烯3a,產率為71%,具有優異的幾何選擇性(eq1)。為了使產物對色譜分離更穩定,作者在糠醛4a的存在下進行了Ru催化的烯烴-炔烴偶聯反應(Table1)。
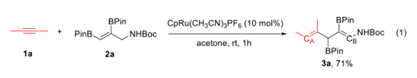
令人欣慰的,這三組分偶合反應在丙酮中順利發生在室溫下,得到高烯丙基醇5a中以58%的產率,為3:1 z/e具有優異的異構體混合物的非對映選擇性。在這種情況下,由于CB周圍的位阻,僅觀察到CA的烯丙基化。5a的 NOE分析表明,C3–C4雙鍵主要幾何結構的立體化學是Z構型。其他數據見下表。

我們提出釕催化劑由于其與醛的配位在烯丙基硼化過程中可能存在問題。當烯烴-炔烴偶聯反應完成后添加醛時,分離出預期產物5a的收率為81%,并且僅觀察到單一的幾何異構體(方案2a)。為了避免羥基和硼酸酯之間的相互作用,進行了進一步的保護過程。以89%的產率獲得作為單一異構體的乙酰化產物6a(方案 2b)。
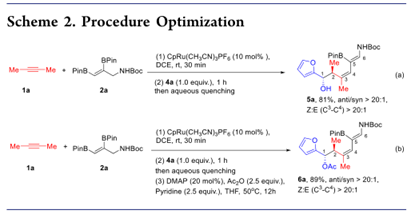
在確定了最佳條件后,作者開始對該三組分反應中的醛進行了底物適用性考察。芳基和烷基取代醛與生成的烯丙基硼酸酯3a反應生成相應的3,5二烯基高烯丙酸乙酸酯,產率高,立體選擇性中等到優良(方案3,6a?6i)。苯甲醛以77%的收率得到目標產物6b,Z選擇性高(C3、?、C4)。含電子給體(-OMe,6c)或吸電子基團(-NO2,6d)的芳香醛與硼酸烯丙酯3a反應平穩,產率分別為78%和77%。當使用4-甲氧基苯甲醛時,Z/E選擇性較低(約8:1)。在標準反應條件下,芳環上的溴取代基具有較好的耐受性,為其進一步改性(6E,70%)提供了更多的機會。與芳醛相比,脂肪醛(如丙醛)與烯丙基硼酸酯3a反應得到的產物6f的產率為85%,具有良好的非對映選擇性,但Z/E(C3?C4)較低(3:1)。α,β-不飽和醛得到相應的乙酰化3,5-二烯基高烯丙醇(6g,6h),產率分別為71%和56%。與醛不同,烯丙基硼酸酯與酮的加成要慢得多。用CF3取代的炔基酮作為烯丙化基團,無需乙酰化即可合成3,5-二烯基高烯丙醇6I,收率38%,Z/E(C3,?,C4)比為10:1。
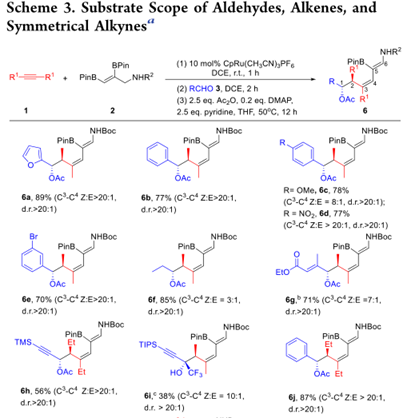
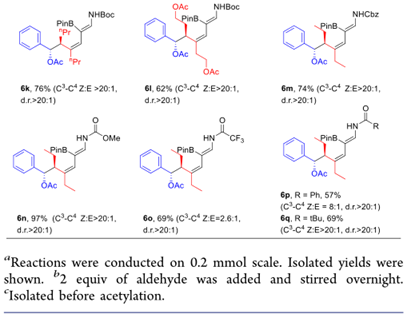
接下來,作者進一步的工藝優化反應條件以各種炔烴和烯烴(方案3,6J - 6Q)。對稱炔烴,包括3-己炔,4-辛炔和-3-炔-1,6-二乙酸己酯,都以87%,77%和62%的比例提供了相應的1,3-二烯產物6j - 6l, 分別。這些結果表明,釕催化的烯烴-炔烴偶聯反應取決于炔烴的空間位阻。此外,具有不同保護基團的2,3-二硼烷基烯丙基胺(包括芐氧羰基,甲氧羰基,三氟乙酰基,苯甲酰基和新戊酰基)與3-己炔和苯甲醛平滑反應,得到相應的產物6m - 6q產量中等至良好。特別是,較小的空間位氨基甲酸甲酯會與炔烴產生最佳偶聯反應性(6n,97%)。當使用三氟乙酰基保護的2,3-二硼烷基烯丙基胺時,C 3 -C 4雙鍵的Z:E比降低至2.6:1(6o,69%)。
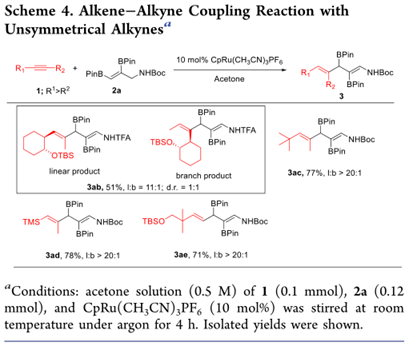
當使用非對稱炔烴作為底物時,烯烴-炔烴偶聯的區域選擇性成為一個主要問題(方案4)。發現在R1和R2的尺寸完全不同的情況下可以獲得優異的區域選擇性。使用N- TFA保護的二硼烷基烯丙基胺與叔丁基二甲基((2-(丙-1-炔-1-基)環己基)氧基)硅烷偶合,得到11:1的線性至分支區域選擇性。與在DCE中相比,在丙酮中可以獲得更好的線性區域選擇性。炔烴上空間更龐大的基團(例如叔丁基和三甲基甲硅烷基)可提高區域選擇性(3ac,77%,3ad,78%)。與末端炔烴的反應產生線性異構體,其為主要產物,產率為71%(3ae)。
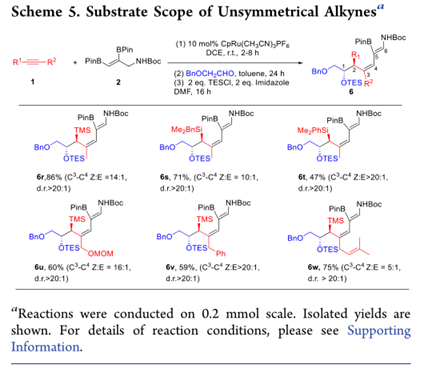
接下來,作者在釕催化的烯烴-炔烴偶聯反應中測試了各種甲硅烷基取代的不對稱炔烴(方案5)。不僅三甲基甲硅烷基取代的丙炔,而且叔丁基二甲基甲硅烷基和二甲基苯基甲硅烷基丙炔也分別以71%和47%的產率得到相應的產物6s和6t。甲氧基甲基保護的3-(三甲基甲硅烷基)丙-2-炔-1-醇以60%的收率,以16:1 Z:E(C3–C4)選擇性提供所需的產物6u。也可以容許芐基和烯丙基取代的甲硅烷基乙炔生成相應的1,3-二烯(6v和6w)的產率分別為59%和75%。
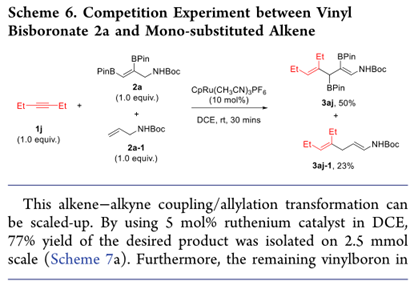
為了證明硼烷基取代基對烯烴的活化作用,進行了雙硼酸酯乙烯基2a與叔丁基烯丙基氨基甲酸酯(2a-1)的競爭實驗(方案6)。有趣的是,雙硼酸乙烯基酯2a與3-己炔的反應性更好,產物3aj的收率為50%,而單取代烯烴2a-1的收率為23%。結果清楚地表明,硼烷基取代基可以促進這種Ru催化的烯烴-炔烴偶聯反應。
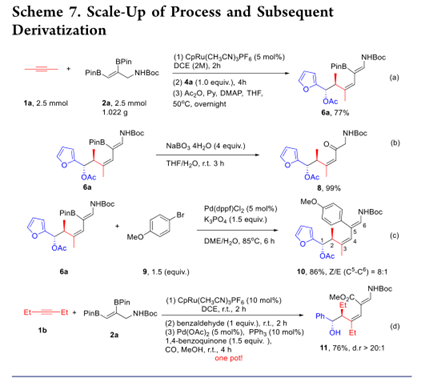
這種烯烴-炔烴偶聯/烯丙基化轉化可以按比例放大。通過在DCE中使用5mol%的釕催化劑,以2.5mmol規模分離出77%的所需產物(方案7a)。此外,均丙醇產物中剩余的乙烯基硼可以用作隨后合成衍生化的通用工具。硼酸乙烯基酯6a被過硼酸鈉氧化,以優異的產率提供抗 -δ-羥基α,β-不飽和酮8(方案 7b)。此外,硼酸乙烯基酯與芳族溴化物的交叉偶聯是通過添加鈀催化劑和化學計量的堿實現的。生產芳基化產物時,C5–C6雙鍵的幾何結構略有損失(方案7 c,86%,C5–C6上的Z / E = 8:1)。(26)也可以按一鍋法順序進行烯烴-炔烴偶聯/烯丙基化/氧化羧化反應(方案7 d)。(27)分離出相應的抗-δ-羥基乙烯基酯11,產率為76%。
https://doi.org/10.1021/jacs.0c01755








