分享一篇發表在JACS上的文章,題目為“Ketoboronate as a Minimal Covalent-Reversible Tag for Targeted Lysosomal Degradation of Extracellular and Membrane Proteins”。通訊作者為伊利諾伊大學芝加哥分校的Alexander Adibekian教授,其研究方向為化學蛋白質組學和藥物發現。

溶酶體靶向嵌合體(LYTAC)和類似技術的發展為細胞表面或細胞外蛋白的靶向降解提供了前所未有的機會,然而,目前該類技術多數使用分子量較大的糖肽或糖聚合物來結合細胞表面效應器(如M6PR等,最近也有使用蛋白binder靶向轉鐵蛋白受體(TfR)實現溶酶體降解的報道),這使相關制劑的合成易得性、穩定性和免疫原性均面臨較大的挑戰。相反地,尋找一種“最小降解標簽”則有望拓展這類溶酶體靶向蛋白降解技術的適用性。
作者早期曾致力于開發一類硫醇介導的細胞攝取方法,例如,通過蘆筍酸(AspA)環狀二硫鍵與半胱氨酸殘基間的交換反應,可將肽、蛋白或成像試劑等“貨物”共價連接到細胞表面的關鍵受體上,從而實現貨物的遞送。然而,細胞表面活性半胱氨酸的數量稀少,相比之下,賴氨酸殘基則更為豐富。本文中,作者受到一種賴氨酸修飾反應的啟發:酮硼酸類化合物可與賴氨酸側鏈氨基形成席夫堿形式的可逆共價鍵,利用這一反應,或可實現“胺介導的攝取(amine-mediated uptake)”。
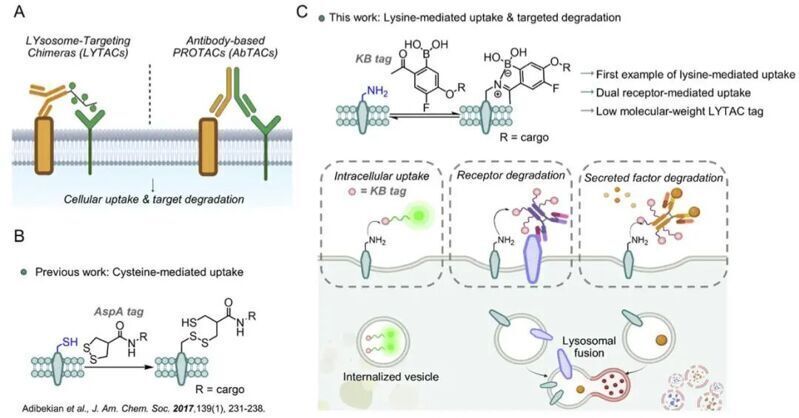
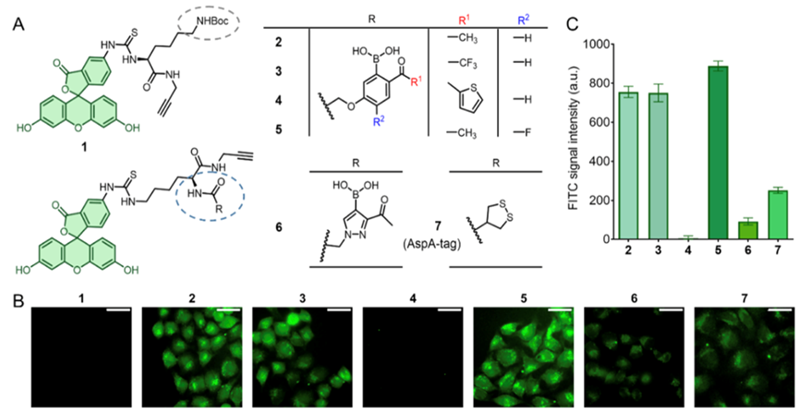
由此出發,作者以熒光素為模型“貨物”,開發并測試了這種攝取策略。作者在熒光素上偶聯了一系列苯基硼酸結構片段,其中硼酸基鄰、對位的取代基均嘗試了不同的候選。細胞成像結果表明,化合物5具有最強的細胞攝取能力,且強于基于蘆筍酸-硫醇攝取策略的對照化合物7。為了進一步證明這種細胞攝取作用是依賴于賴氨酸側鏈氨基的,作者使用廣譜賴氨酸反應性探針STP預封閉細胞表面的活性賴氨酸殘基,該處理阻斷了細胞對化合物5的攝取。上述結果初步證明了氨基介導的攝取這一策略的可行性。
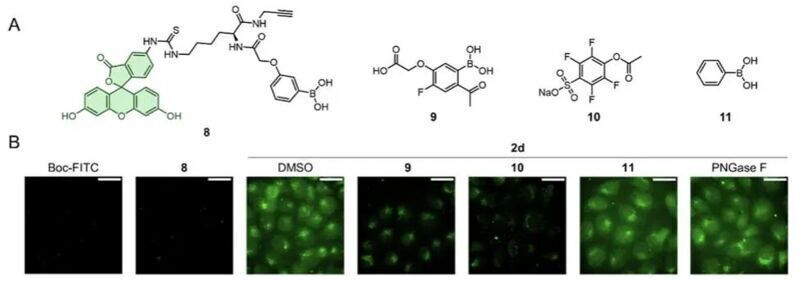
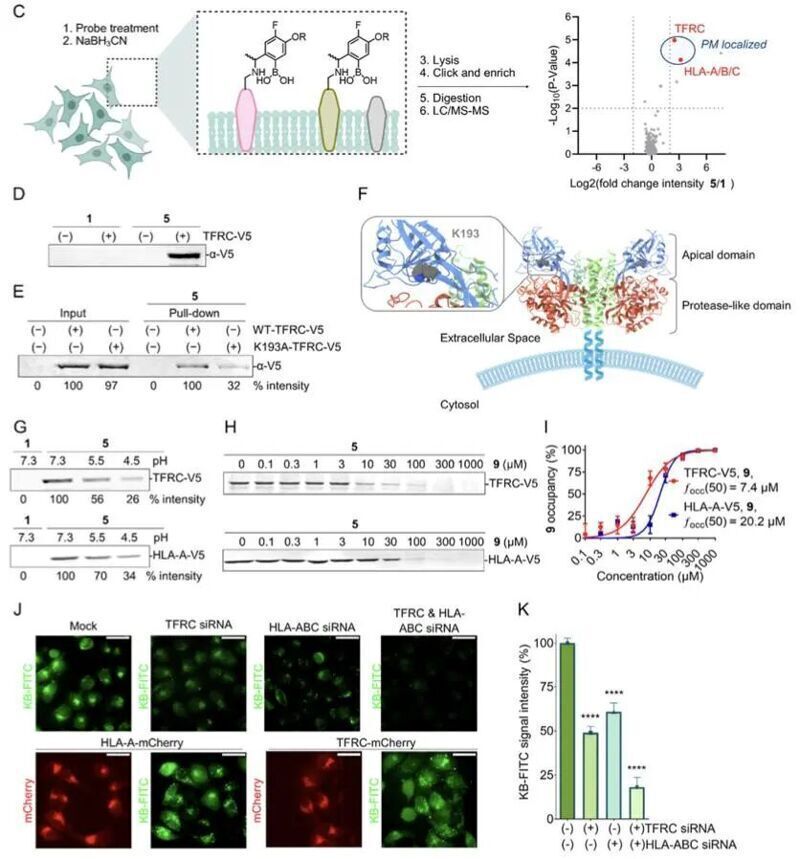
隨后,作者嘗試參與這一攝取過程的關鍵蛋白效應器。通過NaBH3CN還原處理,作者將以可逆共價鍵連接在細胞表面的炔基探針轉化為不可逆共價連接,隨后通過化學蛋白質組學分析鑒定其共價標記的蛋白。結果顯示,探針強烈地富集了兩種質膜蛋白:TFRC和HLA-ABC。隨后的機制驗證表明,關鍵賴氨酸殘基的突變將顯著減少探針對TFRC的標記,此外,TFRC和HLA-ABC的單獨或共同敲低都將破壞細胞對探針的攝取,支持了這兩種質膜蛋白在酮硼酸類探針攝取中的關鍵作用。作者也展示了酮硼酸-氨基可逆共價連接的關鍵優勢:所形成的亞胺硼酸鍵是酸不穩定的,可以在低pH下斷開并釋放出“貨物”。
最后,作者為這種策略尋找了巧妙的應用場景:可將酮硼酸作為一種溶酶體靶向標簽,實現細胞表面/細胞外蛋白的內化和降解。作者以胞外鏈霉親和素為模型成功驗證了這一設計,隨后嘗試了廣泛的應用,包括EGFR、HER2和VEGFA的溶酶體靶向降解。以HER2為例,作者通過SPAAC反應將酮硼酸標簽偶聯到曲妥珠單抗上,在細胞和荷瘤小鼠模型上均實現了強效的HER2降解。
總結而言,作者開發了一種基于酮硼酸-氨基反應的細胞攝取策略,并以酮硼酸作為“最小降解標簽”,實現了多種蛋白的溶酶體靶向降解。
本文作者:TYC
責任編輯:WYQ
DOI:10.1021/jacs.5c16611
原文鏈接:https://doi.org/10.1021/jacs.5c16611








