中國科學院上海有機化學研究所劉文課題組以 35 元大環硫肽類抗生素 sulfomycins為研究對象,發現了一個非線性的兩階段過程能完成了分子中五個唑類雜環的引入,該工作發表在J. Am. Chem. Soc.上(都亞男, JACS, 2020, 142, 18, 8454-8463)。

硫肽類抗生素是一類由微生物次級代謝產生的聚肽類天然產物,大多具有良好的抗革蘭氏陽性菌以及抗腫瘤活性。近年來,研究人員發現人體共生微生物也能夠產生硫肽分子,也就意味著硫肽類抗生素的生物合成可能直接影響共生細菌與人體的互作關系,對維持人體健康有利,因此對于新藥開發具有重要的導向意義。生物合成研究揭示該類分子由核糖體合成并經過翻譯后修飾得到,其核心骨架大環的構筑過程涉及到三個關鍵的翻譯后修飾反應,即環化脫水/脫氫(形成唑類五元雜環)、絲氨酸/蘇氨酸脫水(形成脫水氨基酸)以及雜原子[4 + 2]環加成反應(核心骨架大環的大環化)。鑒于該類天然產物具有復雜的分子結構,其往往難以通過化學全合成得到。因此,對于硫肽類抗生素的生物合成研究將有助于這類化合物的深度開發和利用。
早期人們對于硫肽類抗生素中唑類雜環的認知主要來自于對 26 元和 29 元大環硫肽類抗生素的研究。劉文課題組長期以來致力于硫肽類抗生素的生物合成研究(Nat. Prod. Rep. 2013, 30, 218–226; Curr. Opin. Chem. Biol. 2013, 17, 626-634; Org. Biomol. Chem. 2017, 15, 3376–3390; Curr. Opin. Biotechnol. 2017, 48, 210–219)。近日,他們以 35 元大環硫肽類抗生素 sulfomycins為研究對象,發現了一個非線性的兩階段過程能完成了分子中五個唑類雜環的引入,該工作發表在J. Am. Chem. Soc.上(都亞男, JACS, 2020, 142, 18, 8454-8463)。
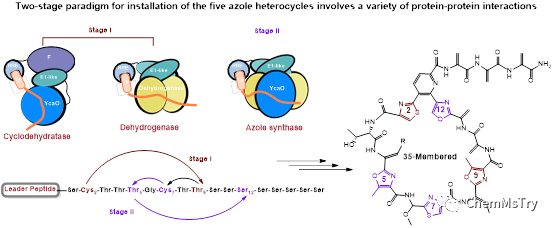
在第一階段中,由雙結構域E1-YcaO蛋白和F伴侶蛋白組成的典型環化脫水酶復合物,將兩個相距較遠的殘基(l-Cys2和l-Thr9)雜環化,隨后異源三聚體脫氫酶再將所得的唑啉轉化為唑。在第二階段中,脫氫酶三聚體與另一個離散的YcaO蛋白結合形成非典型的四組分唑類合成酶復合物,該復合物依次將余下三個殘基l-Cys7、l-Thr5和l-Ser12轉化為唑。E1伴侶蛋白在兩個階段中均起著至關重要的作用,它介導了各種特定的蛋白-蛋白相互作用。這項研究加深了我們對于含唑類核糖體肽生物合成的理解,同時對聚唑形成的翻譯后修飾邏輯研究具有重要意義。四組分唑類合成酶復合物常見于35 元大環硫肽類抗生素,因此該研究成果將有助于利用基因組挖掘和合成生物學方法的發現、改造以及新硫肽的創建。