ZK作者/ 生物醫藥工程智庫
編輯/ ZK主創們
概述
有機物分子結構中的碳,氮、 氧或硫等原子上導入酰基的反應稱為酰化反應,酰化反應的產物分別是酮 (醛),酰胺, 酯或硫醇酯。
酰基是指含氧無機酸、 有機酸或磺酸的分子結構中去掉羥基后所剩的部分,這里主要討論的是導入有機酸酰基的酰化反應。
酰化反應在藥物合成中有著廣泛的應用。 首先, 酰基是某些藥物重要的藥效基團,在許多藥物結構中含有酰基。
此外,酰基也是藥物合成中官能團轉換的重要合成手段,酰基可通過氧化、 還原、 加成、 重排成肟等反應轉化成其他基團, 另外,在涉及羥基、 氨基、 巰基等基團保護時, 將其酰化也是一個常見的保護方法。
酰化反應機理
按酰基的導入方式可將酰化反應分為直接酰化和間接酰化; 按酰基的導入位置可將酰化分為氧原子上的酰化、 氮原子上的酰化和碳原子上的酰化.。氧、 氮原子上的酰化一般均為直接酰化反應,而碳原子上的酰化既有直接酰化, 又有間接酰化反應。
一、電子反應機理
1、親電反應機理
在氧、 氮和碳原子上的絕大部分酰化反應都屬于親電酰化, 這是因為在通常反應條件下, 羰基的 C原子顯部分正電性。 由于酰化劑種類和酰化能力的強弱不同,又可將酰化反應歷程分為單分子歷程和雙分子歷程。
(1)單分子歷程
酰化劑在催化劑的作用下解離出酰基正離子(1),再與被酰化物發生親電取代反應,生成酰化產物 (2),其中酰化劑解離過程是反應的限速步驟,酰化速率僅與酰化劑的濃度相關。
采用酰鹵、酸酐等強酰化劑的酰化反應趨向于按單分子歷程進行。
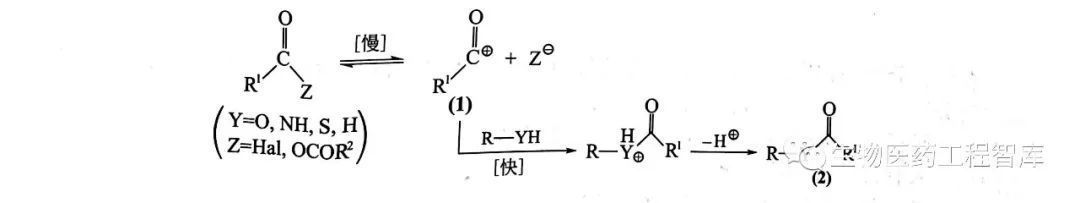
(2) 雙分子歷程
酰化劑的羰基與被酰化物結構中的羥基, 氨基間進行親電反應, 生成中間過渡態 (3),此步是反應的限速步驟。(3) 再解離出離去基團 Z負離子, 脫去質子生成酰化產物(2)。另外一種可能的機理是被酰化物與酰化劑羰基加成生成四面體過渡態 (4), 再脫去 z負離子, 脫去質子生成酰化產物(2)。 雙分子歷程中酰化速率與酰化劑和被酰化物的濃度都相關,為動力學上的二級反應。
一般采用羧酸、羧酸酯和酰胺等為酰化劑的酰化反應趨向于按雙分子歷程進行。
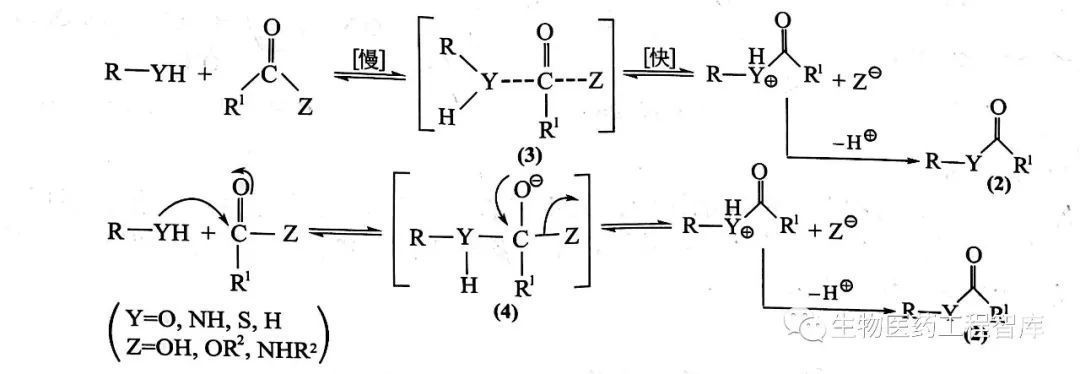
(3) 酰化劑的強弱順序
酰化劑的酰化能力與離去基團Z的電負性和離去能力有關,Z的電負性越大,離去能力越大, 其酰化能力越強 。Z的離去能力可通過其共軛酸HZ的酸性強弱來判斷,而判斷 HZ酸性強弱的最直接的方法是 HZ的pKa值。
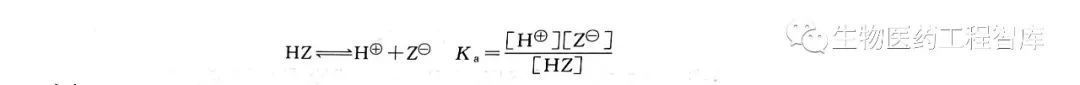
式中,Ka為HZ的電離平衡常數,也稱為酸解離常數,而pKa=一lgKa,所以Ka或pKa的數值反映出酸性的強弱,K.越大或 pKa越小,酸性越強。 常見的酰化劑的活性順序為:
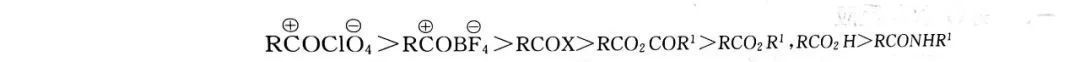
上述強弱順序不是絕對的,例如,某些活性酯或活性酰胺則為強酰化劑。
(4)被酰化物的活性
被酰化物的親核能力越強,越容易被酰化,活性大小可以用被酰化物R一YH 的堿性來衡量, 其堿性越強, 越容易被酰化。當被酰化物結構中的R相同時: RNH2>ROH>RH。
被酰化物結構中的R基團對其酰化的難易也有影響,就O-酰化和N-酰化而言,R為芳基時,由于芳基與N原子或O原子間的共軛效應,使N原子或O原子上的電子云密度降低而反應活性下降,所以RNH2>ArNH2;ROH>ArOH。另外,R基團的立體位阻對其活性也有影響,立體位阻大的醇或胺的酰化要相對困難一些,一般選用活性較強的酰化劑。
2、C-親核反應機理
在通常的反應條件下,羰基的碳原子均顯部分正電性,因此從酰化劑的角度來講, 所參與的酰化反應都應為親電酰化, 但在某些特定的條件下,可通過“極性反轉” 的方法將其轉變成具有親核性的羰基,從而可以與某些具有親電性的被酰化物之間發生親核性的酰化反應, 例如,通過醛與活潑金屬作用, 將其羰基轉化成酰基負離子中間體。
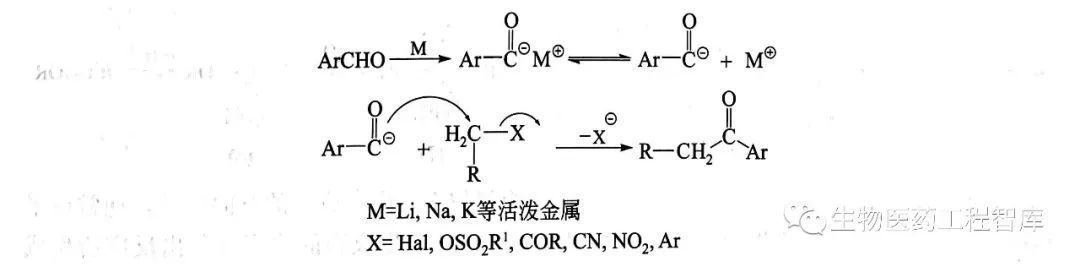
親核性的酰化反應通常發生C-酰化中,通過該反應可以制備不對稱酮、1,2-二酮等化合物。
References:
[1]《藥物合成反應》
以上內容為博普智庫收集整理








