Simon J. Meek團隊曾經報道過(CDC)-Rh-絡合物促進的,N-雜芳烴與末端或內部1,3二烯的位點和對映選擇性反應(Scheme 1A),但是反應底物僅限與親核的芳烴。之后,中國科學院上海有機化學研究所的梅天勝研究員和南開大學周其林教授分別使用N,N和N,P雙齒配體,實現了對映選擇性轉化(Scheme 1B),但是這些反應的底物范圍非常有限,并且產物的對映選擇性較低
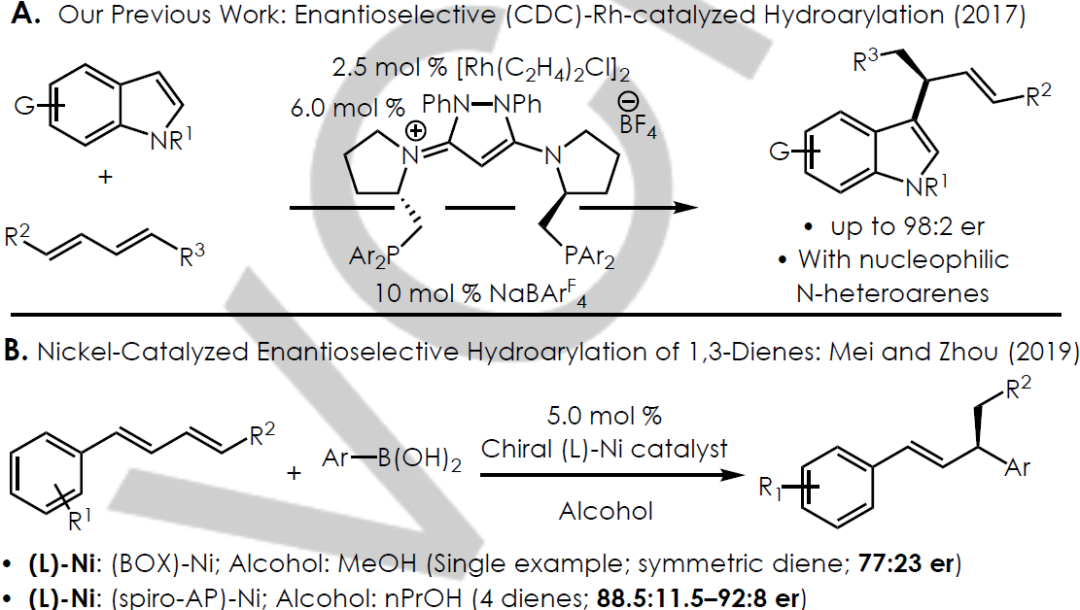
近期,美國北卡羅來納大學教堂山分校化學系Simon J. Meek等人報道了一種高效的Ni-催化對映選擇性加氫芳基化反應,該反應的較好的官能團容忍性,能夠合成大量手性芳烴。相關成果發表在Angew. Chem. Int. Ed.。

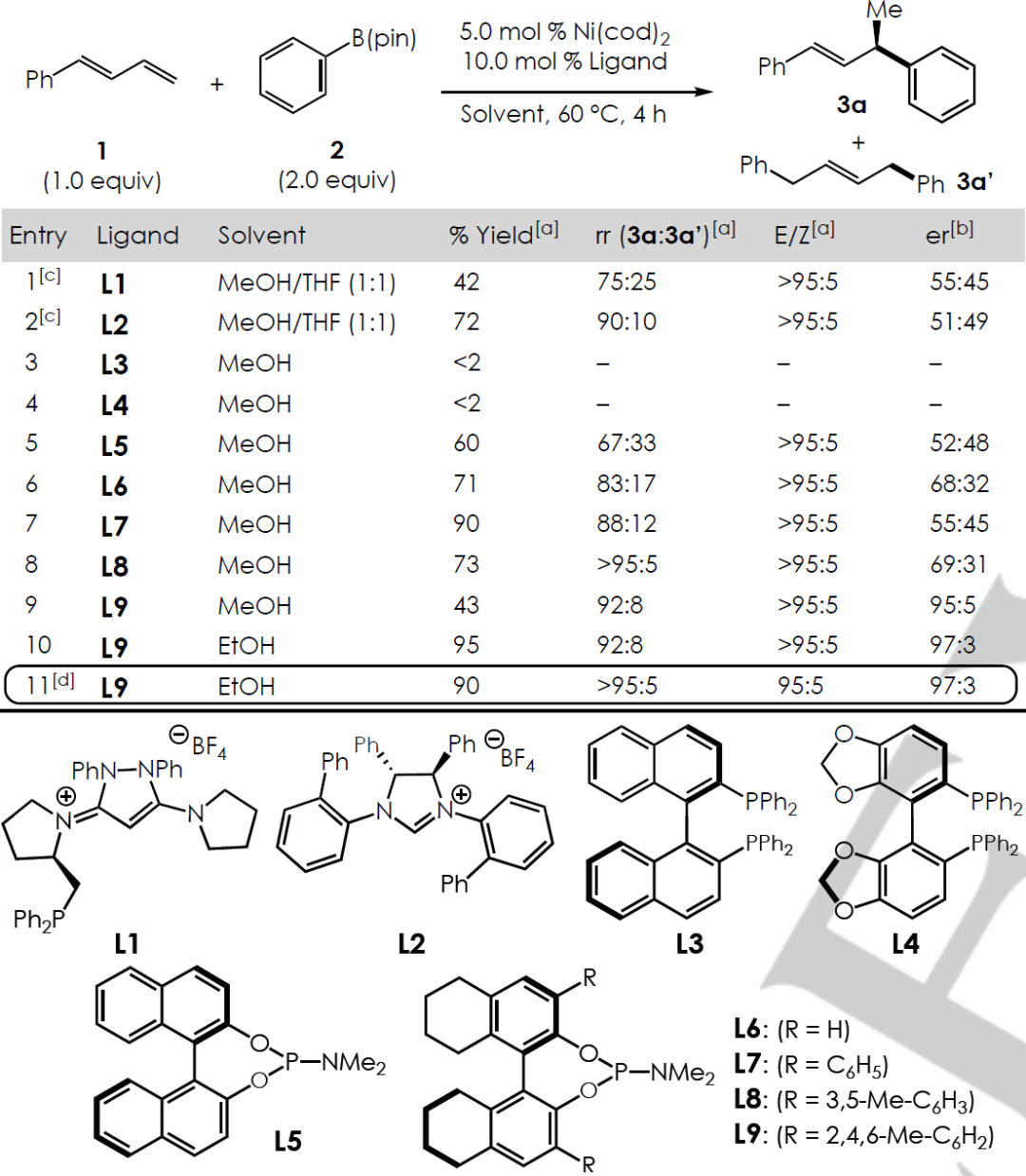
作者首先以苯基丁烷-1,3-二烯和苯基-B(pin)為底物,以5.0 mol % Ni(cod)2為催化劑,MeOH為溶劑,反應溫度為40℃,篩選最佳的配體(Table 1)。碳二卡賓配體(L1)和氮雜卡賓配體(L2)的對映選擇性較低,但是L2較L1的位置選擇性高。而雙齒磷配體(L3-L4)產率較低而難以用于反應(﹤2%)。相反,單齒亞磷酰胺配體(L5-L6)提高了反應的對映選擇性和位點選擇性,作者通過在配體L6二醇主鏈上引入3,3’-a芳香基團(L7-L9),發現空間位阻較大的配體L9的rr和對映選擇性都得到了進一步提高,但是產率相應的降低。最后作者以乙醇為溶劑,發現[Ni(C3H5)Br]2和KOtBu組合,反應的位點選擇性和對映選擇性最優。
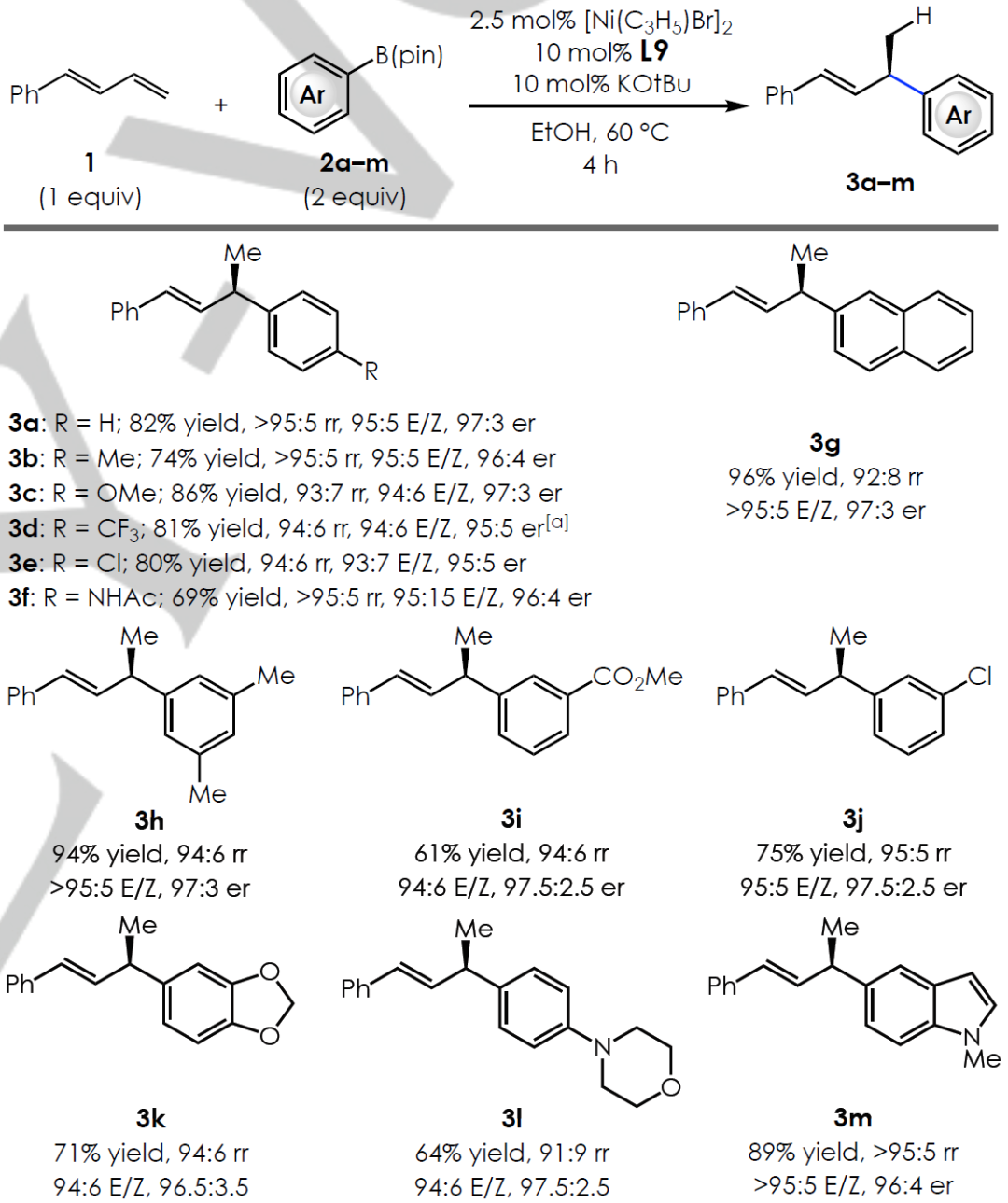
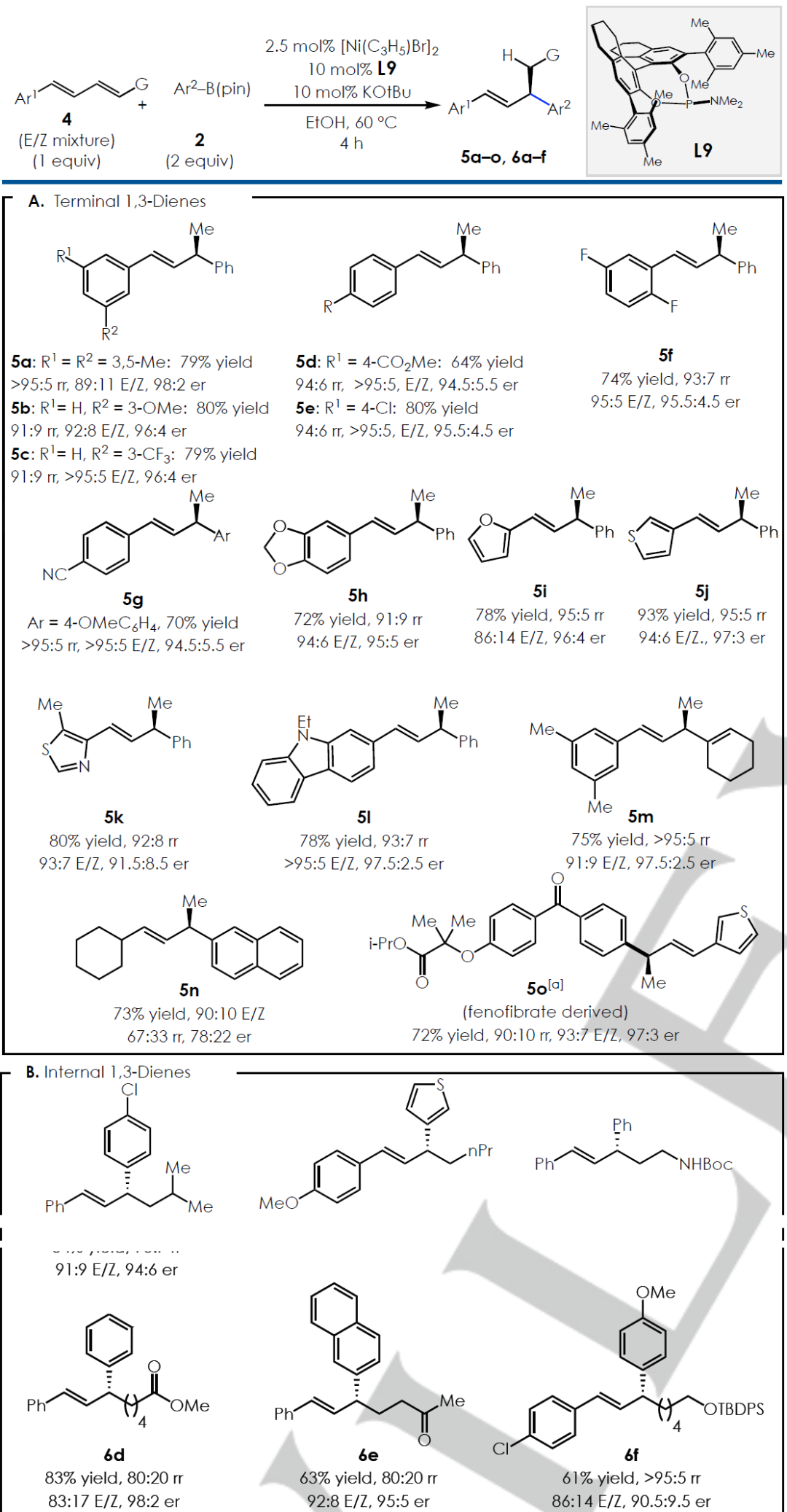
作者之后又探究了1,3-二烯類化合物的底物適應范圍(Scheme 3)。在各個位置上具有吸電子基(5a, h, m)或供電子基(5b–g)取代芳基1,3-二烯均能以高于>95:5 rr和99:1 er.得到烯丙基取代的芳烴(Scheme 3A)。并且,1,3-二烯的E/Z混合異構體也能以較高的催化效率,位點,對映選擇性得到相應的產物。芳雜芳烴取代的二烯(5i-5l),環己烯基取代的二烯(5m),生物活性分子(5O)均能以較高的效率和對映選擇性實現轉化。 對于1,4-二取代的二烯烴的底物(Scheme 3B),由于Ni催化劑需要區分1位和4位,因此另一取代基的存在使反應的位點選擇性更為困難。含有烷基(6a–b),烯丙基NBoc氨基甲酸酯(6c),酯(6d),酮(6e)和甲硅烷基醚(6f)基的部分1,4-二取代的二烯烴底物具有較高容忍性和較高的對映選擇性,但6d和6e的rr值相對較低。
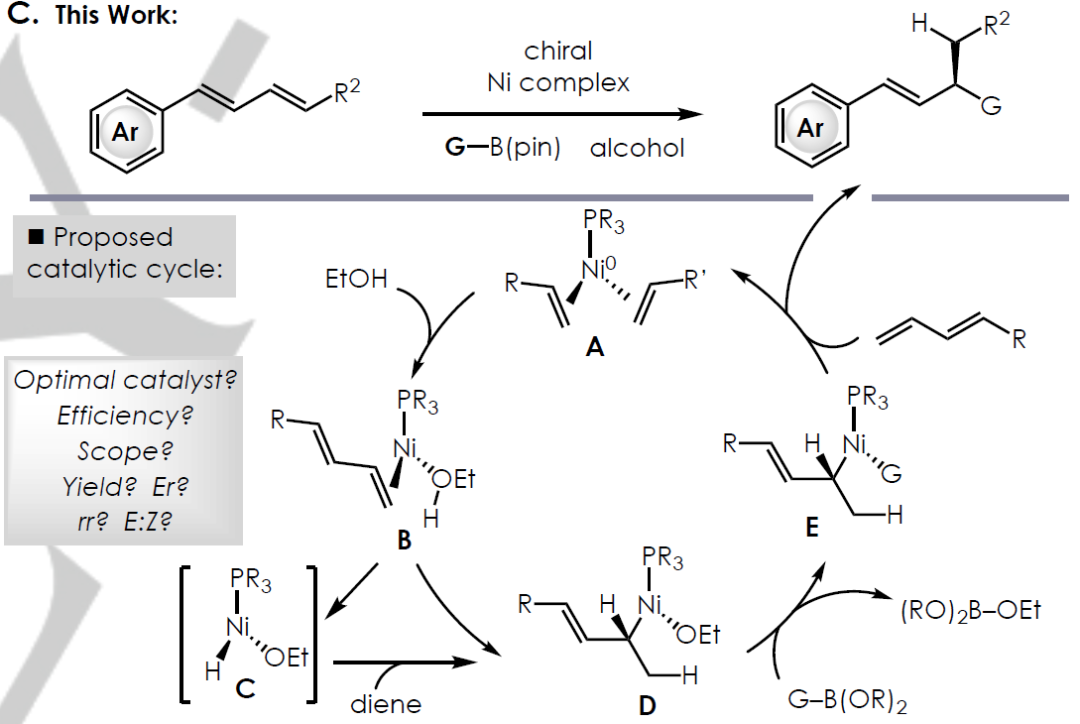
在研究機理的時候作者提出以下幾個問題:(1) 鎳催化劑在加氫芳基化之前是否使E/Z二烯混合物異構化;(2) 如果反應是在氘代醇中進行的,則在哪個位置(如果有)摻入了氘?(3) 硼試劑的結構是否影響反應的選擇性?
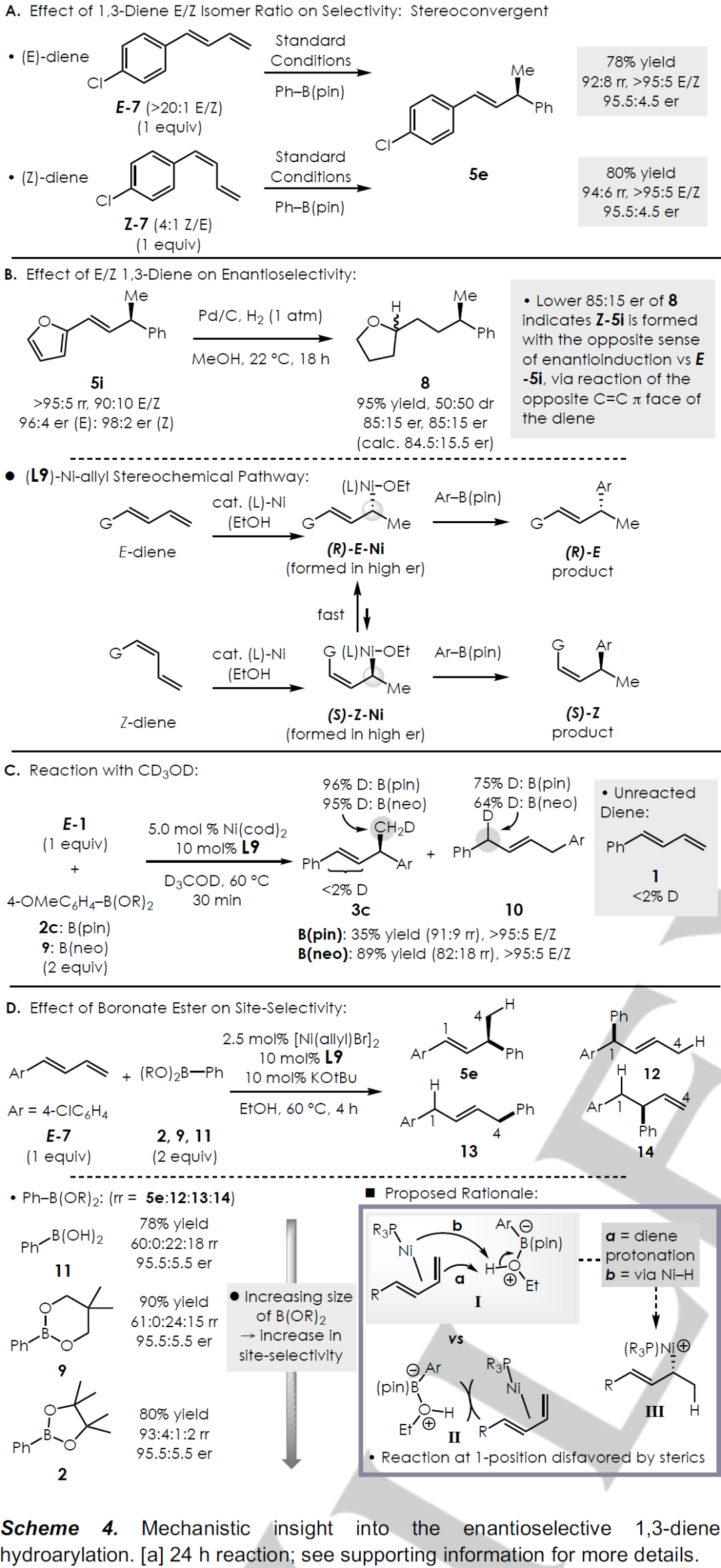
小結:Simon J. Meek課題組報道了通過Ni催化1,3-二烯的對映選擇性加氫芳基化反應生成官能化的芳烴的反應。該反應對鹵化芳烴,雜環,路易斯堿等官能團具有較好的容忍性。反應是通過E/Z立體匯聚(stereoconvergent)的對映選擇性過程進行的,該過程受芳基硼酸酯的影響。
相關文獻推薦:
1、梅天勝課題組(2019):Nickel-catalyzed EnantioselectiveHydroarylation andHydroalkenylation of Styrenes. J. Am. Chem. Soc. 2016, 138, 9, 2957-2960. https://pubs.acs.org/doi/abs/10.1021/jacs.6b00024
2、周其林課題組(2019):Ligand-Enabled Ni-Catalyzed Enantioselective Hydroarylation of Styrenes and 1,3-Dienes with Arylboronic Acids. CCS Chem. 2019, 1, 328–334.
https://www.chinesechemsoc.org/doi/pdf/10.31635/ccschem.019.20190026








