第一作者:趙心茹,鄭紅順
通訊作者:孫華傳,柳清菊
通訊單位:云南大學
氫能作為一種高能量密度,高燃燒熱值的清潔能源,正逐步成為全球能源轉型發展的重要載體之一。在各種制氫技術中,堿性電解水因技術成熟、工藝簡便而備受關注,現已成為制備綠氫的主要途徑之一。然而,堿性電催化析氫反應(HER)需要額外的水解離過程形成氫氧根離子和吸附氫(H*),隨后解吸生成H2。貴金屬Pt位于火山圖的頂端,因此具備優異的HER催化活性,但由于Pt-H鍵的結合能略高,導致其在堿性條件下反應動力學相對緩慢。此外,陽極析氧反應(OER)涉及多步質子耦合電子轉移過程,需要克服較大能壘,嚴重制約制氫效率。相比之下,采用熱力學電位更低的陽極肼氧化反應(HzOR,N2H4+ 4OH– → N2 + 4H2O + 4e–, ?0.33 V vs. RHE)替代OER可大幅降低電解水制氫所需的電壓。然而,HER和HzOR反應對金屬活性中心要求各異,因此設計能同時驅動HER和HzOR的雙功能催化劑具有挑戰性。據現有文獻報道,鎳鉬基氧化物作為典型的HER電催化劑,可同時應用于HzOR過程。然而,其在安培級電流密度下的催化性能有待進一步提升。因此,對NiMoO4進行改性,以開發出高效的HER/HzOR雙功能催化劑具有重要意義。
近期,云南大學柳清菊教授團隊結合水熱法和N2退火策略成功將Pt顆粒與富氧空位NiMoO4耦合,從而制備出類銀柳花狀異質結構電催化劑,即Pt@NMO-N2(圖1)。精細結構表征和理論計算結果表明,Pt@NMO-N2催化劑在異質界面處形成了內建電場(BEF),從而使電子從富氧空位載體(NMO-N2)向Pt顆粒發生轉移,富電子的Pt物種顯著促進了HER過程中氫中間體(H*)的吸附和解吸。同時,界面組分耦合協同效應導致Pt@NMO-N2的d帶中心(εd)下移,從而促進了HzOR過程中從*NH4到*NH3的脫氫過程。此外,原位電化學測試結果表明異質界面處局域電場的形成有效促進了界面水的解離,顯著增強了HER反應動力學。基于此,該催化劑在堿性淡水/海水電解析氫過程中,分別僅需149 mV和180 mV的過電位即可實現1000 mA cm-2的電流密度。值得注意的是,Pt@NMO-N2在HzOR過程中也只需0.12 V的工作電壓即可達到相同電流密度。與此同時,在肼氧化輔助制氫體系中,Pt@NMO-N2(+) || Pt@NMO-N2 (-) 電解槽僅需0.32 V的低電壓即可實現500 mA cm-2電流密度,優于目前報道的大部分催化體系。將自支撐Pt@NMO-N2催化劑作為陰極應用于陰離子交換膜(AEM)電解槽,其僅需1.77 V就能達到 500 mA cm-2電流密度(工作溫度T = 60 ℃)。這項工作為雙功能鎳鉬基電催化劑的可控合成以實現低能耗電解水產氫提供了新的見解。該研究以“Interfacial Component Coupling Effects Induce Electron Redistribution for Enhanced Hydrazine‐Assisted Hydrogen Production at Ampere-Level Current Densities”為題發表在國際知名期刊Nano Energy上。
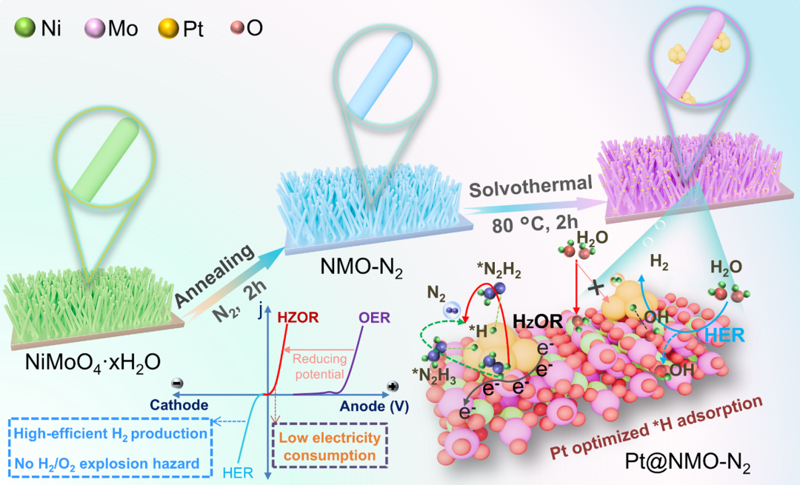
圖 1. Pt@NMO-N2的合成路線示意圖
要點一:本研究首先通過水熱法合成NiMoO4·xH2O/NF前驅體。隨后,將NiMoO4·xH2O/NF置于N2氣氛中退火得到富氧空位的 NMO-N2納米線陣列。最后,采用溶劑熱法將Pt顆粒負載到NMO-N2納米線上,從而得到Pt@NMO-N2類銀柳花狀異質結構電催化劑。X射線衍射(XRD)和拉曼光譜證實了Pt@NMO-N2催化劑的成功制備(圖2a-b)。高分辨透射電子顯微鏡(HRTEM)與選區電子衍射(SAED)相結合揭示了異質結構Pt@NMO-N2中兩相共存的結構特征。得益于NMO-N2納米線陣列的大比表面積優勢,所構筑的三維多級納米陣列前體,有助于提高Pt納米顆粒的分散性和穩定性。
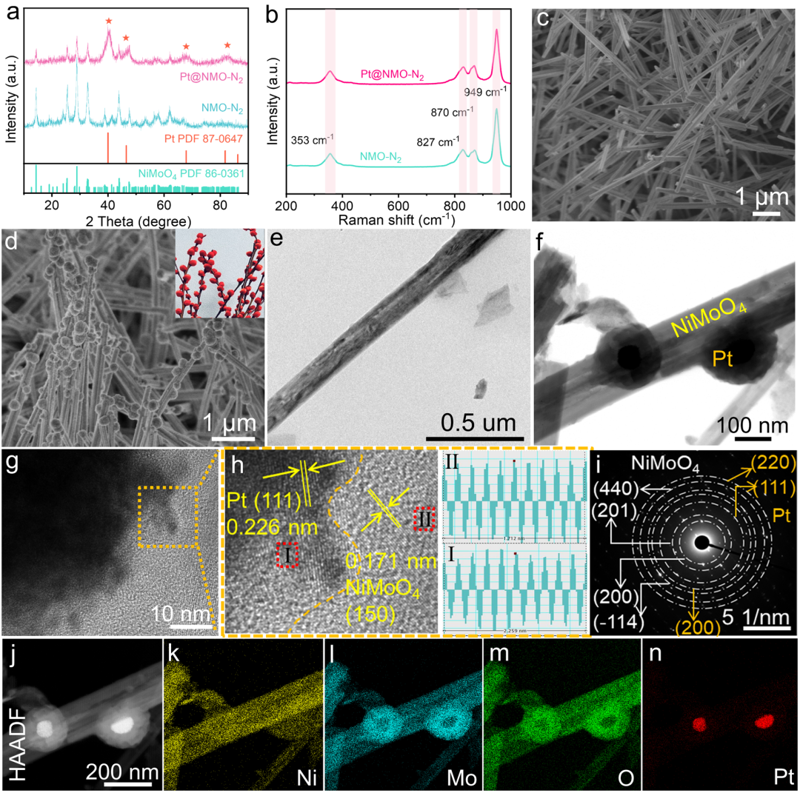
圖 2. 結構表征。(a, b) Pt@NMO-N2和NMO-N2的XRD和拉曼光譜;(c-f)NMO-N2和 Pt@NMO-N2的SEM和TEM圖像,(d)的右上角為銀柳花的形狀;(g、h)Pt@NMO-N2的HRTEM圖像;(i) SAED圖案;(j-n) Pt@NMO-N2的HAADF-STEM和STEM-EDS圖譜。
要點二:X射線光電子能譜(XPS)結果顯示,Pt@NMO-N2的Ni 2p,Mo 3d和O 1s的結合能相較于NMO-N2發生明顯偏移,這表明Pt顆粒與NMO-N2基體之間存在強烈的電子相互作用(圖2a-d)。此外,電子順磁共振(EPR)結果顯示,Pt@NMO-N2中氧空位(Ov)濃度明顯高于基體NMO-N2(圖2e)。金屬氧化物在催化過程中常常面臨著導電性差的問題,引入氧空位可以提高載流子濃度,從而改善材料的導電性。紫外光電子能譜(UPS)測試證明載體NMO-N2有著更低的功函數值(5.36 eV),NMO-N2和Pt之間的功函數差誘導界面處形成BEF(圖3g)。使電子由NMO-N2轉移到Pt,促進異質界面處電荷的重新分布,從而改善界面反應微環境,提高催化活性(圖3h)。進一步的接觸角和氣泡接觸角測試結果表明,Pt@NMO-N2電催化劑表現出超親水(接觸角為0°)和超疏氣特性(液下氣泡接觸角為153.2°)(圖2h-i)。二者協同優化電極表面的傳質能力,同時提供大量氣泡傳輸通道以加速催化過程中H2氣泡的快速脫附。
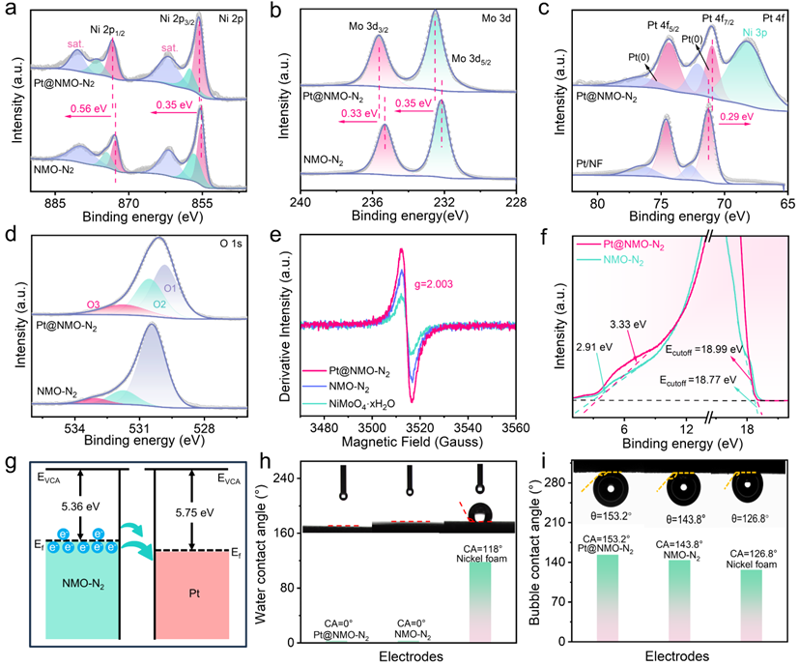
圖3. Pt@NMO-N2樣品的表面電子特性和接觸角。(a) Ni 2p、(b) Mo 3d、(c) Pt 4f 和 (d) O 1s 的 XPS 光譜;(f) NMO-N2和 Pt@NMO-N2的 UPS 光譜;(g) 電子轉移示意圖;(h) 接觸角;(i) 氣泡接觸角。
要點三:Pt@NMO-N2在堿性淡水中表現出優異的HER催化性能,分別僅需55、105和144 mV的過電位即可實現100、500、1000 mA cm-2的電流密度(圖3a, b)。此外,Pt@NMO-N2催化劑表現出較低的Tafel斜率和較低的電荷傳輸阻抗,以及快速的Bode相位角變化,證明Pt顆粒與氧空位的協同加速了水分解動力學,從而提升了HER催化活性(圖3c-g)。

圖4. 堿性淡水中的 HER 性能:(a、b)LSV曲線和不同電流密度下的過電位;(c) 塔菲爾斜率;(d) 催化劑的奈奎斯特圖;(e) Pt/C、(f) NMO-N2和(g) Pt@NMO-N2在不同應用電位下的原位Bode相圖;(h) Pt@NMO-N2與其他已報道的貴金屬基電催化劑催化活性的比較;(i)Pt@NMO-N2在堿性淡水中的計時電位測試(插圖:Pt@NMO-N2的穩定性測試后的SEM圖像以及1000次CV循環前后Pt@NMO-N2的LSV極化曲線)。
要點四:Pt@NMO-N2催化劑在堿性海水達到100、500和1000 mA cm-2的電流密度時分別僅需59、122和180 mV的過電位(圖5a-b)。在0.5、1.0和2.0 M NaCl的堿性溶液中,Pt@NMO-N2催化劑仍表現出較好的催化性能(圖5d,e)。這歸因于Pt@NMO-N2的超親水性和超疏氣特性,加速了生成的H2氣泡的脫附,減少了雜質離子在電極表面的沉積,從而實現堿性海水高效電解制氫。此外,Pt@NMO-N2電催化劑在500 mA cm-2電流密度條件下穩定運行200 h后,催化性能幾乎沒有衰減,且納米線結構特征基本保持,表明其穩定性較好(圖4g)。
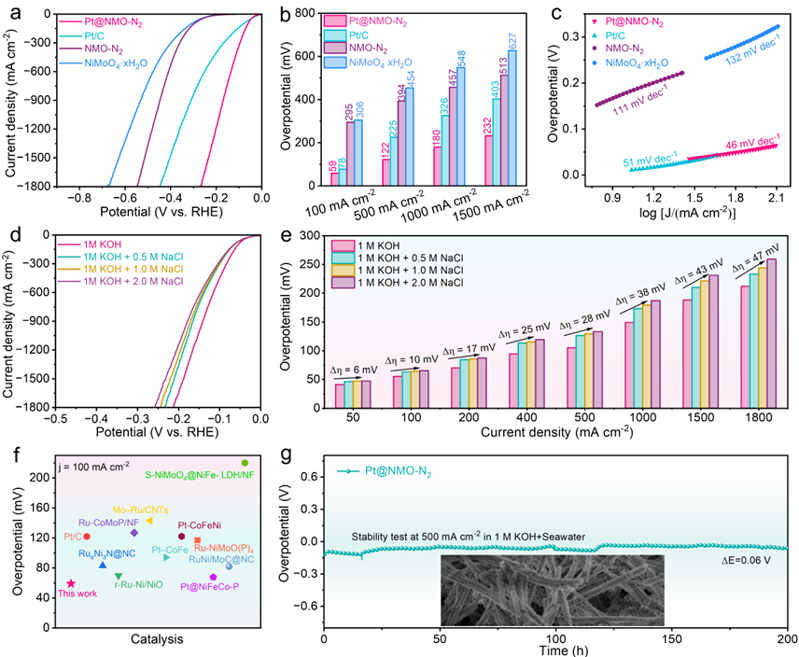
圖5.堿性海水中的 HER 性能測試:(a、b)堿性海水中不同電流密度下的 LSV 曲線和相應的過電位;(c) 塔菲爾斜率;(d, e) LSV 曲線和不同氯化鈉濃度的堿性溶液中不同電流密度下的過電位;(f) Pt@NMO-N2與其他已報道的電催化劑在堿性海水電解性能方面的比較;(g)Pt@NMO-N2的計時電位測試(插圖:Pt@NMO-N2在海水 HER 穩定性測試后的掃描電鏡圖像)。
要點五:構建了NiFe LDH (+) || Pt@NMO-N2 (–) 兩電極電解槽裝置進行全解水性能測試。如圖6a所示,該電解槽分別只需要1.64和1.73 V的電壓就能實現500和 1000 mA cm-2的電流密度,遠低于RuO2(+) || Pt/C (–)電解槽的驅動電壓(2.00 V@500 mA cm-2,2.27 V@1000 mA cm-2)。此外,NiFe LDH (+) || Pt@NMO-N2 (–) 系統可以在500 mA cm-2下穩定運行150h,表明其具有較好的穩定性(圖 6b)。進一步將自支撐Pt@NMO-N2和NiFe LDH催化劑分別作為陰極和陽極組裝陰離子交換膜水電解槽(AEMWE)模擬面向實際應用的電解水制氫,該電解槽達到 1 A cm-2電流密度僅需1.97 V電壓(T = 60 ℃),并且能夠在500 mA cm-2電流密度下穩定運行300 h (T = 25 ℃),彰顯了Pt@NMO-N2催化劑在高電流密度、長周期運行場景中的優異性能與商業化潛力。
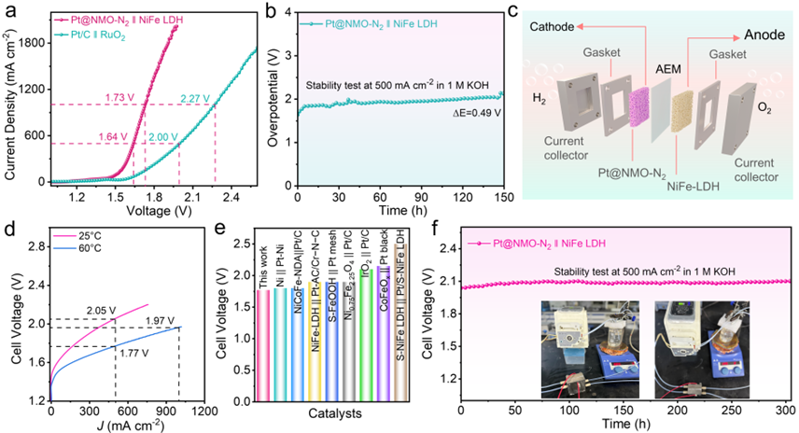
圖6.堿性淡水中的全電解水(OWS)性能測試:(a) LSV曲線;(b)穩定性測試;(c) AEMWE裝置示意圖,以及該AEMWE在堿性介質中產生H2的情況;(d) 使用Pt@NMO-N2作為陰極催化劑的AEMWE裝置在不同溫度下的極化曲線;(e) Pt@NMO-N2與其他已報道的電催化劑在AEMWE中的性能比較;(f)使用 Pt@NMO-N2作為陰極催化劑的AEMWE在500 mA cm-2下運行的計時電位計曲線(插圖:AEMWE器件的照片)。
要點六:如圖 7a 所示,自支撐Pt@NMO-N2表現出優異的HzOR性能,在電流密度為 10、100 和 500 mA cm-2 時,分別僅需–37、–21和36 mV的低工作電位。與陽極OER相比,Pt@NMO-N2 在100 mA cm-2時的HzOR工作電位降低了0.99 V。此外,Pt@NMO-N2(+) || Pt@ (–) 電解池只需要0.20 V的驅動電壓就能達到300 mA cm-2,性能明顯優于Pt/C (+) || Pt/C (–)電解池(0.51 V@300 mA cm-2)。圖7g顯示,傳統的全解水體受限于動力學緩慢的OER過程,需要高達1.93 V 的電壓才能實現500 mA cm-2電流密度,肼氧化輔助析氫體系(OHzS)只需要0.32 V即可達到相同的電流密度。這些結果表明,用陽極HzOR替代OER并與陰極HER相結合,是實現低能耗高效制氫的可行策略。
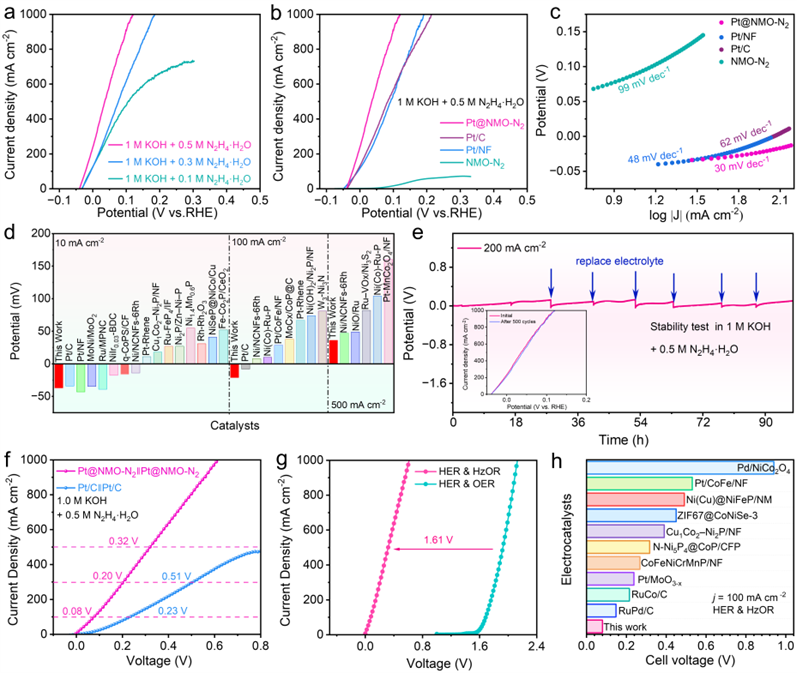
圖7. HzOR性能測試:(a) Pt@NMO-N2在不同濃度水合肼中的肼氧化LSV極化曲線;(b, c) Pt@NMO-N2、Pt/NF、NMO-N2和Pt/C催化劑的肼氧化性能及相應的塔菲爾圖;(d) Pt@NMO-N2與其他已報道的電催化劑在不同電流密度下的 HzOR性能比較;(e) Pt@NMO-N2的穩定性測試(插圖:Pt@NMO-N2在500個 CV循環前后的HzOR極化曲線);(f) 在雙電極系統中,Pt@NMO-N2的肼氧化偶聯制氫的LSV極化曲線;(g)Pt@NMO-N2電解槽全電解水制氫與肼氧化偶聯制氫的性能對比;(h) 不同催化劑組裝的電解槽在肼氧化輔助制氫中的性能對比。
要點七:原位拉曼測試結果表明,隨著電壓的增加,Pt@NMO-N2催化劑ν3(不活躍水分子的O-H懸掛鍵振動)強度相較于NMO-N2下降得更快。這表明異質界面處局部電場的形成促進了界面水的解離,從而增強了 HER 動力學,這與 Tafel 斜坡和原位Bode相角的結果相一致(圖8a-c)。進一步的理論計算結果表明,氧空位有效地調節了Pt@NMO-Ov的d帶中心( εd)。與無氧空位的Pt@NMO相比,Pt@NMO-Ov的εd離費米能級(Ef)更遠,表明更多的電子傾向于填充在反鍵軌道上,從而削弱了活性位點對反應物和反應中間產物的吸附。因此,富氧空位的Pt@NMO-N2能促進H*從活性位點快速解離(圖8f-g)。同時,Pt@NMO-Ov僅需要0.24 eV的低能壘就能使H-OH鍵斷裂,有效促進了水的解離(圖8h)。此外,氧空位顯著降低了Pt位點對H*的吸附,有效提升了Pt@NMO-N2的堿性HER性能(圖8i)。而圖8j結果顯示,Pt與Pt@NMO-Ov在HzOR過程中的速率決速步驟(RDS)均為為*NH4到*NH3的脫氫步驟,但Pt@NMO-Ov發生HzOR需克服的能壘更低,這歸因于氧空位和界面組分的協同效應顯著改善了反應中間體的吸附和解吸,從而提高了其在HzOR和HER過程中的催化活性。
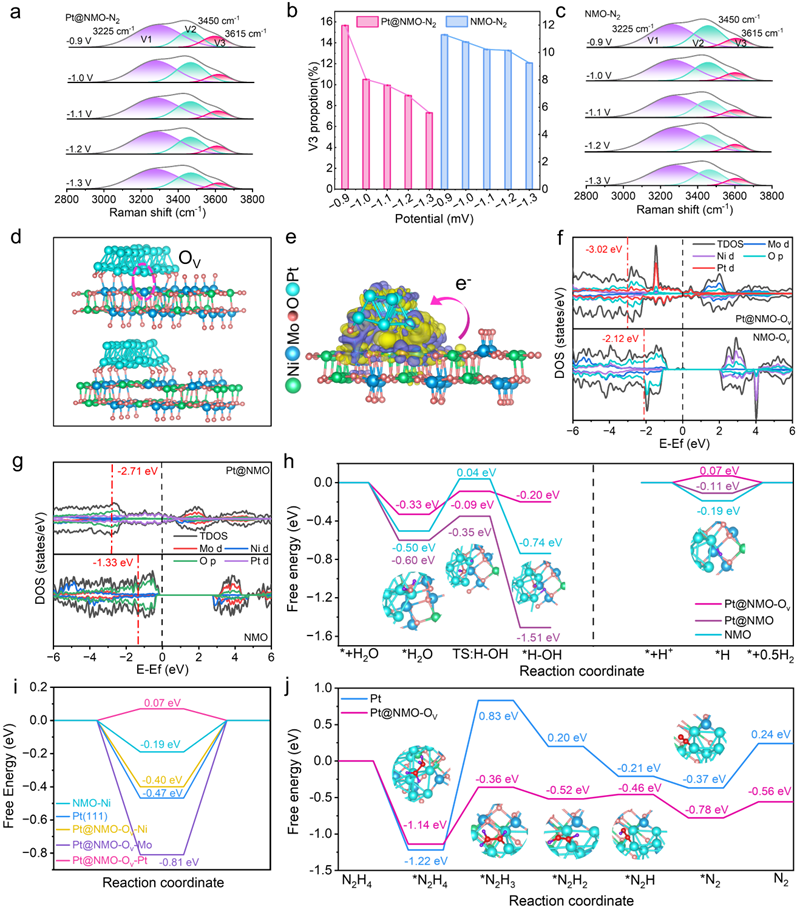
圖8. (a-c)不同電位下Pt@NMO-N2和NMO-N2的原位拉曼光譜;(d) 含氧空位(Ov)與否的Pt@NMO催化劑的原子模型;(e)Pt@NMO-Ov界面的電荷密度差;(f、g)Pt@NMO-Ov、NMO-Ov、Pt@NMO和NMO的DOS;(h) NMO、Pt@NMO和Pt@NMO-Ov表面H*演化的自由能圖;(i) 計算H*吸附的吉布斯自由能;(j) Pt和Pt@NMO-Ov表面的HzOR反應路徑。
在這項研究中,我們成功地構建了類銀柳花狀的Pt@NMO-N2異質結構電催化劑。精細結構表征和DFT計算表明,氧空位和 BEF的協同作用促進了水的解離,優化了氫的吸附/解吸。原位阻抗測試進一步證實,Pt@NMO-N2的HER反應動力學得到了優化,因此該催化劑只需要188 mV的過電位就能達到1500 mA cm-2電流密度。此外,Pt@NMO-N2 的超親水和超疏氣特性有效減少了雜質離子在電極表面的沉積,降低了Cl–對電極的腐蝕,使得該催化劑在堿性海水電解HER中僅需 232 mV就能達到1500 mA cm-2的電流密度。將自支撐 Pt@NMO-N2作為陰極組裝AEM電解槽,同樣表現出優異的催化活性,且能在在500 mA cm-2的電流密度下可連續產氫超300小時。此外,在肼氧化輔助制氫(HzOR/HER)系統中,Pt@NMO-N2(+) || Pt@NMO-N2 (–) 僅需0.32 V的驅動電壓即可達到500 mA cm-2。這些發現為高效電解(海)水制氫以及肼氧化輔助產氫催化劑的開發提供了試驗依據和理論基礎。
文章信息:
Interfacial Component Coupling Effects Induce Electron Redistribution for Enhanced Hydrazine‐Assisted Hydrogen Production at Ampere-Level Current Densities
Xinru Zhaoa,1, Hongshun Zhenga,1, Huachuan Suna,*, Mingpeng Chena, Boxue Wanga, Qingjie Lua, Bin Xiaoa, Tong Zhoua, Dequan Lia, Guoyang Qiua, Jin Zhanga, Yumin Zhanga Feng Liub, Tianwei Hea, Hui Panc, Chundong Wangd, Qingju Liua,*
文章鏈接:
https://doi.org/10.1016/j.nanoen.2025.111201








