酰胺是一類重要的羰基化合物,廣泛存在于天然產物、藥物分子和聚合材料之中。傳統的酰胺合成方法通過羧酸及其衍生物和胺類化合物在偶聯試劑活化下進行縮合反應制備,會產生大量的廢棄物,因此發展綠色、高效、高原子經濟性的酰胺合成新方法具有重要意義。
中國科學院蘭州化學物理研究所羰基合成與選擇氧化國家重點實驗室夏紀寶課題組一直致力于一氧化碳(CO)羰基化催化領域的研究。在他們團隊前期過渡金屬催化的氧化碳—氫羰基化制備(手性)內酰胺工作的基礎上(J. Org. Chem., 2019, 84, 3357;Org. Lett., 2019, 21, 1749),他們提出了一種制備酰胺的新策略:以CO為羰基源,通過金屬氮卡賓中間體,可能通過兩種途徑實現碳—氫酰胺化,異氰酸酯中間體(圖1,中間體I)或碳金屬中間體(圖1,中間體II)。
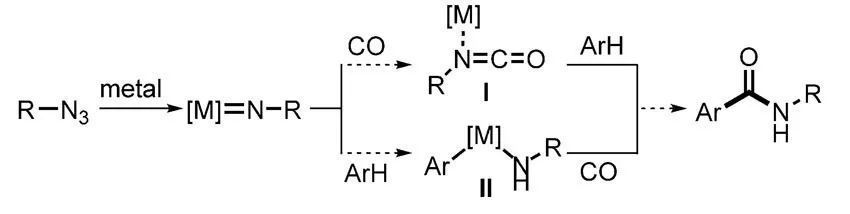
圖1. 研究策略
作者使用商業化的銠鹽或鈀鹽為催化劑、常壓下的CO作為羰基源、有機疊氮化合物作為氮源,實現了富電子(雜)芳烴的碳—氫酰胺化反應。作者首先以N-甲基、芐基、或苯基吲哚為底物,反應均能以優秀的收率得到目標化合物,當使用N上無保護基團的吲哚為底物時,反應也能夠以優秀的結果得到目標產物。最后作者考察了吡咯、甘菊藍、二甲基苯胺等一系列芳烴對反應的耐受性,發現反應在銠和鈀的催化下均表現出較高的反應活性。該反應首次通過金屬氮卡賓中間體實現了分子間碳—氫羰基化,氮氣是唯一副產物,且具有原料易得、反應簡單、條件溫和、綠色高效等優點。
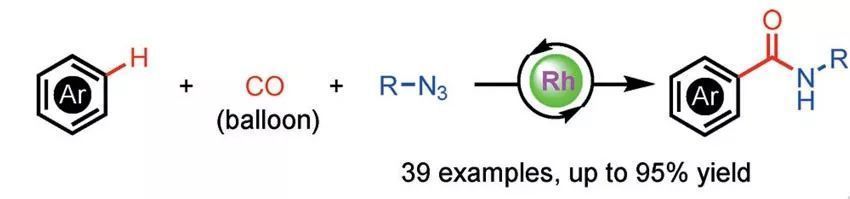
圖2. 分子間碳—氫酰胺化
通過控制實驗和理論計算,作者提出設想中的經由異氰酸酯中間體的反應途徑可能是合理的;金屬和疊氮化合物反應生成金屬氮卡賓,然后和CO反應得到異氰酸酯中間體,接著與富電子芳烴通過親電取代反應機理生成酰胺產物。
這一成果近期發表在《德國應用化學》(Angew. Chem. Int. Ed.)上,文章的第一作者是課題組科研助理元思文和博士研究生韓慧。理論計算部分由蘇州大學鮑曉光教授課題組完成,鹽城工學院的顧正洋博士為共同通訊作者。該研究工作得到國家自然科學基金委、江蘇省自然科學基金,中科院“百人計劃”等資助。








