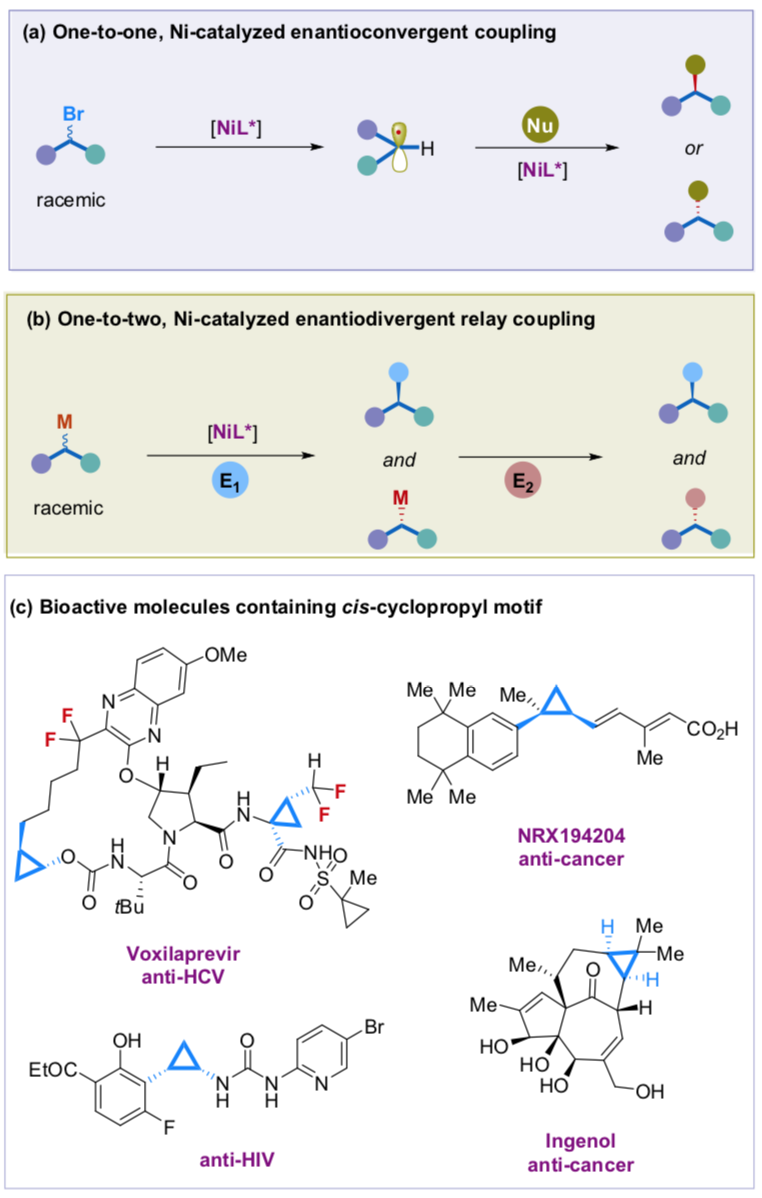
在不對稱合成反應領域中,從容易得到的起始分子出發是最合適的方法,其中過渡金屬催化將二級烷基親電試劑和有機金屬親核試劑之間的對映體收斂(enantioconvergent)偶聯反應在構建手性碳中心中展現了較好的反應性。但是在這種反應過程中,外消旋的二級烷基金屬親核試劑在這種偶聯反應中仍局限在特定的少量底物范圍中,這是由于其中立體結構中心的生成有一定難度導致。
近日,中科院上海有機化學研究所張新剛等報道了手性環丙烷的合成方法,通過外消旋無手性的環丙基鋅試劑作為反應物合成了包括二氟烷基化的環丙烷以及具有手性側鏈的環丙烷產物。這種方法中通過對映發散的兩步接力偶聯反應過程(enantiodivergent relay coupling)。
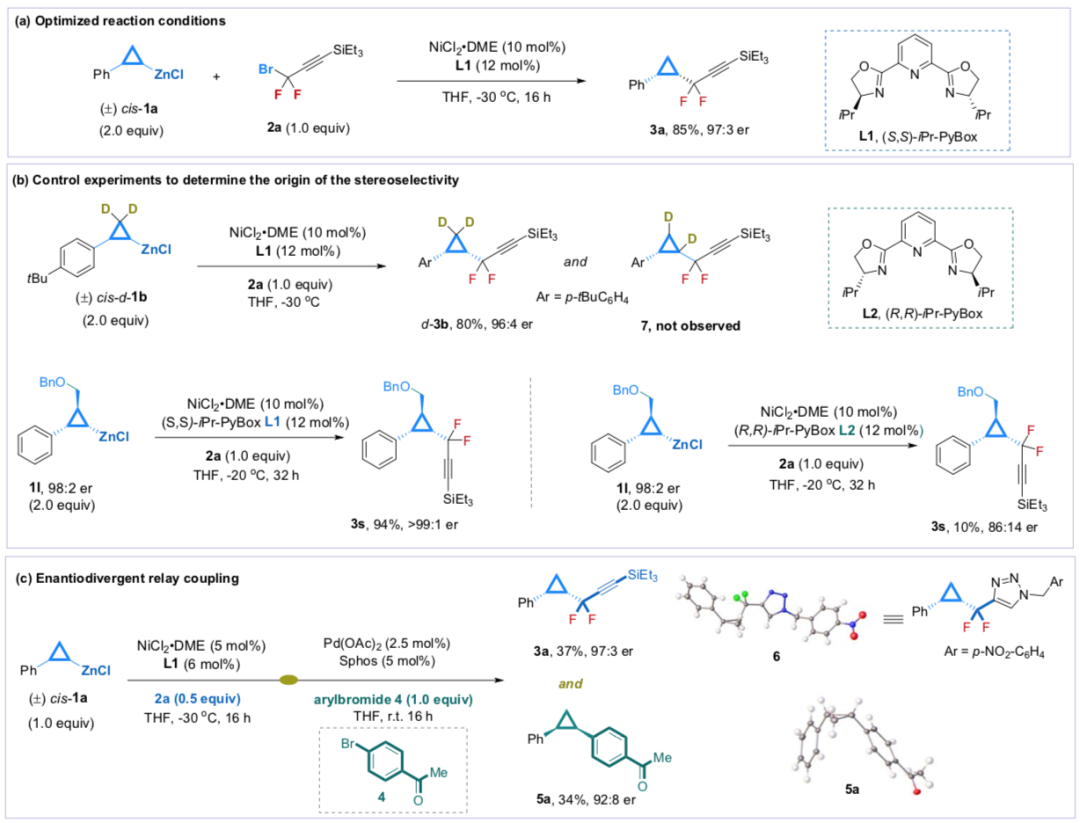
要點1. 反應優化。將環丙烷鋅、外消旋的二氟溴化物作為反應物,通過手性的12 mol %pyridine-2,6-bis(oxazoline)配體和10 mol % NiCl2·DME作為催化體系,在-30 ℃的THF中反應。該反應中能夠在16 h內以85 %的產率和97:3 er手性得到含環丙烷基手性二氟化物。對二氟化物分子進一步對其中的炔基轉化,能轉化為其他官能團分子。要點2. 通過接力兩步方法,在環丙烷上通過和NBS反應加成手性溴,隨后在金屬試劑反應,合成了一系列將環丙烷上的溴取代并安裝手性取代基(PPh2、BPin、SiPh2Me、SPh、CO2H、CONMe2、CN等)。Lun An, Fei-Fei Tong, Shu Zhang, and Xingang Zhang*. Stereoselective Functionalization of Racemic Cyclopropylzinc Reagents via Enantiodivergent Relay Coupling, J. Am. Chem. Soc. 2020https://pubs.acs.org/doi/10.1021/jacs.0c04462