由于金屬Cu大量,廉價,低毒,因此Cu催化或導向的C-H官能化得到了廣泛的關注。自從發現金屬Cu具有官能化芳烴C-H鍵的能力后,開發了各種C-H活化反應。值得注意的是,Cu(Ⅱ)能夠催化Pd催化劑不能實現的反應,并且Cu催化劑也對雜環具有出色的容忍性。但是,與Pd催化的C-H官能化相比,Cu催化的C-H官能化仍處于早期階段。

多取代烯烴和二烯骨架在天然產物和有機材料中廣泛存在,是許多氧化和還原反應中常用的合成子。C-H與乙烯基硼的偶聯是合成此類化合物具有吸引力的途徑。最近,Daugulis,Piguel,Charette等人報道了了在強堿條件下,酸性C-H和乙烯基鹵化物的直接烯基化反應,Li,Chen和Chang等使用烯丙基鹵化物實現了酸性更強的芳基C-H鍵的烯基化(Scheme 1a)。近日,美國Scripps研究所余金權課題組在 Organic letters 報道了在噁唑啉-苯胺導向基團的協助下,Cu(Ⅱ)催化的苯甲酸和烯丙酸衍生物與乙烯基硼酸酯的烯基化反應構建各種多取代烯烴和二烯化合物。(DOI:10.1021/acs.orglett.0c01469)
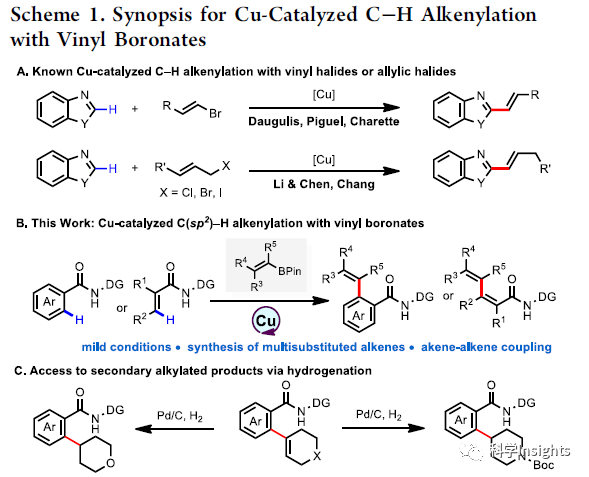
首先,作者使用易于脫去的噁唑啉-苯胺為導向基團進行條件篩選,發現底物1a和(E)-1-戊烯基硼酸頻哪醇酯(2)在此前芳基化的條件下交叉偶聯得到單烯基化產物(產率:7%)和羥基化副產物(產率:11%)。作者進一步系統的篩選了Cu催化劑,溶劑,溫度(Scheme 2),發現在N2保護下,溫度45℃,苯甲酸銅(II)(30 mol%),Ag2O(2.0 equiv),KOPiv(2.0 equiv),KHCO3(2.0 equiv),DMSO(2.0 mL)為最優反應條件。對照實驗表明:若缺少苯甲酸銅(II)和堿,反應不能發生;若缺少Ag2O,則僅得到痕量的產物;KOPiv,KHCO3對反應的產率至關重要。

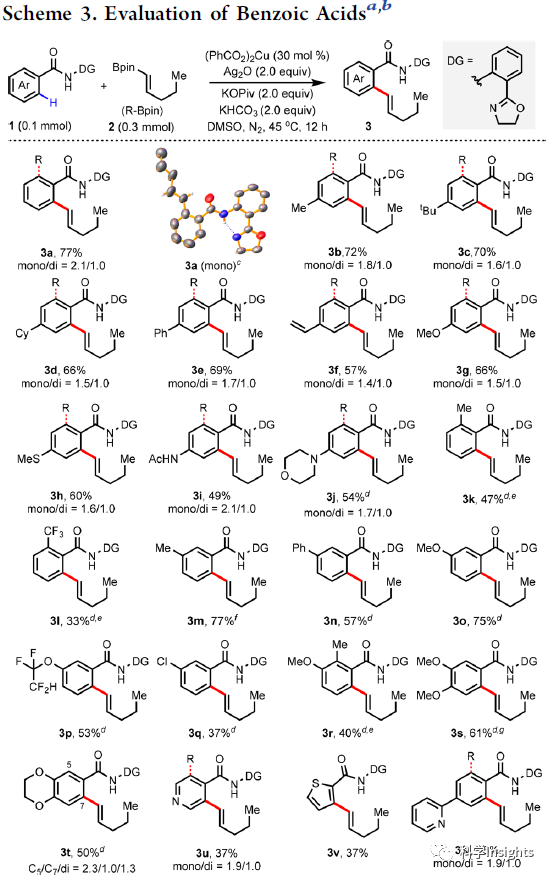
在最優的反應條件下,作者以(E)-1-戊烯基硼酸頻哪醇酯(2)為烯基化試劑評價了苯甲酸的底物范圍(Scheme 3)。相對于間位和鄰位取代的苯甲酸,鄰位取代的苯甲酸產率較低(3k,3l)。對位取代的底物以較高的產率得到單,雙產物混合物(3b-3j,3w),由于空間位阻,間位取代的底物僅發生單烯基化(3m-3r)。雜環底物也能參與該烯基化反應,但是收率較低(3u-3w)。
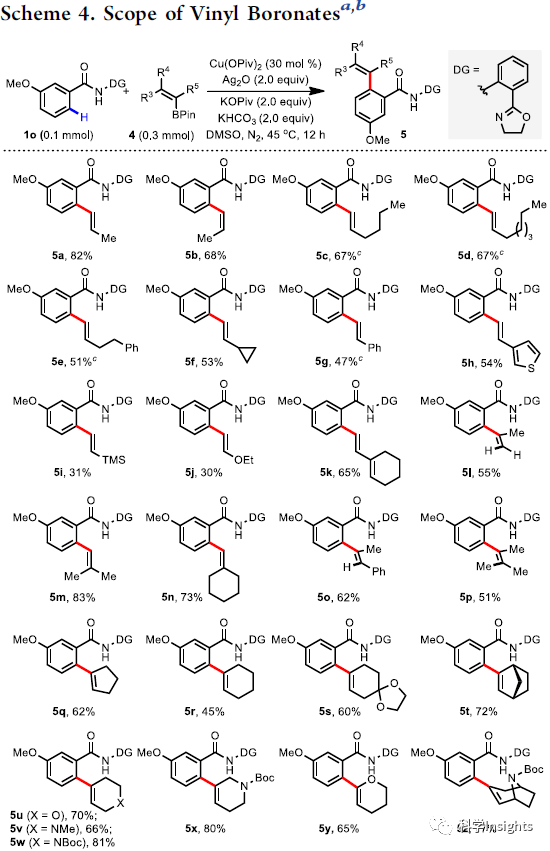
接著,作者以1o為模型底物評價了烯基硼酸酯的適用性(Scheme 4)。順,反乙烯基硼酸酯均能以較高的產率得到順式或反式的烯烴(5a,5b),各種烷基乙烯基硼酸以51-82%的收率得到相應的產物(5a-5f),苯乙烯和雜環苯乙烯衍生的偶聯劑也對該反應具有容忍性(5g,5h),對堿或酸敏感的烯基化試劑,四甲基硅烷(TMS)-乙烯基,乙烯基醚和二烯等對酸或堿敏感的烯基化試劑均能交叉偶聯得到所需產物(5i-5k)。此外,二取代(4m-4o),三取代(4p)和環狀乙烯基硼酸酯(4q-4t)都是合適的偶聯劑,各種雜環烯基硼酸酯對該反應具有兼容性,得到各種新穎的雜烯基化的芳烴化合物(5u?5z)。
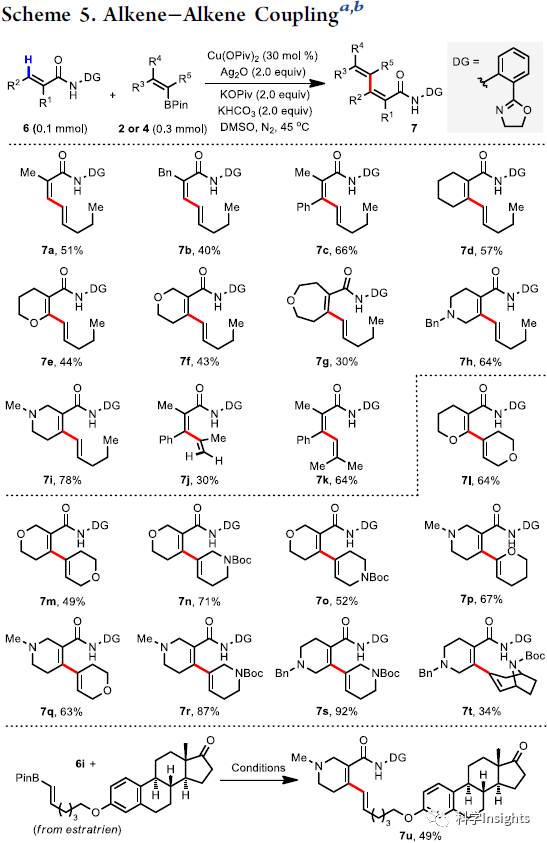
考慮到二烯烴在合成中的重要性,并且在活性分子中廣泛存在,作者探究了乙烯基C-H鍵與乙烯基硼酸酯的直接偶聯(Scheme 5)。各種烯烴在該溫和的反應條件下以30%-78%的產率得到相應的二烯化合物(7a?7k)。雜環底物對該反應也具有兼容性,能夠以較高產率得到烯基化的雜環(7e?7i),也可以直接與雜環烯基硼酸酯高效的偶聯(7l?7t)。6i與雌激素衍生的乙烯基硼酸酯的直接偶聯證明了在復雜生物活性分子后期官能化中的通用性。
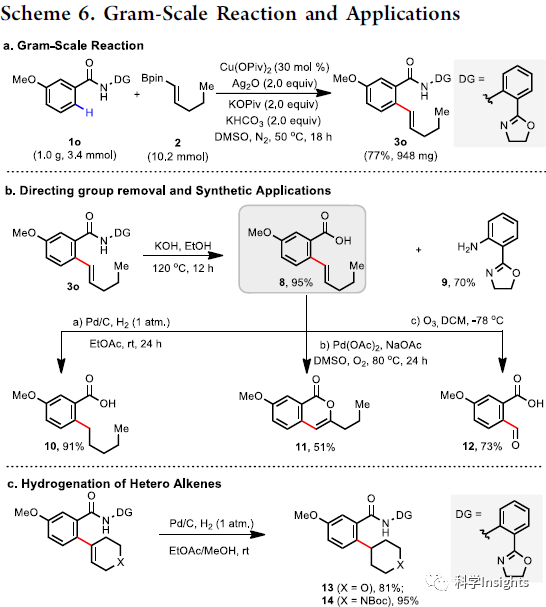
作者通過1o(1g)和(E)-1-戊烯基硼酸頻哪醇酯(2)的反應證明了該反應的可擴展性(Scheme 6a),且導向基團在堿性的條件下能夠輕易的脫去。反應生成的烯基苯甲酸是重要的有機合成中間體,能夠轉化為烷基苯甲酸(10),內酯(11),和醛(12)(Scheme 6b)。雜環烯烴衍生物的氫化反應分別以81%和95%的收率得到烷基化四氫吡喃(13)和哌啶(14)(Scheme 6c)。
總結:余金權課題組報道了在噁唑啉-苯胺導向基團的協助下,Cu(Ⅱ)催化的苯甲酸和烯丙酸衍生物與乙烯基硼酸酯的烯基化反應構建各種多取代烯烴和二烯化合物,該反應具有條件溫和,官能團范圍廣,雜環對該反應也具有容忍性等特點。














