分享一篇發表在ACS Central Science上的文章,題目為“Visible Light Induced Mukaiyama Reagent Promoted Desulfurative Modification of Peptides and Proteins with Nucleotides”,通訊作者是蘭州大學基礎醫學院的許兆青教授,其研究方向是藥物分子的設計合成以及熒光分子探針。

肽和蛋白質的位點選擇性修飾是生物學研究和治療開發的有力工具。之前的研究探究了將Cys變為脫氫丙氨酸進而利用Michael加成構建C-C鍵的方法,但卻丟失了天然立體化學,而使用膦還原劑的策略雖然通過立體化學保留的自由基實現偶聯,但卻與二硫鍵不兼容,且紫外光的生物相容性不好。同時廣泛采用的Cys偶聯彈頭如馬來酰亞胺和二硫鍵存在可逆行為的局限性。
尿嘧啶類似物6-氮雜嘧啶的核糖核苷已顯示出多種生物活性,本文報告了肽和蛋白質與 6-氮雜嘧啶C5位的核酸通過Cys殘基的可見光促進立體保留脫硫的新型位點特異性偶聯。本文的第一部分就進行了這個反應的條件優化,并進一步提高其位點選擇性。證明了其偶聯特異性發生在Cys與6-氮雜嘧啶之間,且兼容二硫鍵,作者在具有多個反應性側鏈的線性肽以及環肽上證明了其實現蛋白質和寡核苷酸的精確偶聯的能力。
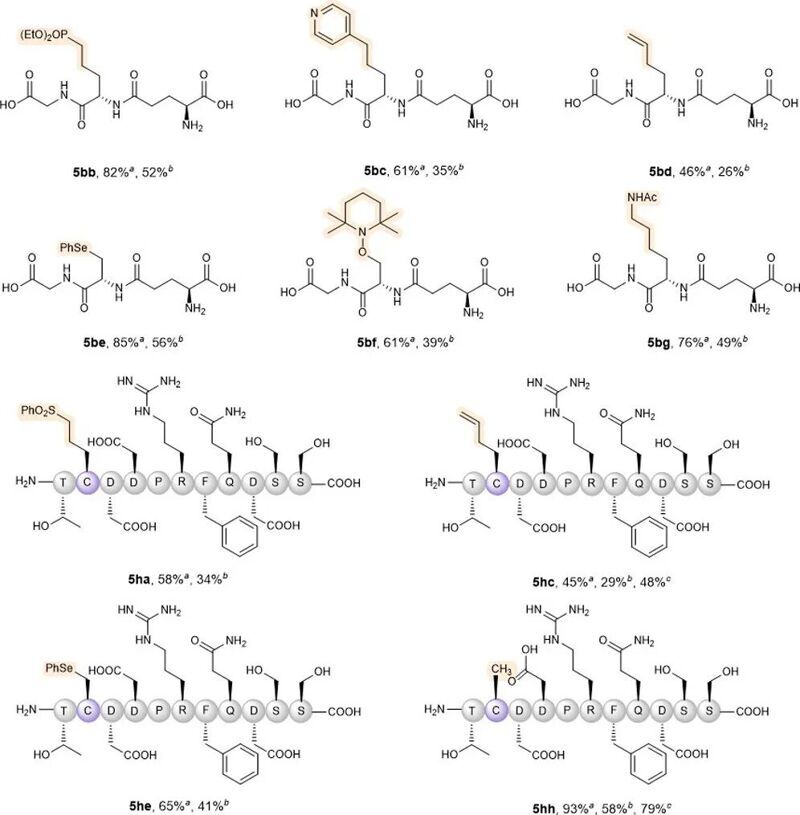
為了擴展該策略的適用性,作者用研究了它與一系列自由基受體(如苯基乙烯基砜)的反應性。作者發現在原體系的基礎上,加入Hantzsch 酯或NADH作為還原劑,可以實現Cys與多種自由基受體的脫硫可見光促進的偶聯。
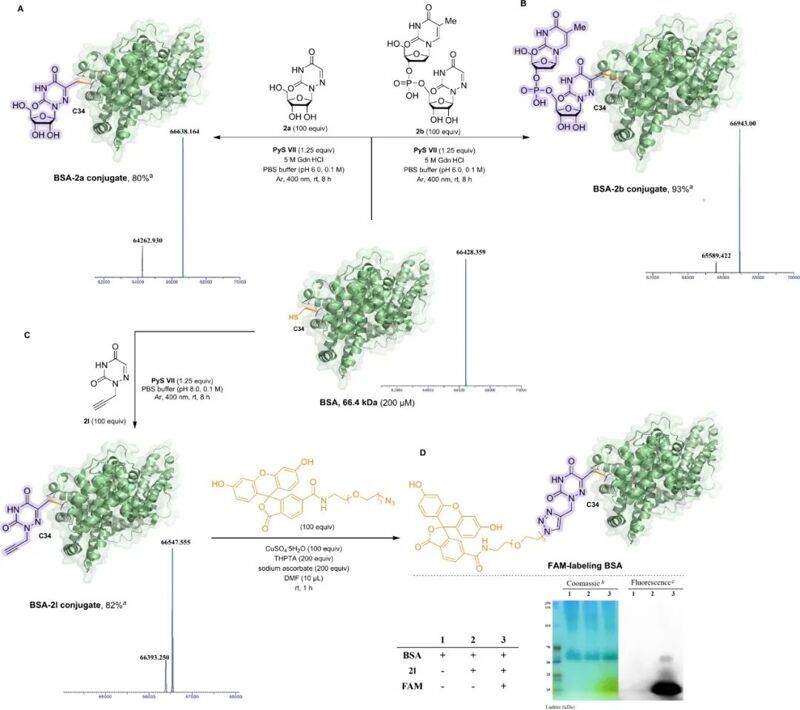
最后作者將這一策略擴展到復雜的蛋白質功能化,以BSA作為模型蛋白,作者成功將BSA與帶炔基的6-氮雜嘧啶偶聯,并通過 CuAAC 與 FAM 染料的點擊化學進行有效的熒光標記。
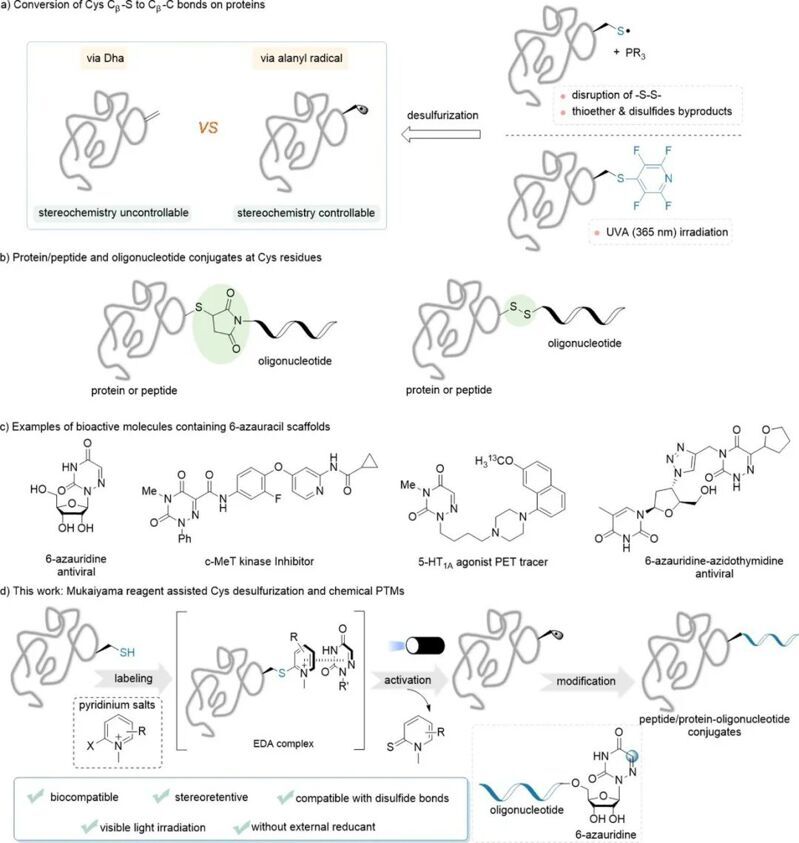
總的來說,本文開發了一種新的策略,通過在可見光活化下通過吡啶鹽定向的 Cys 殘基脫硫對肽和蛋白質進行位點選擇性立體保留修飾。
本文作者:YDP
責任編輯:LYC
DOI:10.1021/acscentsci.5c01241
原文鏈接:https://doi.org/10.1021/acscentsci.5c01241








